Zellen schützen sich kontrolliert vor freien Radikalen
Rückkopplungsmechanismus koordiniert zelluläre Atmung und Abbau freier Sauerstoffradikale
Durch zelluläre Atmung, also die Umwandlung von Kohlenhydraten und Sauerstoff zu Kohlendioxid und Wasser, gewinnen sauerstoffverbrauchende Organismen Energie. Dabei entstehen aber toxische Sauerstoffradikale, die sofort abgebaut werden müssen, da sie sonst die Zellen schädigen würden. Wissenschaftler des Max-Planck-Instituts für molekulare Genetik in Berlin haben jetzt einen Mechanismus entdeckt, mit dem Zellen die Atmungsaktivität und den Abbau freier Radikale koordinieren können. Zellen bereiten also ihren Stoffwechsel auf freie Radikale vor, bevor diese überhaupt entstehen.
Die zelluläre Atmung ist ein sehr effizienter Prozess, um aus wenigen Molekülen Zucker und Sauerstoff viel Energie zu gewinnen. Allerdings werden bis zu zwei Prozent des verbrauchten Sauerstoffs zu Superoxid umgewandelt, einem für Zellen toxischen, freien Radikal. Ein beachtlicher Teil dieses Superoxids entweicht der Atmungskette der Mitochondrien und stellt eine Gefahr für biologische Makromoleküle wie DNA, RNA, Proteine und Fettsäuren dar. Allerdings hat die Evolution eukaryontische Zellen mit umfangreichen Mechanismen ausgestattet, die diese in der Zelle entstehenden freie Radikale abbauen und so Schäden verhindern können. Diese Mechanismen arbeiten hoch effizient und gut koordiniert, so dass entgegen der landläufigen Meinung die Behandlung gesunden Gewebes mit Antioxidantien das natürliche Gleichgewicht stören und im schlimmsten Fall sogar Zellen schädigen und den Alterungsprozess beschleunigen kann.
Forscher am Max-Planck-Institut für molekulare Genetik haben nun atmende mit nicht atmenden Hefezellen verglichen. Wurde die Atmung aktiviert, stieg unmittelbar die Toleranz gegenüber oxidierenden Substanzen, jedoch nicht, wie erwartet, die Konzentration freier Radikale in der Zelle. Atmende Zellen waren also durchaus in der Lage, mit der erhöhten Bildung von freien Radikalen umzugehen und sie auf dem Niveau nicht-atmender Zellen zu halten.
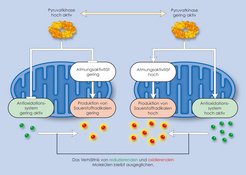
Den Forschern zufolge ist eine bisher unentdeckte Rückkopplung innerhalb eines zentralen Stoffwechselweges für diesen Prozess verantwortlich. Das kohlenhydrat-abbauende Enzym Pyruvatkinase reguliert die Atmungsaktivität von Hefezellen. In atmenden Zellen ist es weniger aktiv, was zu einer Anreicherung seines Substrats Phosphoenolpyruvat führt. Die Akkumulation dieser Substanz hemmt ein anderes Enzym der Glykolyse, die Triosephosphat-Isomerase. Dieses Enzym ist den Forschern bestens bekannt - bereits früher hatten sie entdeckt, dass eine geringe Aktivität dieses Enzyms vor freien Radikalen schützt. „Wenn wir diesen Rückkopplungsmechanismus künstlich unterbinden und die Atmung aktivieren, steigt die freie Radikal-Konzentration in den atmenden Zellen stark an und schädigt Proteine und Mitochondrien. Zellen können also frühzeitig erkennen, wann eine erhöhte Radikal-Produktion auftreten wird und ihren Stoffwechsel schon anpassen, bevor es überhaupt zur Produktion der freien Radikale kommt“, erklärt Markus Ralser vom Max-Planck-Institut für molekulare Genetik.
Diese Entdeckung ist möglicherweise von besonderer Bedeutung für die Krebsforschung. Denn das Enzym Pyruvatkinase ist mit dafür verantwortlich, dass Tumorzellen meist weniger atmen und dafür mehr Zuckerstoffwechsel betreiben als gesundes Gewebe. Dieser Effekt ist nach Otto Warburg genannt, der in den 1920er Jahren erstmals einen erhöhten Zuckerstoffwechsel in Krebszellen nachweisen konnte. Die Forscher hoffen nun, dass der neu entdeckte Rückkoppelungsmechanismus benutzt werden kann, um in Tumorzellen einen gezielten Nährstoffmangel auszulösen und sie dadurch angreifbar zu machen.
HR












