Forschungsbericht 2019 - Max-Planck-Institut für Biologie des Alterns
Umprogrammierung von Mitochondrien bei Krebserkrankungen
Flexibler Stoffwechsel erfordert flexible Mitochondrien
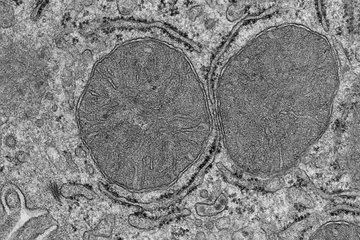
Unsere Zellen sind von faszinierenden, stammesgeschichtlich sehr alten Organellen bevölkert, die Mitochondrien genannt werden. Sie sind aus sauerstoffverwertenden Bakterien entstanden, die vor über einer Milliarde Jahren von Vorformen der heutigen eukaryontischen Zelle aufgenommen wurden. Wenn man sieht, wie dynamisch diese Organellen unter dem Mikroskop ihre Struktur verändern, erhält man einen Eindruck, wie schnell sich Mitochondrien anpassen können, um ihre zahlreichen Funktionen für den Stoffwechsel in den verschiedenen Zellen unseres Körpers sicherzustellen.
Mitochondrien dienen als zelluläre Kraftwerke und verbrennen Sauerstoff, um Energie in einer metabolisch verwertbaren Form bereitzustellen. Neben dieser klassischen Rolle im Zellstoffwechsel erzeugen die Mitochondrien auch zahlreiche metabolische Bausteine, die für das Zellwachstum benötigt werden. Mit zunehmendem Alter nehmen jedoch mitochondriale Aktivitäten ab, was vermutlich entscheidend zu Alterungsprozessen beiträgt. Tatsächlich verursachen mitochondriale Fehlfunktionen eine Vielzahl von menschlichen Krankheiten wie Neurodegeneration, Herzkrankheiten und Diabetes. Die Zellen haben daher verschiedene Mechanismen etabliert, um die Qualität ihrer Mitochondrien zu erhalten und die mitochondriale Aktivität als Reaktion auf veränderte Stoffwechselanforderungen zu optimieren. Diese Mechanismen hängen von der inhärenten Plastizität oder Flexibilität der mitochondrialen Population ab.
Wie unter dem Mikroskop zu beobachten, bilden Mitochondrien dynamische Netzwerke in einer Zelle und können verschmelzen und fragmentieren. Veränderungen in Größe oder Form sind eng mit Änderungen in der mitochondrialen Funktion verbunden. Beispielsweise fragmentiert das mitochondriale Netzwerk mit zunehmendem Alter der Zellen. Auch kann es für Zellen von Vorteil sein, überschüssige Mitochondrien zu zerkleinern und abzubauen, um sich an niedrige Sauerstoffwerte oder mangelnde Nährstoffe anzupassen [1]. Es zeigt sich aber auch, dass die Stoffwechselaktivität der verbleibenden Mitochondrien umprogrammiert und optimiert werden muss, um das Überleben der Zellen unter diesen schwierigen Bedingungen zu sichern.
Krebserkrankungen programmieren Mitochondrien und ihren Stoffwechsel neu
Viele massive Tumore entwickeln sich ohne ausreichende Blutversorgung einzelner Krebszellen, was zu Sauerstoff- und Nährstoffmangel führt. Dies ist zum Beispiel im Falle des Bauchspeicheldrüsenkrebses der Fall, der sich durch eine hypoxische, das heißt sauerstoffarme, und nährstoffarme Mikroumgebung auszeichnet. Wenn wir verstehen wollen, wie Krebszellen unter diesen Bedingungen gedeihen können, ist es notwendig zu untersuchen, wie Zellen dabei die Mitochondrien umprogrammieren. Wir können die Mikroumgebung von Krebs in Gewebekulturen nachahmen und auch direkt in lebenden Organismen untersuchen, um die Reaktion und den Beitrag der Mitochondrien zur Tumorgenese aufzuklären. Die Aufdeckung metabolischer Schwachstellen von Krebszellen in diesen Umgebungen birgt ein enormes therapeutisches Potenzial.

Unsere jüngste Arbeit hat einen neuen Mechanismus aufgedeckt, mit dem Krebszellen ihre Mitochondrien schnell neu programmieren können, um auf die widrigen Herausforderungen in wachsenden Tumoren zu reagieren [2]. Wir fanden, dass die Aktivität eines mitochondrialen proteinabbauenden Enzyms, einer Protease, in hypoxischen und nährstoffarmen Krebszellen erhöht ist (Abb. 1). Zellen können einen Sauerstoff- oder Nährstoffmangel detektieren und ein Teil ihrer Reaktion besteht darin, den proteolytischen Abbau bestimmter mitochondrialer Proteine zu stimulieren. Diese Neuprogrammierung des mitochondrialen Proteingehalts erfolgt an der inneren Mitochondrienmembran, die als wichtiger Kontrollpunkt für die Verwendung und Versorgung von Zellen mit Metaboliten dient. Entscheidend ist, dass die Steigerung der Proteolyse auf reversible Weise erfolgt, sodass sich die Proteinzusammensetzung der Mitochondrien wieder ändern kann, sobald sich der Sauerstoff- oder Nährstoffgehalt normalisiert.
Mitochondrien sind potenzielle therapeutische Ziele bei Bauchspeicheldrüsenkrebs
Was passiert, wenn wir die Fähigkeit von Krebszellen blockieren, ihre Mitochondrien neu zu programmieren? Tatsächlich unterdrückt die Deletion derjenigen Protease, die für die mitochondriale Programmierung bei Hypoxie und Hunger verantwortlich ist, das Wachstum von Bauchspeicheldrüsenkrebszellen in Zellkulturen und nach Injektion in Mäusen. Ähnliche Effekte wurden auch beobachtet, als wir in den Signalweg zur Regulierung dieser Protease eingriffen. Wir analysierten Tumorgewebe von Krebspatienten und erhielten Hinweise, dass bei den schwer hypoxischen Bauchspeicheldrüsentumoren tatsächlich eine signifikante Umprogrammierung der Mitochondrien stattgefunden hatte.
Bauchspeicheldrüsenkrebs hat die niedrigste Überlebensrate aller Krebsarten in Europa und es gibt derzeit keine wirksamen Behandlungen. Es ist sehr Besorgnis erregend, dass die Zahl der Patienten, die an dieser schrecklichen Krankheit leiden, in den alternden Bevölkerungen zunehmen wird [3]. Wir nehmen an, dass die Umprogrammierung der Mitochondrien in proliferierenden Tumorzellen zur Entstehung einer metabolischen Signatur von Bauchspeicheldrüsenkrebs beiträgt [4]. Wir sind daher bestrebt, die mitochondriale Umprogrammierung bei Krebs, wie hier beschrieben, vollständig zu verstehen und nachfolgend das therapeutische Potenzial zu erforschen, um diesen Prozess zu beeinträchtigen – und damit den Krebs zu besiegen.