Weniger Versuchstiere dank sekundärer Nano-Antikörper
Max-Planck-Forscher entwickeln Alternative zu den meistgenutzten Antikörpern und ihrer ethisch umstrittenen Produktion in Versuchstieren
Antikörper sind aus biologischer Forschung und medizinischer Diagnostik nicht mehr wegzudenken. Sie herzustellen ist jedoch zeitintensiv, kostspielig und erfordert den Einsatz vieler Tiere. Wissenschaftler am Max-Planck-Institut für biophysikalische Chemie in Göttingen haben nun sogenannte sekundäre Nanobodies entwickelt, die die meistgenutzten Antikörper ersetzen und die Anzahl der Tiere in der Antikörper-Produktion drastisch reduzieren können. Das ist möglich, weil sich die Sekundär-Nanobodies in praktisch unbegrenzter Menge in Bakterien herstellen lassen. Außerdem haben die sekundären Nanobodies bei vielen zellbiologischen Methoden Vorteile gegenüber ihren Antikörper-Pendants.

Als zentraler Teil des Immunsystems schützen Antikörper uns Menschen und andere Wirbeltiere vor Krankheitserregern. Darüber hinaus sind sie unverzichtbare Werkzeuge in der medizinischen Diagnostik, der Therapie und der Grundlagenforschung – zum Beispiel in der Mikroskopie. Wenn Forscher ein bestimmtes Protein in einer Zelle mikroskopisch untersuchen wollen, markieren sie es mit Antikörpern, die gegen das gewünschte Protein gerichtet sind. Haben diese sogenannten primären Antikörper an das Zielprotein gebunden, kommen in einem zweiten Schritt sekundäre Antikörper zum Einsatz. Diese wiederum binden an die primären Antikörper und können etwa mit einem Fluoreszenzfarbstoff gekoppelt sein, der schließlich unter dem Mikroskop leuchtet und so das Protein sichtbar macht.
Die Produktion der sehr vielfältigen Primär-Antikörper erfolgt traditionell in kleinen Säugern wie Mäusen oder Kaninchen: Die Tiere werden zunächst mit einem gereinigten Protein per Spritze immunisiert – vergleichbar mit einer Schutzimpfung beim Menschen. Daraufhin bildet das Immunsystem der Tiere Antikörper gegen das Protein. Die Antikörper werden schließlich aus dem Blut der Tiere gesammelt und aufbereitet. Da tausende Labors weltweit Antikörper nutzen und fast alle diese Anwendungen sekundäre Antikörper erfordern, ist der Bedarf für letztere enorm. Deshalb sind für die Sekundär-Antikörper-Produktion nicht nur viele, sondern auch große Tiere wie Esel, Ziegen oder Schafe nötig, was ein ethisches Problem darstellt.
Sekundäre Nanobodies aus Bakterien
Forscher am Max-Planck-Institut für biophysikalische Chemie in Göttingen haben jetzt eine nachhaltige Alternative vorgestellt, die Sekundär-Antikörper gegen primäre Antikörper aus Mäusen und Kaninchen komplett ersetzen und somit die Zahl benötigter Tiere für die Antikörper-Herstellung drastisch reduzieren kann – dank spezieller Nanobodies. Nanobodies sind Fragmente besonders einfach aufgebauter Mini-Antikörper aus Kamelen und ihnen verwandten Arten wie Alpakas. „Wir haben Sekundär-Nanobodies entwickelt, die sich – ähnlich wie Bier in einem Fermenter – mikrobiologisch in beliebiger Menge produzieren lassen“, erklärt Dirk Görlich, Direktor am Göttinger Max-Planck-Institut und Leiter des Projekts. Mit herkömmlichen Antikörpern ist diese Herstellungsart aufgrund ihrer komplexen Struktur nicht möglich.
„Die Qualitätsanforderungen für Sekundär-Antikörper sind sehr hoch, weil sie nur Primär-Antikörper aus einer einzigen Tierart und keinerlei Strukturen in den zu analysierenden Zellen oder medizinischen Proben erkennen dürfen. Das Problem war also, Baupläne für wirklich perfekte Sekundär-Nanobodies in die Hände zu bekommen. Begonnen haben wir mit einer Vielzahl von Bauplan-Varianten, die wir aus einer kleinen Menge Blut von zwei immunisierten Alpakas extrahiert haben. Durch ein sogenanntes „Phage-Display“-Verfahren haben wir dann die besten Varianten herausgefischt und mit diesen schließlich Bakterien für die Nanobody-Produktion programmiert“, erläutert Tino Pleiner, Erstautor der jetzt erschienenen Arbeit.
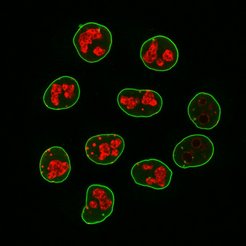
Nanobodies wurden erstmals 1993 von einem belgischen Labor beschrieben. Seitdem versuchen Forscher, sie sich für ihre Arbeit im Labor zunutze zu machen. Speziell der Ersatz von Sekundär-Antikörpern ist allerdings alles andere als trivial. Ein Grund dafür ist die Größe der Nanobodies: Sie sind zehnfach kleiner als normale Antikörper. Daher bieten sie weit weniger Fluoreszenzfarbstoff-Molekülen Platz als konventionelle Antikörper und sollten im Mikroskop viel weniger hell leuchten als diese. „Unsere ersten Versuche mit Sekundär-Nanobodies waren in der Tat sehr enttäuschend und lieferten nur dunkle und verrauschte Bilder. Wir haben aber nicht aufgegeben, sondern die beiden Alpakas nach einer einjährigen Pause ein weiteres Mal immunisiert und damit ihr Immunsystem dazu gebracht, die Nanobodies weiter zu verbessern. Die Evolution im Reagenzglas, eine spezielle Kopplungsstrategie für die Fluoreszenzfarbstoffe und der gleichzeitige Einsatz mehrerer Nanobodies taten dann das Übrige“, berichtet Görlich über anfängliche Schwierigkeiten. Jetzt können die Nanobodies in Sachen Signalstärke mit herkömmlichen Antikörpern mithalten.
Mehr Details im Mikroskop
Im Labor haben Nanobodies darüber hinaus sogar Vorteile gegenüber sekundären Antikörpern. „Mit höchstauflösender Fluoreszenzmikroskopie beispielsweise kann man theoretisch zelluläre Strukturen im Bereich von wenigen Nanometern optisch voneinander trennen. Doch die dabei verwendeten konventionellen Antikörper haben selbst eine Größe von 15 Nanometern. Das lässt das Bild wieder verschwimmen. Nanobodies hingegen sind mit etwa drei Nanometern deutlich kleiner, was eine höhere Bildschärfe erlaubt“, so Pleiner. „Neben der Mikroskopie haben wir die sekundären Nanobodies bereits mit anderen Methoden getestet und die Ergebnisse sind sehr vielversprechend“, betont Görlich. „Wir erwarten, dass unsere Nanobodies die traditionellen Sekundär-Antikörper aus Eseln, Ziegen oder Schafen in vielen Anwendungen ersetzen werden.“
ad/HR