Forschungsbericht 2013 - Max-Planck-Institut für Infektionsbiologie
Vektorbiologie – Ein Musterbeispiel für Wirt-Erreger-Beziehungen
Vector biology - a paradigm of host–pathogen interactions
Insekten und durch sie verbreitete Krankheiten
Blutsaugende Insekten verursachen durch die Übertragung von gefährlichen Krankheiten wie Malaria, Dengue-Fieber, Gelbfieber und West-Nil-Fieber ernstzunehmende medizinische und sozioökonomische Probleme. Über 700 Millionen Menschen weltweit sind jährlich betroffen. Um die Übertragung dieser Krankheiten zu kontrollieren und einzudämmen, ist das Verständnis der Biologie der Überträgerinsekten von entscheidender Bedeutung.
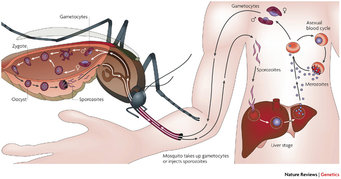
Die Malaria ist eine klassische Infektionskrankheit, von der die Hälfte der Menschheit bedroht ist. Obwohl sie weit verbreitet vorkommt, ist der afrikanische Kontinent südlich der Sahara am stärksten betroffen. Beim Menschen wird die Malaria durch fünf Spezies eines einzelligen Parasiten der Gattung Plasmodium (P. falciparum, P. vivax, P. ovale, P. malariae P. knowlesi) verursacht. Der gefährlichste darunter ist P. falciparum, der in Afrika vorherrscht und zum Tod eines befallenen Menschen führen kann. Malaria-Parasiten entwickeln sich in zwei verschiedenen Wirten: Der ungeschlechtliche Teil des Lebenszyklus findet in Säugern, einschließlich des Menschen, statt, während sich der geschlechtliche Teil in der Mücke vollzieht (Abb. 1). Malaria kann von Mensch zu Mensch nur durch den Stich einer infizierten weiblichen Mücke der Gattung Anopheles übertragen werden. Obwohl der Parasit nur aus einer einzigen Zelle besteht, verändert er während seiner Entwicklung mannigfaltig die Gestalt und kann so in verschiedene Organe und Zellen eindringen. Im Säugerwirt verbirgt sich der Parasit die meiste Zeit innerhalb von Leberzellen und roten Blutkörperchen, wohingegen er in der Mücke meist extrazellulär vorkommt [1].
Der Kreislauf im Menschen
Plasmodium-Zellen, Sporozoiten genannt, werden durch den Stich einer weiblichen Mücke eingeschleust. Sie wandern zur Leber und vermehren sich in den Leberzellen (Hepatozyten). Die entstehenden runden Formen, Merozoiten genannt, brechen die Leberzellen auf, um in die Blutbahn und dort in das Innere der roten Blutkörperchen (Erythrozyten) zu gelangen. Dort erfolgt die Vermehrung der Parasiten durch sich wiederholende Zyklen von Eindringen, Wachstum und Teilung. Durch den massiven Anstieg an befallenen roten Blutkörperchen im Blutkreislauf kommt es zu vielen Krankheitssymptomen und Komplikationen. Im Laufe dieser Infektion des Blutstroms, die unbehandelt Monate dauern kann, verändern sich einige Merozoiten und bilden geschlechtlich differenzierte Zellen (männliche und weibliche Gametozyten) aus. Diese Gametozyten entwickeln sich im Säugerwirt nicht weiter, sondern warten im Blutkreislauf darauf, bis sie nach einem Stich von einer Mücke aufgenommen werden, um dort Zygote und Oocyste zu bilden (Abb. 1).
Der Kreislauf in der Mücke
Während der Blutaufnahme nimmt die Mücke zusammen mit den Blutzellen die Gametozyten in ihren Darm auf. Dort entwickeln sie sich zu reifen weiblichen und männlichen Gameten, die die roten Blutkörperchen verlassen und sich zu Zygoten paaren. Diese entwickeln sich zu beweglichen Ookineten, durchlaufen den Darm der Mücke und sammeln sich auf der basalen Seite in Form von Oozysten an. Wachstum und Teilung jeder Oozyste erzeugt Tausende von aktiven haploiden Sporozoiten, die aus der Oozyste ausbrechen und in die Speicheldrüsen der Mücke eindringen, wo sie, so lange die Mücke lebt, verweilen. Sobald die Mücke sticht, werden die Sporozoiten in den neuen Wirt injiziert und ein neuer Ansteckungszyklus beginnt (Abb. 1).
Die Immunität der Mücke erforschen
Evolutionsbedingt ernähren sich Mücken und andere Insekten von Blut, das für ihre Fortpflanzung unerlässlich ist. Das Blutsaugen wiederum bietet Krankheitserregern, die sich in den Insekten befinden, eine mühelose Eintrittspforte. Um sich vor ihren „Mitbewohnern“ zu schützen, entwickelten die Insekten in ihrer Immunabwehr Strategien, auf verschiedene solcher Pathogene zu reagieren. Neue, leistungsstarke Methoden der reversen Genetik [2, 3] und die komplette Sequenzierung des Genoms der Mücke A. gambiae haben wesentlich dazu beigetragen, die molekularen Wechselwirkungen zwischen der Anopheles-Mücke und Plasmodium zu verstehen.
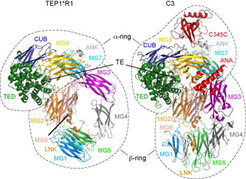
Das Immunsystem der Mücken spielt eine entscheidende Rolle bei der Beherrschung der Plasmodium-Infektion, denn es vernichtet die meisten eindringenden Parasiten bereits kurz nach dem Blutsaugen [4]. Wir fanden, dass die Mücken Malariaparasiten auf ähnliche Weise zerstören, wie Säuger gegen Infektionen reagieren. Die wesentliche Komponente dieses Systems in der Mücke, das Hämozyten spezifische, thioesterhaltige Protein TEP1, erkennt Mikroorganismen und zielt auf deren Vernichtung ab. Die Struktur von TEP1 ähnelt seinem Homolog C3 beim Säugetier (Abb. 2). Mit Hilfe eines Plasmodiumstammes, der grün fluoreszierendes Protein produziert und so im Fluoreszenzmikroskop sichtbar gemacht werden konnte (vgl. Abb. 3), entdeckten wir, dass TEP1 an die Oberfläche der Ookineten - also die beweglichen Zygoten (Zygote = befruchtete Eizelle) von Plasmodium - bindet, und zwar auf der Basalseite des Mitteldarms der Mücken. Die TEP1-Ookinet Bindung führt zum Tod der Zygoten und damit zur Unterbrechung des Infektionszyklus in der Mücke [5-8].
Von Laboruntersuchungen zu Feldbedingungen
"Insects are individuals, and even within a single species insects often do things in subtly different ways from each other; this is, after all, a prerequisite for evolution."
M. J. Lehane “The Biology of Blood-Sucking in Insects”
Mücken der Gattung Anopheles sind, dieses Zitat betrachtend, keine Ausnahme und können hinsichtlich ihrer Fähigkeit, die Entwicklung des Malaria-Parasiten zu fördern oder zu hemmen, beträchtlich voneinander abweichen. So wird in manchen Mückenpopulationen in einigen, jedoch sehr seltenen Fällen die Entwicklung von Plasmodium schon kurz nach der Infektion komplett unterdrückt (Abb. 3). Laborversuche zeigten, dass manche Allele von TEP1 eine solche fast vollständige Unterdrückung des Parasiten hervorrufen können, wohingegen andere TEP1-Allele weniger effizient waren und nur 80% der Ookineten auslöschten [9].
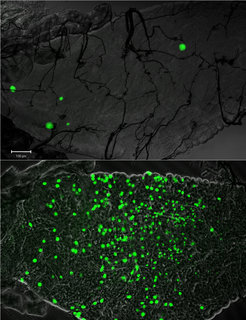
Nun wäre es interessant zu überprüfen, ob solche wie von uns charakterisierten, gegen Plasmodium resistenzverleihenden Allele von TEP1 auch in afrikanischen Mücken natürlicherweise in deren Genomen auftreten. Bei einem Screening Tausender von Mücken in Mali, Kamerun und Kenia stellte sich dann tatsächlich heraus, dass in den dort vorkommenden Mückenpopulationen TEP1 Allele vorhanden sind, die Plasmodium in ihren Därmen fast vollständig besiegen. Allerdings: Neue Daten deuten darauf hin, dass die Parasiten Mutationen entwickeln, die sie wiederum gegen TEP1-Angriffe widerstandsfähig machen. Zukünftige Untersuchungen sollten daher die genetische Vielfalt der beiden Organismen Mücke und Parasit berücksichtigen, um das „molekulare Wettrüsten“ besser zu verstehen.
Wir konzentrierten unsere Studien auf ein Dorf in Mali, wo alle allelen Formen von TEP1 gefunden wurden. Erstaunlicherweise ist die allele Verteilung in dieser Population nicht zufällig, was auf einen dort herrschenden Selektionsdruck schließen lässt. Welche Stadien der Mückenentwicklung sind für diesen Selektionsdruck empfindlich? Welche Kräfte treiben diese Auslese an? Es sind zwar noch viele interessante Fragen offen, doch erste Befunde legen nahe, dass neben der genetischen Vielfalt von Mücke und Plasmodium viele andere Umweltfaktoren die genetische Struktur der Mückenpopulationen prägen und dabei das Vermögen der Mücke, Malaria zu übertragen, beeinflussen.
Genetik versus Umwelt
Die unreifen Stadien von A. gambiae leben in der mikrobenreichen Umgebung bestimmter Wasservorkommen mit der Folge, dass Mikroorganismen den Mitteldarm von Larven besiedeln. Es ist wahrscheinlich, dass schon die Umgebung der Larvenbrutstätten zur Entwicklung verschiedener Immunabwehrmechanismen führt. Erste Berichte dokumentieren bereits die Zusammensetzung und Auswirkung der mikrobiellen Umgebung auf die Widerstandsfähigkeit von Mücken gegenüber Malaria; eine gründliche Analyse steht noch aus. Über ein komplettes Jahr wollen wir den Einfluss der Larvenbrutstätten auf die genetische Struktur von Mückenpopulationen in einem einzelnen Dorf in Mali untersuchen. Dabei sollen eine genaue Beschreibung der mikrobiellen Zusammensetzung in den Brutstätten erstellt und diejenigen Mikroorganismen-Gemeinschaften ermittelt werden, die einen derartigen Selektionsdruck auf die Mückenpopulationen ausüben könnten, dass daraus auch eine Änderung des Übertragungsmusters der Malaria folgen könnte. Das Verstehen regionaler Umstände und Bedingungen, die Malaria-Epidemien prägen, könnte neue Möglichkeiten zur Bekämpfung von Krankheitsüberträgern eröffnen. Vor allem aber werden diese Befunde auch neue Denkansätze bezüglich der Wirt-Parasit Wechselwirkung anstoßen, die auch umweltbedingte Faktoren in die vielfältigen Übertragungswege einbezieht.
Immunität und Fortpflanzung
Mit der Aufnahme von Blut erwerben A. gambiae Mückenweibchen die für ihre Eientwicklung und damit für ihre Fortpflanzung notwendigen Nährstoffe. Enthält das Blut jedoch Plasmodium, infizieren die Mücken sich gleichzeitig mit den Malariaerregern. Uns interessiert, ob eine Modulation von Immunfaktoren wie TEP1 den Reproduktionserfolg der Mücken beeinflusst. Tatsächlich fanden wir, dass zwei lipidtransportierende Proteine, die zur Nährstoffversorgung der Eier nach der Blutaufnahme von der Mücke im Darm gebildet werden (Lipophorin und Vitellogenin), die TEP1-gesteuerte Vernichtung der Parasiten einschränken [10]. Bei Abwesenheit der beiden Lipidtransportproteine wiederum ist die Bindung von TEP1 an die Ookineten von Plasmodium effizient und vollständig - der Erreger wird erfolgreich attackiert. Folglich mogeln sich die Erreger nicht nur durch das Blutsaugen in eine Mücke hinein, sondern nutzen gleichzeitig diese Gelegenheit auch, um unentdeckt vom Immunsystem der Mücke sich in deren Darm versteckt zu halten. Dagegen nun entwickelt die Mücke eine Strategie, bei der sie durch Aktivierung des Immunsystems die Synthese ihrer fortpflanzungsrelevanten, Nährstoff transportierenden Proteine stilllegen kann [10].
Zurzeit erforschen wir detailliert die molekularen Mechanismen dieses crosstalks und überlegen gleichzeitig, wie diese neuen Erkenntnisse zur Eindämmung gefährlicher, Plasmodium übertragender Mückenpopulationen genutzt werden könnten.