Forschungsbericht 2004 - Max-Planck-Institut für medizinische Forschung
Neue Einblicke ins Gehirn – Beobachtung von Gliazellen in der intakten Hirnrinde
Zellphysiologie
MPI für medizinische Forschung, Heidelberg
Gliazellen in der Hirnrinde
Das Gehirn umfasst eine Vielzahl von Zellpopulationen, die in der Hirnrinde in enger Nachbarschaft existieren. Grundsätzlich wird zwischen den Nervenzellen (Neuronen) und den Gliazellen unterschieden. Neurone sind mit ihrer elektrischen Erregbarkeit für die schnelle Signalverarbeitung und Signalweiterleitung zuständig. Gliazellen hingegen wurden in der Vergangenheit oft als reine Stützzellen angesehen, als Nerven-Kitt (griechisch glia: Leim, Kitt), der die Neurone im Wesentlichen mit Nährstoffen versorgt. Neuere Untersuchungen deuten jedoch darauf hin, dass Gliazellen eine weit größere Bedeutung für die Funktion des Gehirns haben als bislang angenommen und dass enge wechselseitige Beziehungen mit den Neuronen bestehen. Zunehmend werden Gliazellen nicht mehr als bloße Statisten, sondern als wichtige Akteure des neuronalen Geschehens verstanden.
Es gibt verschiedene Typen von Gliazellen. Oligodendrozyten beispielsweise bilden die so genannten Myelinscheiden um Nervenfasern. Sie isolieren die Nervenfaser elektrisch – ähnlich wie die Kunststoffhülle eines Kabels – und ermöglichen dadurch erst eine schnelle neuronale Signalübertragung. Die Astrozyten regulieren unter anderem die molekulare Zusammensetzung des Extrazellulärraumes und beeinflussen damit den Gleichgewichtszustand im Gehirn. Mit ihren Zellfortsätzen umschließen sie das Blutgefäß-System und vermitteln den Austausch der wesentlichen am zellulären Stoffwechsel beteiligten Stoffe. Mikrogliazellen schließlich sind die immunkompetenten Zellen des Gehirns. Sie sind die ersten Zellen, die auf pathologische Ereignisse reagieren und die Immunantwort des Gehirns einleiten.
Neue Methoden zur Beobachtung von Gliazellen
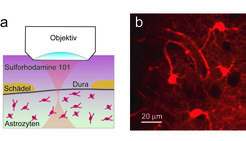
Bis vor kurzem konnten Gliazellen fast aussschließlich in vitro, das heißt außerhalb des lebenden Organismus untersucht werden. Derartige Untersuchungsverfahren stellen jedoch einen Eingriff in das natürliche Gefüge des Gehirns dar und führen zu Veränderungen des sensiblen extrazellulären Gleichgewichts. Neue Verfahren erlauben es nun, einen direkten Blick ins Gehirn zu werfen und Zellen in vivo, das heißt im intakten Gehirn zu beobachten. Eine Schlüsseltechnologie ist dabei die Zwei-Photonen-Fluoreszenz-Mikroskopie [1], die es ermöglicht, hochauflösende Fluoreszenzbilder aus relativ großer Tiefe (bis zu einem Millimeter) im stark lichtstreuenden Nervengewebe aufzunehmen [2, 3, 4]. Voraussetzung für die Anwendung der Zwei-Photonen-Fluoreszenz-Mikroskopie ist jedoch die nach Möglichkeit selektive Anfärbung der zu untersuchenden biologischen Strukturen. Im Hinblick auf die spezifische Anfärbung der verschiedenen Arten von Gliazellen konnten in den letzten Jahren entscheidende Fortschritte erzielt werden. Eine überraschende Entdeckung war, dass ein bestimmter roter Fluoreszenzfarbstoff (Sulforhodamine 101) selektiv von Astrozyten aufgenommen wird, wenn er in verdünnter Lösung auf die Oberfläche der Hirnrinde geträufelt wird [5] (Abb. 1). Obwohl der Transportmechanismus, der zur selektiven Aufnahme führt, noch nicht verstanden ist, konnte gezeigt werden, dass sich der Farbstoff über Poren in der Zellmembran (gap junctions) zwischen den Astrozyten verteilt. Dieses einfache Verfahren erlaubt daher die Fluoreszenzmarkierung der Astrozyten in einem begrenzten Hirnrinden-Bereich und lässt sich insbesondere mit neuen Verfahren zur In-vivo-Anfärbung von Zellpopulationen mit Kalzium-empfindlichen Farbstoffen kombinieren. Dadurch ist es erstmals möglich geworden, bei gleichzeitiger Messung neuronaler Aktivität, im Astrozyten-Netzwerk langsame Oszillationen (im Bereich von Sekunden bis Minuten) der intrazellulären Konzentration von Kalzium, einem wichtigen intrazellulären Botenstoff, aufzulösen.
Eine zweite wichtige Methode, Gliazellen im intakten Gehirn sichtbar zu machen, ist die Herstellung transgener Mäuse, in denen ein fluoreszierendes Protein in einem bestimmten Zelltyp produziert wird. Neben Mäusen mit Neuronen-spezifischer Expression gibt es inzwischen verschiedene transgene Mauslinien, die das grün-fluoreszierende Protein (GFP) entweder in Astrozyten oder in Mikrogliazellen exprimieren [6]. Diese transgenen Mäuse können mithilfe der Zwei-Photonen-Mikroskopie untersucht werden. Von großem Vorteil ist dabei, dass die Zellen bereits von Geburt des Tieres an gefärbt sind, sodass in vielen Experimenten Fluoreszenzbilder nicht-invasiv durch die gedünnte, aber ungeöffnete Schädeldecke aufgenommen werden können (Abb. 2).
![Beobachtung von Mikrogliazellen durch die ungeöffnete Schädeldecke. (a) Schematische Darstellung der Messmethode. Es werden transgene Mäuse benutzt, die in der Hirnrinde spezifische Expression von GFP (grün- fluoreszierendes Protein) in Mikrogliazellen zeigen [6]. Die Zellen können mit Hilfe der Zwei-Photonen-Mikroskopie durch die gedünnte, aber ungeöffnete Schädeldecke in hoher Auflösung sichtbar gemacht werden. (b) Fluoreszenzaufnahme von drei Mikrogliazellen durch die Schädeldecke mit Hilfe der Zwei-Photonen-Mikroskopie.](/829960/original-1294357499.jpg?t=eyJ3aWR0aCI6MjQ2LCJvYmpfaWQiOjgyOTk2MH0%3D--43a4fbfd927a8d446129ac5893742461d31a63a3)
Mikroglia: Aufmerksame Wächter in der Hirnrinde
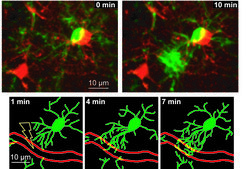
Die Beobachtung von Mikrogliazellen in einer transgenen Mauslinie mit spezifischer GFP-Färbung hat besonders aufschlussreiche Ergebnisse über das Verhalten dieser Gliazellen geliefert. Durch die wiederholte Aufnahme von Fluoreszenzbild-Stapeln ein und desselben Volumens der Hirnrinde konnten die Forscher die Form der Mikrogliazellen über mehrere Stunden beobachten. In diesen Filmen wird offensichtlich, dass Mikrogliazellen in ihrem so genannten ,Ruhezustand' keineswegs in Ruhe sind, sondern beständig das umgebende Gewebe mit ihren feinen Zellfortsätzen abtasten [7]. Dabei zeigen sie ein erstaunlich hohes Maß an Veränderung ihrer Form: Innerhalb von wenigen Minuten bilden sich immer wieder neue Tentakel-ähnliche Fortsätze, die zum Teil vermutlich abgestorbenes Zellmaterial umschließen und dann wieder abgebaut werden. Diese Vorgänge laufen kontinuierlich und ohne Vorzugsrichtung ab und unterstützen wahrscheinlich die Aufrechterhaltung des extrazellulären Gleichgewichts.
Mikrogliazellen, als die immunkompetenten Zellen des Gehirns, sind an jeglicher Immunreaktion in der Hirnrinde beteiligt, etwa bei Hirnschädigungen oder bei neurodegenerativen Erkrankungen. Mithilfe der Zwei-Photonen-Mikroskopie konnten die Wissenschaftler untersuchen, wie Mikrogliazellen auf eine lokale Hirnblutung reagieren, wie sie zum Beispiel bei einem durch Bluthochdruck bedingten Schlaganfall auftreten kann. Es zeigte sich, dass Mikrogliazellen bei der Verletzung eines Blutgefäßes sehr schnell (innerhalb von Minuten) aktiv werden (Abb. 3). Die Aktivierung wird deutlich durch einen Wechsel vom ungerichteten Ruheverhalten zu einem gezielten Auswachsen der Zellfortsätze benachbarter Mikrogliazellen in Richtung der verletzten Stelle. Daraufhin wird der beschädigte Gefäßabschnitt abgedichtet [7]. Ebenfalls konnten die Heidelberger Wissenschaftler in den ersten Stunden nach der Verletzung beobachten, wie aus den Zellen oder dem Gefäß ausgetretenes Material von den Mikrogliafortsätzen umschlossen und anscheinend verdaut (phagozytiert) wird. Ähnliche Vorgänge wie bei diesen Mikroverletzungen laufen vermutlich in den ersten Minuten und Stunden nach einem Schlaganfall ab.
Zusammenfassend hat es sich gezeigt, dass die Kombination der Zwei-Photonen-Mikroskopie mit neuen zellspezifischen Färbemethoden ungeahnte Möglichkeiten eröffnet, nicht nur die Aktivität der Nervenzellen, sondern auch die Form und Funktion der Gliazellen sowie ihre wechselseitigen Beziehungen zu anderen Zellen in der intakten Hirnrinde zu untersuchen. Bisher sind diese Verfahren zwar im Wesentlichen auf die Hirnrinde von narkotisierten Versuchstieren angewendet worden. Fortschritte in der Miniaturisierung der Zwei-Photonen-Mikroskopie mithilfe optischer Fasern [8, 9, 10] lassen Untersuchungen an tiefergelegenen Hirnstrukturen und an freilaufenden, sich verhaltenden Tieren in naher Zukunft möglich erscheinen.

![Beobachtung von Mikrogliazellen durch die ungeöffnete Schädeldecke. (a) Schematische Darstellung der Messmethode. Es werden transgene Mäuse benutzt, die in der Hirnrinde spezifische Expression von GFP (grün- fluoreszierendes Protein) in Mikrogliazellen zeigen [6]. Die Zellen können mit Hilfe der Zwei-Photonen-Mikroskopie durch die gedünnte, aber ungeöffnete Schädeldecke in hoher Auflösung sichtbar gemacht werden. (b) Fluoreszenzaufnahme von drei Mikrogliazellen durch die Schädeldecke mit Hilfe der Zwei-Photonen-Mikroskopie. Beobachtung von Mikrogliazellen durch die ungeöffnete Schädeldecke. (a) Schematische Darstellung der Messmethode. Es werden transgene Mäuse benutzt, die in der Hirnrinde spezifische Expression von GFP (grün- fluoreszierendes Protein) in Mikrogliazellen zeigen [6]. Die Zellen können mit Hilfe der Zwei-Photonen-Mikroskopie durch die gedünnte, aber ungeöffnete Schädeldecke in hoher Auflösung sichtbar gemacht werden. (b) Fluoreszenzaufnahme von drei Mikrogliazellen durch die Schädeldecke mit Hilfe der Zwei-Photonen-Mikroskopie.](/829960/original-1294357499.jpg?t=eyJ3aWR0aCI6MzQxLCJmaWxlX2V4dGVuc2lvbiI6ImpwZyIsIm9ial9pZCI6ODI5OTYwfQ%3D%3D--249dea4bcb3b1f194cf7a13d837dcbee467a6c7c)
