Forschungsbericht 2013 - Max-Planck-Institut für Dynamik und Selbstorganisation
Ein innerer Taktgeber des Actin-Zytoskeletts
The intrinsic pace of the actin cytoskeleton
Beta, Carsten
Bewegungsprozesse gehören zu den herausragenden Merkmalen der belebten Natur. Dies gilt nicht nur für hochentwickelte, vielzellige Organismen, sondern auch auf zellulärer Ebene. Die Beweglichkeit einzelner Zellen ist die Voraussetzung für zahlreiche essentielle biologische Funktionen. Die Embryonalentwicklung, der Heilungsprozess an einer Wunde oder auch die Funktion unseres Immunsystems sind Beispiele für Prozesse, die entscheidend von der Fähigkeit einzelner Zellen abhängen, sich unter dem Einfluss chemischer Signale zielgerichtet zu bewegen [1,2].
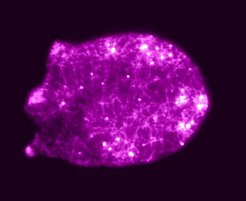
Auch bei zahlreichen pathologischen Prozessen, wie beispielsweise der Ausbreitung von metastasierenden Krebszellen im Körper, spielt die Zellbewegung eine zentrale Rolle. In den Zellen höherer Organismen, den sogenannten eukaryotischen Zellen, beruht der Bewegungsprozess in den meisten Fällen auf der Dynamik des Actin-Zytoskeletts. Es handelt sich dabei um eine Netzwerkstruktur, die sich an die Innenseite der Zellmembran anschließt und der Zelle ihre Form und mechanische Stabilität verleiht. Dieser Bereich wird auch als Actin-Kortex der Zelle bezeichnet. Grundelement des kortikalen Netzwerkes sind Biopolymerfasern aus dem Protein Actin, die einem kontinuierlichen Wachstums- und Abbauprozess (Polymerisation und Depolymerisation) unterliegen. Zusammen mit einer Vielzahl weiterer Komponenten, die die Polymerisationsprozesse regulieren und die Actin-Filamente verbinden und bündeln, entsteht ein komplexes, dynamisches Netzwerk, das beständig umgebaut und remodelliert wird. Werden die Wachstumsprozesse im Actin-Netzwerk lokal gegen die Zellmembran gelenkt, so entstehen Kräfte, die zu einer Deformation der Membran und damit zu einer gerichteten Ausstülpung − der Bildung eines sogenannten Pseudopodiums − führen können. Geht diese Ausstülpung mit einer gleichzeitigen Kontraktion des Actin-Kortex auf der gegenüberliegenden Seite einher, so kommt es zu einer Verschiebung des Zellkörpers in Richtung der Ausstülpung und damit zu einer gerichteten Bewegung. Abbildung 1 zeigt die fluoreszenzmikroskopische Aufnahme des Actin-Netzwerkes im Inneren einer Zelle während eines solchen Prozesses. Linker Hand sind deutlich die beschriebenen Ausstülpungen zu erkennen, die die Bewegung der Zelle nach links treiben.
Ein entscheidendes Element dieser Bewegungsprozesse ist ihre Koordination mit den äußeren Umgebungsbedingungen. Bewegliche Zellen sind in der Regel mit Membranrezeptoren ausgestattet, spezialisierten molekularen Bausteinen, die der Zelle erlauben, die Umgebungskonzentration bestimmter chemischer Spezies zu detektieren. Sind bestimmte Lockstoffe vorhanden, so kann dies den Bewegungsprozess beeinflussen. Insbesondere chemische Gradienten, also Lockstoff-Konzentrationen, die in einer bestimmten Richtung zunehmen, sind geeignet die Bewegung von Zellen räumlich auszurichten. Man spricht in diesem Fall von Chemotaxis, der gerichteten Bewegung unter dem Einfluss eines chemischen Gradienten [3]. Aufgrund der herausragenden biologischen und medizinischen Relevanz chemisch gesteuerter Zellbewegung ist die Untersuchung dieser Prozesse ein hochaktuelles und dynamisches Feld gegenwärtiger interdisziplinärer Forschung, in dem Wissenschaftler der angrenzenden Disziplinen, insbesondere aus der Zellbiologie und der Biophysik, gemeinsam aktiv sind.
![Abb. 2: Konzentrationsverlauf von filamentösem Aktin in Antwort auf einen kurzen chemischen Stimulus (rot), getrennt nach zytosolischem (schwarz) und kortikalem Actin (blau). Siehe auch [4].](/11603182/original-1508157087.jpg?t=eyJ3aWR0aCI6MjQ2LCJvYmpfaWQiOjExNjAzMTgyfQ%3D%3D--2c0b140df1c5948cc2332bf2a33cb90fe7276233)
In einer kürzlich in den Proceedings der National Academy of Sciences of the USA veröffentlichten Arbeit haben Wissenschaftler vom Max-Planck-Institut für Dynamik und Selbstorganisation und von der Universität Potsdam die Reaktionen des Actin-Zytoskeletts auf äußere chemische Reize genauer untersucht [4]. Die Experimente wurden an Zellen der sozialen Amöbe Dictyostelium discoideum durchgeführt, einem beliebten und weit verbreiteten Modellorganismus zur Untersuchung von Actin-getriebener Zellbewegung. Mithilfe einer kürzlich in der Abteilung „Hydrodynamik, Strukturbildung und Biokomplexität” entwickelten Methode ist es möglich, einzelne Zellen mit exakt definierten chemischen Signalen zu stimulieren und die Reaktionen im Actin-Zytoskelett gleichzeitig mithilfe eines Fluoreszenzmikroskops zu verfolgen [5−7]. Durch eine genaue Analyse der Actin-Reaktion auf kurze chemische Konzentrationspulse konnte gezeigt werden, dass dem Actin-System eine eigene Schwingungsfrequenz innewohnt. Ähnlich einem mechanischen Pendel, das man anstößt, reagieren die Zellen auf einen kurzen Konzentrationspuls mit einer gedämpften Schwingung. In Abbildung 2 sind Daten gezeigt, die den Konzentrationsverlauf von filamentösem Actin infolge eines kurzen Stimulus wiedergeben. Diese Beobachtung wurde zum Anlass genommen, die Zellen mit periodischen Sequenzen von Konzentrationspulsen anzuregen. Die Anregungsfrequenz wurde dabei systematisch über einen weiten Bereich variiert. Beispiele für das Antwortverhalten der Zellen bei unterschiedlichen Frequenzen sind in Abbildung 3A−C zu sehen. In Abbildung 3D ist zusammenfassend die Amplitude der Actin-Schwingungen als Funktion der Anregungsfrequenz aufgetragen. Der Verlauf zeigt ein klar ausgeprägtes Maximum bei einer Frequenz von 0,05 Hz, was einer Anregungsperiode von 20 sec entspricht. Hier ist die dem Actin-System eigene Frequenz in Resonanz mit der äußeren Anregung.
![Fig. 3: A−C: Antwort des Actin-Systems auf periodische Stimuli (rot) mit unterschiedlicher Frequenz. D: Amplitude der Actin-Antwort als Funktion der Anregungsfrequenz mit einer klaren Resonanz bei 0,05 Hz (20 sec). Siehe auch [4].](/11603190/original-1508157088.jpg?t=eyJ3aWR0aCI6MjQ2LCJvYmpfaWQiOjExNjAzMTkwfQ%3D%3D--990217e806a4db7d26ffae82e32a36aa6fea59ea)
Diese Ergebnisse können als klarer Beleg dafür gewertet werden, dass das Actin-System beweglicher Zellen durch einen inneren Taktgeber mit einer intrinsischen Periode von ca. 20 sec kontrolliert wird. Diese Zeitskala zeigt eine gute Übereinstimmung mit Messungen der Frequenz der Pseudopodienbildung. Die Zeit, die bei einer beweglichen Dictyostelium Zelle zwischen der Bildung zweier Membranausstülpungen vergeht, liegt ebenfalls im Bereich von 20 sec [8]. Ein Zusammenhang zwischen dem inneren Taktgeber und der Dynamik der Pseudopodien ist daher ein naheliegender Schluss. Weiterführende Arbeiten richten sich nun auf die Frage, welche molekularen Komponenten des Actin-Zytoskeletts und der beteiligten Signalwege für die Frequenz des inneren Taktgebers verantwortlich sind. Um diese Frage systematisch zu erforschen, haben die beteiligten Wissenschaftler ein mathematisches Modell vorgeschlagen, das die vorliegenden Messergebnisse korrekt wiedergibt. Die intrinsische Frequenz des Actin-Systems wird im Rahmen dieses Modells durch eine zeitverzögerte Rückkopplung erklärt. Die Zelle überwacht den Actin-Gehalt in ihrem eigenen Kortex mithilfe bestimmter Regulatoren. Da diese aufgrund der beteiligten biochemischen Reaktionen erst mit einer gewissen Verzögerung auf eine Änderung in der Actin-Konzentration ansprechen, kommt es zu einem zeitlichen Versatz, der eine mathematische Erklärung für das beobachtete oszillatorische Verhalten liefert. In laufenden Arbeiten werden nun Zelllinien untersucht, in denen durch genetische Defekte bestimmte Zytoskelett-Regulatoren und Signalmoleküle ausgeschaltet wurden (sogenannte knockout Mutanten). Das geänderte Antwortverhalten dieser Zellen gibt Aufschluss über die Rolle der jeweils ausgeschalteten Komponenten und kann, durch Abgleich mit dem vorliegenden mathematischen Modell, unser Bild vom inneren Taktgeber des Actin-Zytoskeletts vervollständigen.

![Abb. 2: Konzentrationsverlauf von filamentösem Aktin in Antwort auf einen kurzen chemischen Stimulus (rot), getrennt nach zytosolischem (schwarz) und kortikalem Actin (blau). Siehe auch [4]. Abb. 2: Konzentrationsverlauf von filamentösem Aktin in Antwort auf einen kurzen chemischen Stimulus (rot), getrennt nach zytosolischem (schwarz) und kortikalem Actin (blau). Siehe auch [4].](/11603182/original-1508157087.jpg?t=eyJ3aWR0aCI6MzQxLCJmaWxlX2V4dGVuc2lvbiI6ImpwZyIsIm9ial9pZCI6MTE2MDMxODJ9--600dbcab073149329799b474fbe25eb15a4f201e)
![Fig. 3: A−C: Antwort des Actin-Systems auf periodische Stimuli (rot) mit unterschiedlicher Frequenz. D: Amplitude der Actin-Antwort als Funktion der Anregungsfrequenz mit einer klaren Resonanz bei 0,05 Hz (20 sec). Siehe auch [4]. Fig. 3: A−C: Antwort des Actin-Systems auf periodische Stimuli (rot) mit unterschiedlicher Frequenz. D: Amplitude der Actin-Antwort als Funktion der Anregungsfrequenz mit einer klaren Resonanz bei 0,05 Hz (20 sec). Siehe auch [4].](/11603190/original-1508157088.jpg?t=eyJ3aWR0aCI6MzQxLCJmaWxlX2V4dGVuc2lvbiI6ImpwZyIsIm9ial9pZCI6MTE2MDMxOTB9--0561ddaadffce40ddb60109141dd078e833a02b9)