Forschungsbericht 2005 - Max-Planck-Institut für Kernphysik
Atmosphärische Schwefelsäure: Einflüsse auf Umwelt und Klima
Atmosphärische Spurengase und Ionen (Prof. Dr. Frank Arnold)
MPI für Kernphysik, Heidelberg
Schwefelsäure und Umwelt
Die atmosphärische Schwefelsäure und die aus ihr entstehenden Schwefelsäure- und Sulfat-Aerosolteilchen (SAT) beeinflussen nicht nur das Klima, sondern tragen auch wesentlich zum so genannten sauren Regen bzw. sauren Niederschlag bei und beeinträchtigen durch direkten Kontakt die Biosphäre und insbesondere auch die menschliche Gesundheit. SAT erhöhen die planetare Albedo und wirken somit dem Treibhauseffekt entgegen [2]. Allerdings ist diese durch SAT bewirkte Albedoerhöhung noch nicht ausreichend gut quantifiziert und stellt daher eine der größten Unsicherheiten in heutigen Klimamodellen dar. Bemerkenswerterweise stammen sowohl das anthropogene CO2 als auch der anthropogene Schwefel vorwiegend aus der Verbrennung fossiler Brennstoffe.
Offenbar verdankt die Menschheit nur einem Zufall, dass sich bisher die vom anthropogenen CO2 und anthropogenen Schwefel ausgehenden gegenläufigen Klimastörungen zumindest teilweise aufheben. In Zukunft wird diese Schwefelbremse des anthropogenen Treibhauseffekts jedoch schwächer werden. Während CO2 weiter zunehmen wird, begann der atmosphärische Schwefel aufgrund des zunehmenden Einsatzes moderner Rauchgasentschwefelungstechnik auch in Schwellenländern wie insbesondere China und Indien bereits seit etwa 1990 wieder abzunehmen.
Gelangt Schwefel in die obere Troposphäre oder gar in die Stratosphäre, so kann er dort länger verweilen. Quellen stratosphärischen Schwefels sind große Vulkaneruptionen, Flugzeuge und Transport aus der Troposphäre insbesondere durch hochreichende Konvektion (Abb. 1).

Die enorme Klimawirkung, welche von stratosphärischen SAT ausgehen kann, wird uns durch heftige Vulkaneruptionen sehr drastisch vor Augen geführt. Derartige, allerdings relativ seltene Eruptionen injizieren große Mengen von SO2 in die Stratosphäre, wo SO2 auf photochemischem Weg in gasförmige H2SO4 und schließlich in SAT umgewandelt wird. Diese SAT sind sehr klein, sedimentieren daher nur sehr langsam und verweilen etwa 1-2 Jahre in der Stratosphäre, wo sie einfallendes Sonnenlicht in den Weltraum zurückstreuen. Dies führt zu einer Absenkung der global gemittelten Oberflächentemperatur des Planeten um etwa 0,4 K. Tatsächlich wurde eine derartige Abkühlung nach der jüngsten großen Vulkaneruption (Pinatubo 1991) beobachtet [2].
Bildung von Schwefelsäure und Schwefelsäureaerosol
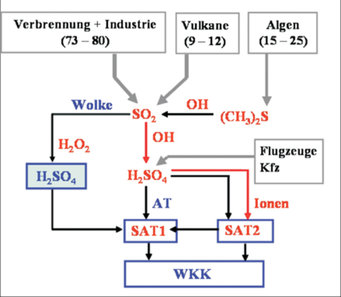
Abbildung 2 zeigt ein stark vereinfachtes Schema der Bildung atmosphärischer Schwefelsäure und SAT. Es soll die wesentlichen Prozesse illustrieren und auf Forschungsbeiträge des Instituts (rot) hinweisen. Das atmosphärische Spurengas SO2 spielt als Vorläufer der H2SO4 eine zentrale Rolle. Es wird sowohl in die Atmosphäre eingetragen (vorwiegend durch Verbrennung fossiler Brennstoffe und in geringerem Umfang auch durch Industrie und Vulkanismus), als auch in der Atmosphäre auf photochemischem Weg vorwiegend aus dem von Algen produzierten (CH3)2S gebildet. In der Atmosphäre wird SO2 unter der Einwirkung von Photooxidantien in Schwefelsäure umgewandelt. Die Umwandlung erfolgt sowohl in der Gasphase als auch in der Flüssigphase (Wolkentröpfchen). Bei der H2SO4-Bildung wirken als Oxidationsmittel vorwiegend die photochemisch gebildeten atmosphärischen Spurengase OH und H2O2. Während das nur am Tag existierende OH gasförmige Schwefelsäure bildet, ist das auch nachts existierende H2O2 nach Aufnahme in Tröpfchen für die SO2-Umwandlung in der Flüssigphase (hellblau unterlegte Box) hauptsächlich verantwortlich.

Die in einem Wolkentröpfchen gebildete Schwefelsäure bleibt nach Verdampfen des Tröpfchenwassers (90% der Tröpfchen verdampfen wieder in der Atmosphäre) mit dem Aerosolteilchen assoziiert, das ursprünglich die Bildung des Tröpfchens als Wasserdampfkondensationskern auslöste. Hier entsteht also kein völlig neues Teilchen, sondern vielmehr wird ein ursprünglich bereits vorhandenes Teilchen zum SAT1-Teilchen, das zusätzlich Schwefelsäure oder Sulfat enthält.
Gasförmige H2SO4 ist sehr hygroskopisch und bildet starke Wasserstoffbrückenbindungen mit H2O-Molekülen sowie mit anderen H2SO4-Molekülen. Unter typischen troposphärischen Bedingungen entstehen daher H2SO4/H2O-Kondensate, deren H2SO4-Massenfraktion meist bei 50-70% liegt. Diese Kondensation erfolgt bevorzugt an präexistenten Aerosolteilchen (AT) und begrenzt die Lebensdauer eines gasförmigen H2SO4-Moleküls auf weniger als 1000 s, was dessen Transport in der Atmosphäre sehr stark limitiert. Reagiert H2SO4 nicht mit dem AT, so entsteht ein mit H2SO4/H2O beschichtetes Teilchen (SAT1).
Alternativ können sich durch Zusammenlagerung gasförmiger H2O- und H2SO4-Moleküle (Nukleation) molekulare Cluster bilden, die schließlich zu stabilen SAT2 anwachsen können. Atmosphärische gasförmige Ionen können die Nukleation durch Stabilisierung der Cluster erleichtern. In der Troposphäre und Stratosphäre entstehen Ionen vorwiegend durch die kosmische Strahlung. Die ioneninduzierte Nukleation ist ein wesentlicher Bestandteil einer gegenwärtig heftig und durchaus kontrovers diskutierten „Cosmic Ray-Climate Connection“-Hypothese [1]. Durch Nukleation gebildete frische SAT2 wachsen anschließend durch Aufkondensation übersättigter Spurengase und durch SAT2-SAT2 Zusammenlagerung (Selbst-Koagulation). Hierdurch können SAT2 durchaus bis zur Größe von Wolkenkondensationskernen (Durchmesser > 50 nm) anwachsen. SAT2 können aber auch durch Anlagerung an die größeren AT und an SAT1 verloren gehen. Je schneller SAT2 wachsen, umso größer wird ihre Lebensdauer und umso leichter können sie Wolkenkondensationskerne werden.
In der Atmosphäre existiert nicht nur die oben diskutierte sekundäre, sondern auch primäre H2SO4. Letztere wird vorwiegend durch Verbrennungsprozesse in die Atmosphäre eingetragen. Primäre H2SO4 entsteht im noch sehr jungen Verbrennungsabgas (z.B. von Kraftfahrzeugen und Flugzeugen) und kommt daher in Abgasfahnen derartiger Verbrennungsquellen vor. Sie kann bereits im sehr jungen Verbrennungsabgas durch Nukleation zur Bildung zahlreicher SAT2 führen. Hierbei können aus der Verbrennung stammende Ionen die Nukleation erleichtern. Außerdem werden im Verbrennungsabgas aus AT (hier vorwiegend Rußteilchen) auch SAT1 gebildet. Die Beschichtung atmosphärischer Rußteilchen durch Kondensation von H2SO4 verändert ganz erheblich die Fähigkeit eines Rußteilchens, als Wasserdampfkondensationskern bzw. als Wassergefrierkern wirken zu können. Somit verändert H2SO4 den Einfluss von Rußteilchen auf die Wolken.
Messungen von Schwefelsäureaerosolvorläufern
Im Labor wurden Untersuchungen zur ioneninduzierten Nukleation (H2SO4/H2O) durchgeführt. Diese zeigen, dass negative Ionen effizienter nukleieren als positive Ionen. Negative Clusterionen enthalten anfänglich mehr H2SO4-Moleküle und wachsen schneller [3, 4].
In der Atmosphäre wurden zahlreiche neutrale (H2SO4, SO2, OH, HO2, H2O2) und ionische SAT-Vorläufer gemessen. In jüngster Zeit gelangen erste massenspektrometrische Messungen atmosphärischer, durch kosmische Strahlung gebildeter, großer positiver und negativer Clusterionen in der oberen Troposphäre und unteren Stratosphäre, wo diese Nukleation induzieren [1].
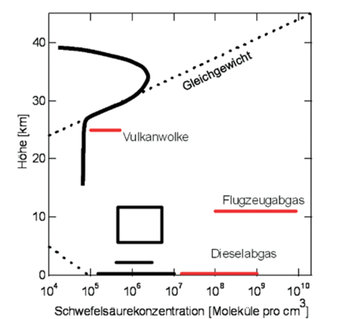
Abbildung 3 zeigt in schematischer Form die vertikale Verteilung der gemessenen atmosphärischen sekundären (schwarz) und primären (rot) H2SO4. Die durchgezogene schwarze Kurve ergibt sich aus der Mittelung von Messdaten, die bei stratosphärischen Ballonflügen bei Tag gewonnen wurden. Die schwarzen Balken und die Box geben die Variationsbreite der auf Messflugzeugen, auf Bergen und im Tiefland gewonnen atmosphärischen „Hintergrundwerte“ an. Primäre Schwefelsäure (rot) wurde in Abgasfahnen von Verkehrsflugzeugen im Flug und am Boden und in Abgasfahnen von Diesel-Fahrzeugen erstmals gemessen. Die gestrichelte schwarze Kurve stellt die Konzentration gasförmiger H2SO4 (für ein mittleres Atmosphärentemperaturprofil) dar, welche sich im Falle eines Gleichgewichts von H2SO4/H2O-Kondensation und Verdampfen von H2SO4/H2O-Aerosolteilchen einstellen würde. Liegt in einer gegebenen Höhe die gemessene atmosphärische H2SO4-Konzentration über dem Gleichgewichtswert, so ist sie übersättigt. Dies ist bei Tag ohne Wolken in allen Höhen unter 27 km der Fall. Somit sind H2SO4/H2O-Teilchen in diesem Höhenbereich thermodynamisch stabil. Die sehr großen, in der oberen Troposphäre auftretenden Übersättigungen (Sättigungsverhältnisse > 100) erlauben sogar die Bildung neuer Aerosolteilchen durch Nukleation.

Schwefelsäure-Messungen im Abgas von Flugzeugen im Flug und an Flugzeugtriebwerkstestständen zeigen, dass etwa 3% des im Flugzeugtreibstoff enthaltenen Schwefels in primäre gasförmige H2SO4 umgewandelt werden [5]. Die Messungen zeigen ebenfalls, dass die bei der Verbrennung gebildeten Clusterionen H2SO4-Moleküle enthalten, und dass diese Clusterionen die SAT2-Bildung durch Nukleation wesentlich fördern.
Messungen auf der Zugspitze (Abb. 4) sowie entsprechende Langzeitmessungen (jeweils mehrere Wochen) gasförmiger Schwefelsäure in Finnland (2003, 2005) und Heidelberg (2004) zeigen, dass gasförmige H2SO4 durch Nukleation neue SAT2 bildet, dass aber andere übersättigte, bisher noch nicht identifizierte Spurengase (wahrscheinlich organische Säuren) für das Größenwachstum der frischen SAT2 verantwortlich sind (H2SO4 trägt meist weniger als 10% zum Größenwachstum bei) [6, 7]. Weitere Messungen zeigen, dass nicht nur gasförmige H2SO4, sondern auch die photochemisch gebildete gasförmige Salpetersäure (HNO3) von speziellen AT aufgenommen werden kann. Sie reagiert chemisch mit Mineralstaub, einer wichtigen Form primärer AT [8].

Die Vermutung liegt nahe, dass die beobachtete große Variabilität der sekundären gasförmigen Schwefelsäure wesentlich durch die Variabilität des Vorläufers SO2 bedingt ist. In den Jahren 2004 und 2005 wurden mithilfe eines weiterentwickelten flugzeuggetragenen Massenspektrometers sehr umfangreiche SO2-Messungen über Europa, Südamerika, Asien und Australien durchgeführt. Diese in Zusammenarbeit mit dem DLR erfolgten Messungen zeigen tatsächlich eine sehr große SO2-Variabilität, welche einerseits durch die inhomogene Verteilung der SO2-Quellen und andererseits offenbar ganz wesentlich durch Transportvorgänge und SO2-Abbau (Wolkenprozesse und Photooxidation) verursacht wird. Die jüngsten Messungen über Europa lieferten sogar deutliche Anzeichen für einen konvektiven SO2-Transport in die unterste Stratosphäre. Außerdem zeigen sie, dass SO2-Ferntransport über tausende von Kilometern erfolgen kann. Diese Transportprozesse erlauben eine effiziente Bildung von SAT2 und Wolkenkondensationskernen in großen Höhen und weit entfernt von den SO2-Quellen [9, 10].
Schlussfolgerungen und Ausblick
Die jüngsten Arbeiten lieferten neue und wichtige Erkenntnisse über die Bildung und Verteilung atmosphärischer sekundärer und primärer Schwefelsäure sowie deren Vorläufer und aerosolbildender Wirkung. Geplante zukünftige Arbeiten werden sich auf Messungen atmosphärischer ionischer Vorläufer sekundärer Aerosolteilchen konzentrieren. Hierbei geht es nicht nur um SAT, sondern auch um organische Aerosolteilchen. Das Fernziel ist ein besseres Verständnis der Entstehung sekundärer Aerosolteilchen und deren Einfluss auf die Umwelt und das Klima.