Forschungsbericht 2008 - Max-Planck-Institut für Kohlenforschung
Nicht (nur) aus Sparzwang: Eisen statt Palladium!
Metallorganische Chemie (Prof. Dr. Alois Fürstner)
MPI für Kohlenforschung, Mülheim an der Ruhr
Einleitung: Kreuzkupplungen
Im Verlauf der letzten Jahrzehnte hat die homogene Katalyse insgesamt einen nicht zu übersehenden Siegeszug angetreten. Mit der Verleihung der Nobelpreise an Pioniere der homogenen asymmetrischen Hydrierung (Noyori, Knowles) und Oxidation (Sharpless) im Jahr 2001 bzw. der Olefinmetathese im Jahr 2005 (Chauvin, Grubbs, Schrock) wurde dies auch einer breiteren Öffentlichkeit deutlich. Diesen beiden Gebieten an Bedeutung ebenbürtig, oder – in Bezug auf die industrielle Praxis – vielleicht sogar überlegen, ist der Bereich der so genannten „Kreuzkupplungsreaktionen“ [1]. Bei diesem auf den ersten Blick unscheinbaren Reaktionstyp werden metallorganische Verbindungen mithilfe homogener Übergangsmetall-Katalysatoren mit Aryl- oder Alkenylhalogeniden (-sulfonaten) unter Bildung neuer Kohlenstoff-Kohlenstoff-Bindungen umgesetzt. Später wurden auch Kreuzkupplungen entwickelt, mit deren Hilfe Kohlenstoff-Heteroatom-Bindungen aufgebaut werden können [1].
Erschienen derartige Umsetzungen zum Zeitpunkt ihrer Entdeckung allenfalls als Kuriositäten, so ist heute unbestreitbar, dass Kreuzkupplungen selbst die industrielle Praxis in Forschung, Entwicklung und Produktion nachhaltig verändert haben. Sie sind aus der modernen medizinischen Chemie ebenso wenig wegzudenken, wie aus der Herstellung diverser Materialien, Feinchemikalien oder pharmazeutischer Wirkstoffe im Tonnen-Maßstab [1]. Dies ist umso erstaunlicher, als die etablierten Verfahren weitgehend auf der Nutzung von Palladiumkomplexen beruhen, wobei die nötigen Steuerliganden häufig sogar noch teurer sind als das als Zentralatom dienende Edelmetall. Diese ökonomischen Nachteile werden aber durch die Anwendungsbreite, Toleranz und Verlässlichkeit der Palladiumkatalyse (mehr als) aufgewogen.
Alternativen zum Palladium?
Vor dem Hintergrund dieser Erfolgsgeschichte mag es müßig erscheinen, nach Alternativen zum Palladium zu suchen. Da die Elementarschritte von Kreuzkupplungsreaktionen im Prinzip aber von vielen Metallen durchlaufen werden können, ist dies dennoch nicht aussichtslos. Idealerweise wäre der Ersatz für das Palladium billig, nicht toxisch, umweltverträglich, gut verfügbar und hoch reaktiv.
Dieses Anforderungsprofil könnte beim Eisen verwirklicht sein. Umso erstaunlicher ist es, dass gerade dieses Metall in der homogenen Katalyse bislang weit unterrepräsentiert ist, sieht man von der Tatsache ab, dass Eisenenzyme eine zentrale Rolle in biologischen Systemen spielen. Der auffällige Mangel an Eisen-Designerkatalysatoren in der präparativen Chemie mag mehrere Ursachen haben, unter denen das komplexe Redoxverhalten sowie die enormen Schwierigkeiten im Umgang und bei der Charakterisierung von Organoeisen-Verbindungen eine besondere Rolle spielen dürften. Während die Grundlagen der Palladiumchemie insgesamt recht übersichtlich und heute gut verstanden sind, stellt die metallorganische Chemie des Eisens einen vergleichsweise „weißen Fleck“ auf der Landkarte dar.

Allerdings fehlt es nicht an empirischem Wissen über den Einfluss von Eisensalzen auf den Verlauf metallorganischer Reaktionen. So wurde früh beobachtet, dass Spuren an Eisen im Magnesium-Metall, das zur Darstellung von Grignard-Regenzien ArMgX verwendet wird, einen erheblichen Einfluss auf den Verlauf der Reaktion ausüben [2]. Dennoch gelang es erst im Jahr 2002 einem Mülheimer Team um Bogdanović diesen Effekt gezielt zu nutzen [3].
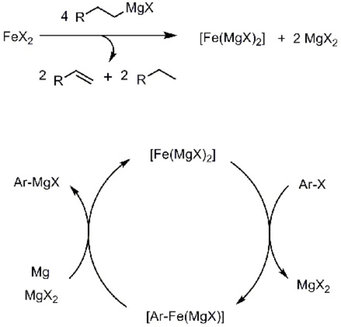
So konnte gezeigt werden, dass FeCl2 (2 Mol-%) die Bildung von C-Mg-Bindungen effektiv katalysiert, wobei wahrscheinlich einem in situ gebildeten, hoch reduzierten intermetallischen Cluster vom Typ [Fe(MgCl)2]n die entscheidende Rolle zukommt (Abb. 1). Dieses Verfahren unterscheidet sich grundsätzlich von den üblichen Methoden zur Induktion von Grignard-Reaktionen, bei denen mithilfe diverser Additiva die Magnesiumoberfläche aktiviert wird. Vielmehr schiebt sich die niedervalente Eisenverbindung in die Kohlenstoff-Halogen-Bindung des Substrats ArX ein; die sich anschließende reduktive Eliminierung der so gebildeten Organoeisen-Spezies liefert dann das gewünschte Grignard-Reagenz ArMgX. Daraus ergibt sich ein leistungsfähiger Katalysezyklus, mit dessen Hilfe sogar desaktivierte Arylchloride in die entsprechenden Organomagnesium-Verbindungen überführt werden können, die sonst nicht reagieren (Abb. 1) [3].

Kurz danach hat unsere Gruppe vorgeschlagen, dass derselbe niedervalente Eisencluster auch als Katalysator für C-C-Verknüpfungen dienen könnte [4]. Angeregt durch Pionierarbeiten von Kochi über Reaktionen von Alkenylhalogeniden mit Grignard-Verbindungen [5], die lange Zeit wenig Beachtung erhielten, gelang es mithilfe einfacher Eisensalze selbst reaktionsträge Arylchloride, -triflate und -tosylate effizient kreuzzukuppeln, wobei wiederum in situ gebildetes [Fe(MgCl)2]n die eigentlich katalytisch wirksame Spezies bilden dürfte (Abb. 2). Obschon dieser Prozess (bisher) nicht so universell ist wie seine Palladium-katalysierten Verwandten, erfolgen viele derartige Umsetzungen mit exzellenten Ausbeuten und präzedenzlosen Reaktionsgeschwindigkeiten und können problemlos auch im größeren Maßstab durchgeführt werden. Zudem erwiesen sich zahlreiche polare Gruppen als kompatibel, die an sich mit Organomagnesium-Verbindungen reagieren [4]. Dieses Verfahren hat sich in der Zwischenzeit bei der Darstellung verschiedener Wirkstoffe ebenso bewährt wie bei der Totalsynthese komplexer Naturstoffe. Ausgewählte Beispiele sind in Abbildung 3 zusammengefasst [6].

Seither haben viele Gruppen zur Erweiterung der Anwendungsbreite eisenkatalysierter Kreuzkupplungen beigetragen [6]. Besonders erwähnenswerte Entwicklungen betreffen den Einsatz von Alkylhalogeniden als elektrophile Reaktionspartner, die bei Verwendung von Palladiumkatalysatoren traditionell große Schwierigkeiten bereiten, mithilfe von Eisensalzen als Katalysatoren aber erstaunlich einfach zu kuppeln sind [6]. Dieser Befund zeigt, dass Eisen nicht bloß als Substitut für Edelmetalle fungieren kann, sondern sein Einsatz auch neue und originäre Möglichkeiten auftut. Ebenso erwähnenswert sind an dieser Stelle die jüngsten Erfolge im Bereich eisenkatalysierter Reaktionen unter Bildung von C-O- oder C-N-Bindungen [7].
Vom Empirischen zum Konzeptionellen
Um die Entwicklung der Eisenkatalyse zu verstetigen, bedarf es vordringlich aber der Entwicklung eines konzeptionellen Rahmens sowie eines besseren Verständnisses der metallorganischen Chemie dieses Metalls. Dem steht jedoch die extreme Empfindlichkeit und Reaktivität vieler Eisen-Kohlenstoff-Bindungen entgegen, wenn keine stabilisierenden Liganden im Komplexverband vorhanden sind. Auch der wahrscheinlich für die oben geschilderten Reaktionen verantwortliche intermetallische Eisencluster vom Typ [Fe(MgCl)2]n entzog sich aus den genannten Gründen bislang einer eingehenderen Charakterisierung.
Erst vor kurzem gelang es unserer Gruppe, grundlegende mechanistische Einblicke zu erhalten. So konnte gezeigt werden, dass zwischen mindestens zwei Arten eisenkatalysierter C-C-Verknüpfungen unterschieden werden muss. Zum einen sind offensichtlich hoch reaktive „Eisen-At“-Komplexe am Werk, von denen repräsentative Vertreter trotz ihrer enormen Empfindlichkeit isoliert und vollständig charakterisiert werden konnten; einige der dabei entdeckten Strukturtypen erwiesen sich als präzedenzlos [8]. Ist jedoch der vom Grignardreagenz auf das Eisen übertragene Rest zur β-Hydrid-Eliminierung fähig, so entstehen primär niedervalente Spezies, wie ursprünglich von Bogdanović postuliert [3].

Deren Struktur und Reaktivität ließ sich anhand wohl definierter intermetallischer Komplexe vom Typ 1 und 2 [9] studieren (Abb. 4). Darin liegt das Eisen in niederen, formal sogar negativen Oxidationsstufen (0 bzw. –II) vor, weist weitgehend kovalente Bindungen zu den eskortierenden Lithium-Atomen auf und ist an kinetisch labile Ethylen-Liganden gebunden. Solche Komplexe gehen bereitwillig oxidative Insertionen in aromatische, allylische, benzylische und aliphatische Halogenide ein, wie durch Isolierung und Strukturaufklärung der gebildeten, nicht-stabilisierten und außerordentlich empfindlichen Organoeisen-Verbindungen nachgewiesen werden konnte [8]. Auf diese Weise ließen sich erste unverrückbare Orientierungspunkte im bisher weitgehend unkartographierten Terrain der niedervalenten Eisenchemie festmachen.

Ausblick
Auch wenn es lange dauern wird, bis Eisen-katalysierte Kreuzkupplungen die Reife ihrer Palladium-katalysierten Verwandten erreichen werden, konnten im Verlauf des letzten Jahrzehnts dennoch erhebliche Fortschritte erzielt werden. Neben der empirischen Optimierung gelangen auch erste mechanistische Einblicke, die zuvor unmöglich schienen. Diese können den Weg für die Weiterentwicklung dieses vielversprechenden Gebietes weisen. Ferner zeichnet sich ab, dass die Eisenkatalyse über das Feld der Kreuzkupplung hinaus erhebliches Potenzial besitzt. So ließ sich zum Beispiel zeigen, dass auch Cycloadditionen und Cycloisomerisierungen von diesem Metall effektiv induziert werden können (Abb. 5) [10], die bislang ebenfalls den Edelmetallen Rhodium, Ruthenium oder Palladium vorbehalten schienen. War das Eisen für lange Zeit eine der wenigen verbleibenden Nischen im Periodensystem, was Anwendungen in der homogenen Katalyse betrifft, so beginnt sich dieses Vakuum in den letzten Jahren rasch zu füllen. Dies verspricht Entdeckungen von gleichermaßen grundlegender wie praktischer Bedeutung.