Forschungsbericht 2003 - Max-Planck-Institute für experimentelle Medizin
Die Gifte der Kegelschnecken - Lernen aus 50 Millionen Jahren Neuropharmakologie
Molekulare und Zelluläre Neuropharmakologie (Dr. Heinrich Terlau)
MPI für experimentelle Medizin, Göttingen
Kegelschnecken sind eine sehr erfolgreiche Gattung von Wirbellosen, die heute mit etwa 500 Arten überall auf der Welt in marinen Lebensräumen vorkommen. Ihre besonders schön gezeichneten Schalen weckten sehr früh das Interesse der Menschen und wurden bereits vor mehreren tausend Jahren für die Herstellung von Schmuck eingesetzt (Abb. 1).

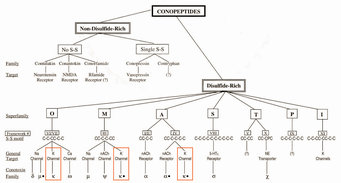
Heute erfahren neben den Schalen die Gifte dieser räuberisch lebenden Tiere ein zunehmendes wissenschaftliches Interesse. Das Gift einer Kegelschneckenart enthält bis zu 200 verschiedene aktive Bestandteile, die Conotoxine. Dabei handelt es sich um kurzkettige Peptide, die in der Regel mehrere Cysteine enthalten, schwefelhaltige Aminosäuren, und durch eine außergewöhnliche Variabilität und Spezifität gekennzeichnet sind [5]. Die bisher bekannten Conotoxine sind anhand ihrer Cysteinbrücken und ihrer Zielmoleküle eingeteilt worden (Abb. 2).
Die Wissenschaftler gehen davon aus, dass jede Kegelschneckenart im Laufe der 50 Millionen Jahre ihrer Evolution einen eigenen Giftcocktail entwickelt hat. Demzufolge enthalten die Gifte dieser Tiere eine im Tierreich einmalige Vielfalt von wahrscheinlich mehreren zehntausend hochspezialisierten pharmakologisch aktiven Substanzen. Bisher ist jedoch erst die Wirkungsweise einiger weniger dieser Toxine bekannt. Aufgrund ihrer besonderen Eigenschaften werden die charakterisierten Conotoxine bereits intensiv in den Neurowissenschaften eingesetzt. Ihre hohe Wirkspezifität macht sie auch interessant für klinische Anwendungen. Ein großer potenzieller Anwendungsbereich zeichnet sich für Substanzen ab, die zum Beispiel mit spannungsabhängigen Natriumkanälen oder Kaliumkanälen interagieren; diese könnten als Lokalanästhetika, Antiarrhythmika oder Antikonvulsiva eingesetzt werden. Mehrere Conotoxine befinden sich bereits in der klinischen Testung.
Kaliumkanäle als Zielmoleküle von Conotoxinen
Kaliumkanäle sind eine sehr heterogene Gruppe von Ionenkanälen, die an den unterschiedlichsten physiologischen Vorgängen beteiligt sind. Bekannt sind bereits mehr als 70 Gene, die für Kaliumkanäle kodieren. Für die elektrische Erregbarkeit von Zellen sind diese Kanäle enorm wichtig, da sie für die Form der Aktionspotenziale mit verantwortlich sind. Die Gifte verschiedenster Organismen wie Schlangen, Skorpione, Seeanemonen und Spinnen enthalten eine Vielzahl von Polypeptidtoxinen, die an Kaliumkanäle binden und für den Beutefang wichtig sind.
Interessanterweise sind trotz der großen Vielzahl der verschiedenen Kaliumkanäle bei Kegelschnecken nur wenige Conotoxine bekannt, die mit diesen Ionenkanälen interagieren. Das Team von Heinrich Terlau war bei der Charakterisierung von drei neuen Familien von Conotoxinen beteiligt, die an spannungsabhängige Kaliumkanäle binden (siehe Abb. 2).
1. κ-Conotoxine
Das erste Conotoxin, bei dem die Forscher zeigen konnten, dass es spannungsabhängige Kaliumkanäle blockiert, ist κ-Conotoxin PVIIA (κ-PVIIA), welches aus der fischfangenden Art Conus purpurascens isoliert wurde. κ-PVIIA bindet an die extrazelluläre Seite der Ionenkanalpore in einer bimolekularen Reaktion. Die Interaktionsfläche des Peptids mit der Ionenkanalpore konnte identifiziert werden. Wie andere Kaliumkanal-blockierende Peptide enthält κ-PVIIA ein so genanntes kritisches Dyaden-Motiv aus zwei Aminosäuren, das wichtig für die Blockierung des Kaliumkanals ist. Für κ-PVIIA besteht diese Dyade aus den Aminosäuren Lysin-7 und Phenylalanin-9, wobei davon ausgegangen werden muss, dass Lysin-7 die Ionenkanalpore blockiert.
2. κA-Conotoxine
Das Peptid κA-Conotoxin SIVA wurde aus dem Gift der fischfangenden Art Conus striatus identifiziert. Das Disulfidbrückenmuster von κA-SIVA ist komplett verschieden von dem von κ-PVIIA. Die aktive Form von κA-SIVA enthält ein O-glycosyliertes Serin an Position 7. Dies ist der erste Beweis für eine O-Glycosylierung als post-translationale Modifizierung eines biologisch aktiven Conotoxins.
3. κM-Conotoxine
Die κM-Conotoxine enthalten das gleiche Cysteinbrückenmuster wie die μ-Conotoxine und die ψ-Conotoxine (Abb. 2). Das erste bekannte Peptid dieser Familie, κM-RIIIK, zeigte im Gegensatz zu den strukturell ähnlichen μ-Conotoxinen keine Effekte auf Natriumkanäle - Conotoxine mit ähnlichem Cysteinmuster können demnach unterschiedliche pharmakologische Eigenschaften haben (siehe unten). Ein humaner Kaliumkanal (Kv1.2) konnte als Zielmolekül dieses Peptides identifiziert werden, wobei κM-RIIIK wahrscheinlich mit der Pore in Wechselwirkung tritt [1;2].
Mittlerweile identifizierte die Arbeitsgruppe am Max-Planck-Institut für experimentelle Medizin mindestens drei weitere Familien von Conotoxinen, die mit spannungsabhängigen Kaliumkanälen interagieren (unveröffentlichte Ergebnisse). Interessanterweise haben alle diese Peptide andere Cysteinbrückenmuster als die drei oben beschriebenen Familien, wobei eine Gruppe zur I-Superfamilie gehört (Abb. 2). Diese Ergebnisse zeigen, dass Kegelschnecken im Laufe der Evolution verschiedenste Peptide entwickelt haben, die mit Kaliumkanälen interagieren und die "darauf warten, entdeckt zu werden". Sie sind von besonderem Interesse, da die große Variationsbreite von Kaliumkanälen in Kombination mit der Ausbildung von Kanälen, die sich aus verschiedenen Untereinheiten zusammensetzen (so genannte Heteromere), eine besonders "hoch entwickelte" Pharmakologie benötigt, die dann von der Grundlagenforschung bis zur Klinik eingesetzt werden kann.
Gating versus Toxinbindung
Bei ihrer Aktivierung machen spannungsabhängige Ionenkanäle eine Konformationsänderung ("gating") durch, die unter physiologischen Bedingungen zu einem selektiven Kationenfluss durch die Pore führt. Von diesem "Offen-Zustand" aus können spannungsabhängige Ionenkanäle entweder durch eine weitere Konformationsänderung inaktiviert werden, wobei in diesem Zustand kein Ionenfluss mehr stattfindet, oder die Kanäle deaktivieren, indem sie sich schließen (Abb. 3).
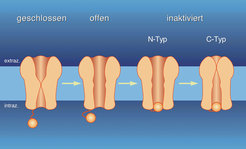
Somit sind Ionenkanäle Zielmoleküle ("Targets"), die während ihrer Aktivität verschiedene Konformationszustände einnehmen, welche wiederum unterschiedliche pharmakologische Eigenschaften haben können. Entsprechend dieser Mechanismen sollte man erwarten, dass die Interaktion einer Substanz mit dem Ionenkanal von der Konformation des Targets abhängt. Eine konformationsabhängige Bindung an spannungsabhängige Ionenkanäle ist tatsächlich nicht nur für die klassischen Natriumkanalblocker Tetrodotoxin und Saxitoxin, sondern auch für Lokalanästhetika und andere in der Klinik eingesetzte Substanzen bekannt.
Für bestimmte therapeutische Anwendungen kann die Konformationsabhängigkeit der Bindung den Vorteil haben, dass die Ionenkanäle nur in einer bestimmten Konformation beeinflusst werden. Die Wissenschaftler in Göttingen haben zeigen können, dass die Bindung von κ-PVIIA aber auch von κM-RIIIK für den geschlossenen und offenen Zustand des Ionenkanales unterschiedlich ist. Ferner zeigte sich überraschenderweise, dass schnelle C-Typ-Inaktivierung und κ-PVIIA-Bindung sich gegenseitig ausschließen [4]. Dies ist von größerer funktioneller Bedeutung, da unter bestimmten Bedingungen die Bindung des Kaliumkanalblockers κ-PVIIA zu einem vergrößerten Kaliumstrom führen kann und somit die Wirkung des Peptids invertiert ist. Diese Ergebnisse zeigen eindeutig, dass die Bindung von Polypeptid-Antagonisten eine Konformationsabhängigkeit mit funktioneller Relevanz besitzt.
Strukturelle Ähnlichkeit versus pharmakologische Spezifität
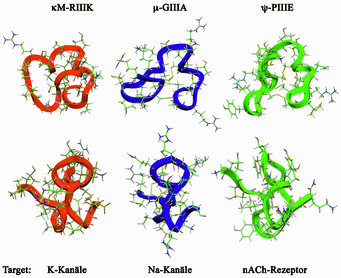
Alle drei Familien von Conotoxinen, die an Kaliumkanäle binden, enthalten ein eigenes Cysteingrundgerüst (siehe Abb. 2), was zeigt, dass Kegelschnecken im Laufe der Evolution strukturell unterschiedliche Moleküle mit ähnlichen pharmakologischen Eigenschaften entwickelt haben. Es stellt sich die Frage, wie strukturell unterschiedliche Moleküle funktionelle Ähnlichkeiten haben können. Interessanterweise wurden für die bekannten Neurotoxine, die an Kaliumkanäle binden, auch unabhängig von den strukturellen Unterschieden konvergente Eigenschaften postuliert: Eine Vielzahl von Toxinen unterschiedlicher Organismen, wie Charybdotoxin aus dem Gift eines Skorpions oder Dendrotoxin aus Schlangen, besitzen ein Dyaden-Motiv von zwei Aminosäuren, welches aus einem Lysin und einer hydrophoben, meistens aromatischen Aminosäure besteht und als kritischer Bestandteil dieser Peptide für die Bindung an den Kaliumkanal angesehen wird. Die Wissenschaftler gehen davon aus, dass hierbei das Lysin die Kaliumkanalpore blockiert. Wie bereits beschrieben enthält κPVIIA diese funktionelle Dyade, obgleich es keine offensichtlichen strukturellen Ähnlichkeiten mit anderen Polypeptid-Toxinen aufweist, die diese Dyade enthalten. Im Gegensatz hierzu enthält κM-RIIIK keine aromatische Aminosäure, was auf einen anderen Mechanismus der Bindung hinweist. Erst kürzlich konnten wir in einer Zusammenarbeit mit Teresa Carlomagno, Max-Planck-Institut für biophysikalische Chemie, Göttingen, zeigen, dass der Pharmacophor dieses Peptides vollkommen unterschiedlich zu der postulierten Dyade ist. Auf der anderen Seite zeigte sich, dass die Struktur von κM-RIIIK sehr ähnlich ist zu den bekannten Strukturen der μ-Conotoxine, bei denen es sich um hochselektive Blocker von Natriumkanälen des Skelettmuskels handelt und ψ-Conotoxine, welche nichtkompetetive Blocker von Acetylcholinrezeptoren sind (Abb. 4).
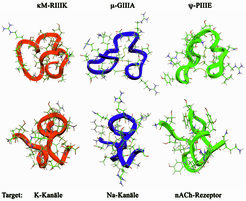
Somit befindet sich κM-RIIIK an einem einzigartigen Schnittpunkt zwischen struktureller Ähnlichkeit und ähnlicher pharmakologischer Spezifität. κM-Conotoxin RIIIK und κ-Conotoxin PVIIA binden beide die gleichen Kaliumkanalsubtypen, sind jedoch strukturell verschieden und binden mit unterschiedlichen Mechanismen. Im Gegensatz hierzu ist κM-Conotoxin RIIIK strukturell ähnlich zu den genetisch verwandten Conotoxinen, die pharmakologische Spezifität ist jedoch komplett verschieden (Kaliumkanäle, Natriumkanäle, Acetylcholinrezeptoren). Dies könnte ein mögliches Grundgerüst für das Verständnis von molekularer Konvergenz und Divergenz für Liganden von Ionenkanälen bilden.
Literatur
[1] Al-Sabi, A., D. Lennarz, M. Ferber, J. Gulyas, J. Rivier, B.M. Olivera, T. Carlomagno and H. Terlau: κM-conotoxin RIIIK, structural and functional novelty in a K+ channel antagonist. Biochemistry, in press (2004).
[2] Ferber, M., A. Sporning, G. Jeserich, R. DeLaCruz, M. Watkins, B.M. Olivera and H. Terlau: A novel Conus peptide ligand for K+ channels. Journal of Biological Chemistry 278, 2177-2183 (2003).
[3] Ferber, M., A. Al-Sabi, M. Stocker, B.M. Olivera and H. Terlau: Identification of a mammalian target of κM-conotoxin RIIIK. Toxicon 43, 915-921 (2004).
[4] Koch, D.E., B.M. Olivera, H. Terlau and F. Conti: The binding of κ-conotoxin PVIIA and fast C-type inactivation Shaker K+-channels are mutually exclusive. Biophysical Journal 86, 191-209 (2004).
[5] Terlau, H and B.M. Olivera: Conus venoms: A rich source of novel ion channel-targeted peptides. Physiological Reviews 84, 41-68 (2004).