Forschungsbericht 2013 - Max-Planck-Institut für biologische Intelligenz (Standort Seewiesen)
Gene und Umwelt: Wie beeinflussen sie Verhalten und Physiologie bei Singvögeln?
Einfluss der Gene und der Umwelt auf das Verhalten
Seit Langem ist die Frage, zu welchen Anteilen das Verhalten genetisch bedingt ist oder durch Umwelteinflüsse geformt wird, ein zentrales Thema in der Verhaltensforschung. Heute weiß man, dass unsere Persönlichkeit und unser Verhalten weit weniger stark durch die Gene bestimmt wird, als man früher angenommen hat. Besonders während der Jugendentwicklung können Umweltfaktoren über sogenannte epigenetische Effekte einen entscheidenden Einfluss auf die Ausbildung von Gehirn und Verhalten haben. Epigenetische Mechanismen regulieren über Modifikation der Gene oder des Chromatins, in welchem Maße die Gene aktiviert werden. Ob der Einfluss der Umwelt stark oder schwach ausfällt, kann aber wiederum entscheidend von der genetischen Veranlagung abhängen. Erb- und Umweltfaktoren sind daher nach wie vor schwer auseinanderzuhalten.
Einfluss der Umweltfaktoren auf die Brutaktivität bei Kanarengirlitzen

Umweltfaktoren können festgelegte Verhaltensweisen grundlegend beeinflussen. Zum Beispiel steuert die jahreszeitliche Veränderung in der Tageslänge, auch Photoperiode genannt, bei Tieren der gemäßigten Zonen die Jahresrhythmik und ermöglicht ihnen, sich in Zeiten von günstigen Umweltbedingungen fortzupflanzen. Dies ist wichtig für die Aufzucht der Nachkommen und so entscheidend für die biologische Fitness [1]. Ein sehr gut untersuchtes Phänomen ist die zeitliche Regulierung des Brutbeginns bei Vögeln: Die zunehmende Tageslänge im Frühling bewirkt einen Anstieg der Konzentration von Geschlechtshormonen im Blut. Wir sprechen dabei von der Photoperiode als proximatem Faktor, da dieser alleine ausreicht, grundlegende Änderungen im Verhalten und in der Physiologie auszulösen. Zusätzliche Faktoren, wie Nahrungsangebot, Niederschlagsmenge und soziale Interaktionen, dienen saisonal brütenden Vogelarten dann zur Feinabstimmung der Brutaktivität. Jedoch können bei günstigen Bedingungen diese zusätzlichen Faktoren auch allein eine Brutaktivität auslösen. Zum Beispiel konnte Stefan Leitner und sein Team bei Kanarengirlitzen (Serinus canaria, Abb. 1) experimentell zeigen, dass das Vorhandensein von wachsenden Grünpflanzen ausreicht, um während der kürzesten Tage im Jahr die Brutaktivität auszulösen – bis zu zwei Monate vor dem eigentlichen Brutbeginn! Normalerweise brüten die Vögel bei solch kurzen Tageslängen (sogenannter Kurztag) nicht. Um diesen Effekt zu erhalten, muss jedoch den Tieren unter Kurztag-Bedingungen voller Zugang zu den wachsenden Grünpflanzen gewährleistet werden (Abb. 2). Bietet man den Tieren nur einzelne Komponenten einer Pflanze an, wie Pflanzengeruch als olfaktorischen oder Kunstpflanzen als visuellen Reiz, erfolgt keine vorzeitige Brutaktivität [2]. Jedoch fangen nicht alle beobachteten Tiere gleichzeitig mit dem Brüten an, sie reagieren also unterschiedlich stark auf die Umweltreize. Dies spiegelt eine Variation der Merkmalsausprägung (phänotypische Variation) im Verhalten und in der Physiologie wider.

Ursachen phänotypischer Variation
Wenn man erklären will, wie genetische Variation in einem Merkmal aufrechterhalten wird, obwohl das Merkmal Selektionskräften unterliegt, muss man die Ursachen für die phänotypische Variation eines Verhaltensmerkmals untersuchen [3]. Um festzustellen, wie sich die komplexen Gesänge der Singvögel durch Evolution herausgebildet haben, müssen wir die genetische Variation und die Art der Umweltfaktoren messen, die für die Ausprägung der Gesänge verantwortlich sind, sowie alle Wechselbeziehungen zwischen beiden. Die Bestimmung solcher Genotyp-Umwelt-Wechselwirkungen (GxE) ist wichtig, denn sie zeigen den Bereich der Merkmalsausprägung auf, den ein Genotyp unter sich ändernden Umweltbedingungen zeigen kann, und legen fest, ob ein Merkmal wie der Vogelgesang die erblichen Eigenschaften eines Individuums signalisieren kann (siehe [4] für eine Übersicht). Somit sind Singvögel ein wichtiges Modell, um Verhaltens- und Gehirnkorrelationen zu untersuchen. Beim Zebrafink (Taeniopygia guttata) beispielsweise besitzen wesentliche Gesangsparameter wie die Anzahl der Silben oder die Länge der Gesangsphrasen eine geringe Erblichkeit und sind eher von sich ändernden Umweltbedingungen abhängig [5]. Gehirnstrukturen, die für die Steuerung des Gesanges verantwortlich sind, haben dagegen eine höhere Erblichkeit [6].
Diese Ergebnisse aus früheren Studien lassen vermuten, dass die Gesangsstruktur und die ihr zugrundeliegenden sogenannten Gesangskerne im Gehirn von einer Kombination aus sich ändernden Umweltbedingungen und der genetischen Ausstattung eines Tieres abhängen. Jedoch besteht die Möglichkeit, dass bestimmte Genotypen stärker als andere auf ungünstige Umweltbedingungen reagieren, was durch die sogenannte Entwicklungsstress-Hypothese (engl. developmental stress) gezeigt wurde. Diese Hypothese besagt, dass der sich entwickelnde Organismus bei ungünstigen Umweltbedingungen während der Jugendentwicklung, wie Nahrungsknappheit, Ressourcen von Organen wie dem sich entwickelnden Gehirn abzieht und eher in die Entwicklung von lebenswichtigen Körperfunktionen steckt [7]. Der Gesang stellt also ein „ehrliches Signal“ für den Empfänger dar, um eine gute körperliche Verfassung des Senders anzuzeigen. Um ehrlich zu sein, muss ein Signal wie der Vogelgesang im Individuum durch entsprechende physiologische Grundlagen gestützt werden. Zum Beispiel wäre ein geschwächtes Tier nicht in der Lage, einen kunstvollen Gesang zu produzieren. Allgemein erwartet man, dass solche Signale mit hohen Kosten für den Sender verbunden sind, damit sie ehrlich bleiben. Obwohl also die Bedeutung der genetischen und umweltbedingten Einflüsse auf das Gesangslernen bei Singvögeln innerhalb der letzten vierzig Jahre mehrmals untersucht wurde, gab es bislang keine Studie, die den Einfluss beider Faktoren in Bezug auf die neuronale Kontrolle des Gesanges untersucht hat.
Untersuchung der Interaktion von Genetik und Umweltfaktoren bei Zebrafinken

In einem Langzeitexperiment an Zebrafinken wurden zusammen mit Kollegen aus England und Australien nun die Genotyp-Umwelt-Wechselwirkungen untersucht. In diesem Experiment wurden zwei wichtige Umweltfaktoren verändert: die Nahrungsverfügbarkeit während der Jugendentwicklung und die für das Gesangslernen von jungen Männchen wichtige akustische Umgebung. Um den jeweiligen Beitrag des Genotyps und der Umweltbedingungen zu bestimmen, die für eventuelle Unterschiede bei der Gehirn- und Gesangsentwicklung verantwortlich sind, wurde ein sogenannter partieller cross-fostering Ansatz gewählt. Dabei wird jeweils die Hälfte eines Geleges ausgetauscht und anderen Eltern untergeschoben, so dass die Hälfte der Eier in jedem Nest sozusagen aus “Kuckuckseiern“ besteht. Somit wuchs eine Hälfte der geschlüpften Jungvögel bei den eigenen Eltern auf, während die andere Hälfte von Stiefeltern großgezogen wurde (Abb. 3). Bei einer Hälfte der Paare wurde die Menge an verfügbarem Körnerfutter durch kontrollierte Zugabe von wertlosen Spelzen beschränkt (sogenannter Futterstress). Auf diese Weise müssen die Elterntiere längere Zeit mit der Futtersuche verbringen und haben so weniger Zeit, sich um die Jungtiere zu kümmern und sie zu füttern. Zudem haben die Männchen weniger Zeit zu singen, was die Gesangsentwicklung junger Männchen beeinflussen könnte. Eine Nahrungsbeschränkung der Elterntiere war notwendig, um eine größere und vor allem kontrollierte Variation in den Umweltbedingungen herzustellen. Abgesehen von der akustischen Umgebung, also der Zuordnung der Jungtiere zu dem Gesang des leiblichen, beziehungsweise des Stiefvaters, können die restlichen, eher unspezifischen Umweltfaktoren wie Fütterungsraten, Nesttemperatur oder tatsächliche Gesangsaktivität der Väter im Experiment nicht in kontrollierter Weise verändert werden. Tatsächlich hatte die Nahrungsknappheit einen Einfluss auf die Entwicklung der Jungtiere [8; 9]: Weibchen, die während der Aufzuchtphase jenem Futterstress ausgesetzt waren, waren bei Partnerwahlversuchen weniger aktiv als Weibchen, die normal aufwuchsen. Allerdings bevorzugten diese Weibchen die Gesänge männlicher Zebrafinken in gleicher Weise wie normal aufgezogene Weibchen.
Auswirkungen auf Gesangs- und Gehirnstruktur
Im Langzeitexperiment ergab zunächst ein Vergleich der Blutplasma-Konzentrationen des Stresshormons Kortikosteron leicht erhöhte Werte bei männlichen und weiblichen Nachkommen, die unter Futterstress-Bedingungen aufwuchsen. Abbildung 4 zeigt die Anteile, die die genetische Herkunft, die Aufzuchtbedingungen und die Wechselwirkungen zwischen Genotyp und Futterstress zur Ausbildung der phänotypischen Variation beitragen. Die Berechnung dieser Anteile erfolgte sowohl durch Vergleiche zwischen zwei Brüdern, die in verschiedenen Nestern aufwuchsen, als auch durch Vergleiche von Vätern und Söhnen.
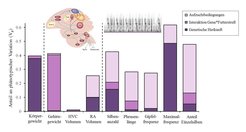
Die Ergebnisse zeigen, dass die Gesänge der männlichen Nachkommen mit denen ihrer Väter nur wenig übereinstimmen. Einzig die Anzahl der Silben und die Maximalfrequenz eines jungen Männchens hängt mit der Silbenanzahl des leiblichen Vaters stärker zusammen. Bei der lautesten Gesangsfrequenz und dem Anteil einzigartiger Gesangssilben der Söhne wiederum gibt es eine stärkere Übereinstimmung mit dem Gesang des Stiefvaters, letztere besteht jedoch nur bei ausreichendem Nahrungsangebot. Noch bemerkenswerter waren die Ergebnisse bei der Gehirnstruktur: Sie wird kaum vererbt und ist in hohem Maße von den Umweltbedingungen abhängig. Von daher ist die individuelle Variation in der Größe des sogenannten HVC, einer Gehirnregion, die für das Gesangslernen und die Gesangsproduktion verantwortlich ist, fast vollständig von verschiedensten Umweltbedingungen abhängig. Weiterhin kann ein unter Normalbedingungen bestehender Zusammenhang zwischen der Gehirngröße von Vater und Sohn durch Veränderung der Bedingungen während der Aufzucht, z.B. Futterstress, aufgelöst werden. Diese Ergebnisse sind umso erstaunlicher, da man in den früheren Studien von einer recht hohen Vererbbarkeit der dem Gesang zugrundeliegenden Gehirnstrukturen ausgegangen war. Damals hatte man allerdings die Bedeutung der Umweltbedingungen außer Acht gelassen. So kann eine hohe Empfindlichkeit gegenüber Umweltfaktoren die genetische Vielfalt aufrechterhalten. Sie hat somit großen Einfluss auf die Gesangs- und Gehirnentwicklung beim Singvogel [10]. Die Ergebnisse zeigen die große Bedeutung der Umweltbedingungen für die Ausprägung von komplexen Verhaltensweisen und die neuronale Entwicklung bei Wirbeltieren.



