Forschungsbericht 2019 - Max-Planck-Institut für Struktur und Dynamik der Materie
Die Gestaltungsprinzipien der Natur auf atomaren und elektronischen Zeitskalen
Eike C. Schulz, Robert Bücker, Günther H. Kassier, Hong Guan Duan, R.J. Dwayne Miller
Abteilung Dynamik in Atomarer Auflösung am Max-Planck-Institut für Struktur und Dynamik der Materie, Hamburg
Wie können wir diese verschiedenen räumlichen und zeitlichen Skalen erklären? Gibt es ein allgemeines Prinzip bei der Optimierung von Struktur-Funktionsbeziehungen in der Biologie?
Die Miller-Gruppe hat einen Weg gefunden, um hierfür relevante Experimente nicht nur erheblich zu vereinfachen, sondern auch die Datenerfassung massiv zu beschleunigen und die Bildrekonstruktionsmethoden zu verbessern.
Der bedeutendste Fortschritt ist die Entwicklung von Methoden zur vollständigen Auflösung enzymatischer Reaktionen mithilfe eines einzigartigen kristallografischen Chipkonzepts mit strukturierter Zeitabtastung, um vollständige enzymatische Zyklen unter Verwendung leicht zugänglicher Synchrotron-Mikrofokus-Beamlines abzubilden.
Bisherige Annahmen von langlebigen elektronischen Zusammenhängen erwiesen sich als falsch, standen jedoch eher in Verbindung mit geringfügigen Vibrationen. Diese Arbeit zeigt, dass die Natur Dissipationsprozesse, die Dekohärenz verursachen, nicht vermeidet.
Im Gegenteil: Sie nutzt die Dissipation gezielt, um den Prozess durch optimierte Energiegradienten intensiv zu steuern. Dieser Mechanismus ist praktisch dieselbe grundlegende Physik, die die Natur auf längeren Zeitskalen nutzt: Dort lenken freie Energiegradienten, die durch Dissipation in der Energie abwärtsgerichtet sind, die Chemie und hauchen ansonsten unbelebten Objekten Leben ein.
Atomare Sicht auf die erstaunlichen molekularen Maschinen der Natur bei der Arbeit
Eine der wenigen Methoden zum Verständnis der biomolekularen Dynamik ist die zeitaufgelöste Röntgenkristallographie. Dabei wird die Reaktion eines biologischen Moleküls im Inneren der Kristalle ausgelöst und mit Momentaufnahmen abgebildet.
Allerdings sind diese Experimente äußerst zeitaufwändig. Erst nach mehreren Stunden Datenerfassung entsteht eine einzige strukturelle Momentaufnahme.
![Abb.1: Die “hit-and-return” (HARE) Methode vereinfacht es Biomoleküle bei der Arbeit zu beobachten.Jahrzehntelang lieferte die Röntgenkristallographie unübertroffene Einblicke in die Struktur von Molekülen, und entschlüsselte gleichzeitig die Position einzelner Atome. Eine der wenigen Methoden zum Verständnis der biomolekularen Dynamik ist die zeitaufgelöste Röntgenkristallographie. Dabei wird die Reaktion eines biologischen Moleküls im Inneren der Kristalle ausgelöst, und dann werden Momentaufnahmen gemacht, während es reagiert. Allerdings waren diese Experimente traditionell äußerst zeitaufwändig. Die vom Miller-Labor entwickelte neue Hit-and-Return-Methode [1] ist auf die Untersuchung von biologisch relevanten Reaktionszeitskalen zugeschnitten, die in der Größenordnung von Millisekunden bis Sekunden oder sogar Minuten liegen.](/13622075/original-1604834954.jpg?t=eyJ3aWR0aCI6MjQ2LCJvYmpfaWQiOjEzNjIyMDc1fQ%3D%3D--f894d6d3036a795e019a8a6b0d08d82550b4ad60)
Jahrzehntelang lieferte die Röntgenkristallographie unübertroffene Einblicke in die Struktur von Molekülen, und entschlüsselte gleichzeitig die Position einzelner Atome. Eine der wenigen Methoden zum Verständnis der biomolekularen Dynamik ist die zeitaufgelöste Röntgenkristallographie. Dabei wird die Reaktion eines biologischen Moleküls im Inneren der Kristalle ausgelöst, und dann werden Momentaufnahmen gemacht, während es reagiert. Allerdings waren diese Experimente traditionell äußerst zeitaufwändig. Die vom Miller-Labor entwickelte neue Hit-and-Return-Methode [1] ist auf die Untersuchung von biologisch relevanten Reaktionszeitskalen zugeschnitten, die in der Größenordnung von Millisekunden bis Sekunden oder sogar Minuten liegen.
Die vom Miller-Labor entwickelte neue Hit-and-Return-Methode [1] beschleunigt das gesamte Experiment, weil sie eine effiziente Abtastung von Zeitpunkten durch das parallele, zeitsegmentierte Abtasten verschiedener Kristalle ermöglicht.
In Kombination mit den auf mikrofokussierten Synchrotron-Beamlines verfügbaren hochintensiven Röntgenstrahlen werden viele Momentaufnahmen nacheinander erfasst. Es entsteht eine Zeitrafferaufnahme, die die Strukturänderungen während der vollständigen Reaktion eines Biomoleküls in einem einzigen 24-Stunden-Experiment zeigt.
Die Methode ist sie auf die Untersuchung von biologisch relevanten Reaktionszeitskalen zugeschnitten (z.B. den Umsatz eines Arzneimittels), die von Millisekunden bis zu Sekunden oder sogar Minuten andauern.
So konnten die Forscher ein wichtiges Enzym für das Aufbrechen der C-F-Bindung – die stärkste Einfachbindung in der Natur – auf der Millisekunden-Zeitskala abfragen. Sie verfolgten die Nutzung der gespeicherten potentiellen Energie in den thermischen Schwankungen des Enzyms, um die Umgebung des aktiven Zentrums und die damit verbundene Barrierehöhe zu regulieren und die Wärmeenergie effektiv zum Lösen selbst der stärksten Bindungen zu fokussieren.
Dieses neue Verfahren birgt großes Potenzial für bestehende und entstehende Synchrotronstrahlungsquellen mit hoher Brillanz. Der weitaus größere Dynamikbereich und das effiziente Zeitmanagement werden es wesentlich mehr Forschern ermöglichen, zeitaufgelöste Kristallographiestudien durchzuführen.
Gemeinsam mit dem EMBL und der Universität Hamburg wird die Hit-and-Return-Methode bereits als Standard-Probenumgebung für die neue zeitaufgelöste makromolekulare Kristallographie-Endstation auf der EMBL-Beamline P14-2 im PETRA-III-Synchroton des DESY implementiert.
Ein vertieftes Verständnis der grundlegenden biochemischen Prozesse wird dazu beitragen, wichtige Fragen bezüglich unserer Gesundheit und unserer Umwelt zu beantworten.
Die Natur nutzt die lokale Energieverteilung, um die Energieübertragungswege bei der Photosynthese effizient zu steuern
Die Photosynthese fängt Sonnenenergie ein, um Kohlendioxid in Biomasse umzuwandeln. Während des ersten Schritts der Photosynthese wird die Energie der Sonnenphotonen in elektronische Anregungsenergie der Lichtsammelkomplexe mit Einheitsquanteneffizienz umgewandelt.
Der Quantenaspekt der Lichtabsorption und die Wahrnehmung von Farbe veranlassten Schrödinger dazu, die Möglichkeit von Quanteneffekten in biologischen Systemen zu erwägen, besonders nachdem die Quantenmechanik erfolgreich auf die Chemie angewendet wurde.
Jüngste Studien deuteten darauf hin, dass die Phase der Quantenkohärenz-Effekte tatsächlich dazu beiträgt, einen der schnellsten Prozesse in der Natur zu steuern, nämlich den Energietransport von den Lichtsammelsystemen zu dem speziellen Paar, das am Photosyntheseprozess beteiligt ist.
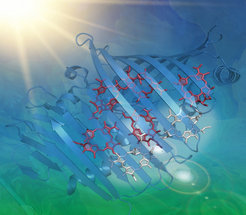
Abb.1: Der Energietransfer im natürlichen photosynthetischen Komplex (FMO-Komplex) zeigt die geringfügige, kurzlebige elektronische Kohärenz und demonstriert, dass die bisherigen Vorstellungen von langlebiger elektronischer Kohärenz falsch sind. Diese Arbeit zeigt, dass die Natur den Dekohärenz verursachenden Dissipationsprozess nicht vermeidet, sondern die Dissipation nutzt, um den Prozess durch optimierte Energiegradienten stark zu steuern.
Diese Arbeiten trugen dazu bei, das Gebiet der Quantenbiologie einzuführen, doch es gab quälende Inkonsistenzen bezüglich der Daten und einen allgemeinen Mangel an theoretischer Unterstützung für die Beobachtungen.
Aus diesem Grund haben Miller und Thorwart (UHH) den Energieübertragungsprozess im Fenna-Matthews-Olson-(FMO)-Komplex, einem der einfachsten natürlichen Proteinkomplexe zur Übertragung der Fotoenergie von der Antenne zum Reaktionszentrum, erneut untersucht.
Statt eines kohärenten Energietransfers entdecket das Forscherteam, dass die Lebensdauer der elektronischen Kohärenz schlicht zu kurz war, um eine funktionell wichtige Rolle zu spielen. Die durch Lichtabsorption hervorgerufene Dekohärenz der elektronischen Polarisation wird durch starke dissipative Wechselwirkung innerhalb der Proteinumgebung zerstört.
Anstatt dass die Natur die Proteinumgebung anpasst, um Bewegungen zu korrelieren und die Kohärenz zu bewahren, nutzt sie die unvermeidlichen dissipativen Prozesse der lokalen Energielandschaft, um den Weg zur direkten Energieübertragung freizumachen.
Dieses scheinbar einfache Konzept macht das System in der angegebenen Funktion, Energie von Punkt A zu Punkt B zu leiten, außerordentlich robust. Vorausgesetzt, dass der FMO-Komplex in Form und Funktion nahezu identisch ist und dass alle für die Charakterisierung des Systems (Chlorophyll-Antennen) und des Bades (umgebende Proteinumgebung) relevanten Parameter in allen Photosynthesesystemen gleich sind, wird erwartet, dass diese Entdeckung allgemeine Gültigkeit hat und Annahmen von langlebigen Zusammenhängen in Frage stellt, die in der Biologie eine wichtige Rolle spielen [2]+[3].
Zusammenhängen in Frage stellt, die in der Biologie eine wichtige Rolle spielen [2]+[3].
![Abb.1: Die “hit-and-return” (HARE) Methode vereinfacht es Biomoleküle bei der Arbeit zu beobachten.Jahrzehntelang lieferte die Röntgenkristallographie unübertroffene Einblicke in die Struktur von Molekülen, und entschlüsselte gleichzeitig die Position einzelner Atome. Eine der wenigen Methoden zum Verständnis der biomolekularen Dynamik ist die zeitaufgelöste Röntgenkristallographie. Dabei wird die Reaktion eines biologischen Moleküls im Inneren der Kristalle ausgelöst, und dann werden Momentaufnahmen gemacht, während es reagiert. Allerdings waren diese Experimente traditionell äußerst zeitaufwändig. Die vom Miller-Labor entwickelte neue Hit-and-Return-Methode [1] ist auf die Untersuchung von biologisch relevanten Reaktionszeitskalen zugeschnitten, die in der Größenordnung von Millisekunden bis Sekunden oder sogar Minuten liegen. Abb.1: Die “hit-and-return” (HARE) Methode vereinfacht es Biomoleküle bei der Arbeit zu beobachten.Jahrzehntelang lieferte die Röntgenkristallographie unübertroffene Einblicke in die Struktur von Molekülen, und entschlüsselte gleichzeitig die Position einzelner Atome. Eine der wenigen Methoden zum Verständnis der biomolekularen Dynamik ist die zeitaufgelöste Röntgenkristallographie. Dabei wird die Reaktion eines biologischen Moleküls im Inneren der Kristalle ausgelöst, und dann werden Momentaufnahmen gemacht, während es reagiert. Allerdings waren diese Experimente traditionell äußerst zeitaufwändig. Die vom Miller-Labor entwickelte neue Hit-and-Return-Methode [1] ist auf die Untersuchung von biologisch relevanten Reaktionszeitskalen zugeschnitten, die in der Größenordnung von Millisekunden bis Sekunden oder sogar Minuten liegen.](/13622075/original-1604834954.jpg?t=eyJ3aWR0aCI6MzQxLCJmaWxlX2V4dGVuc2lvbiI6ImpwZyIsIm9ial9pZCI6MTM2MjIwNzV9--606f923e514e5b5f6a4daa4cd047c22ec382764a)
