Forschungsbericht 2016 - Max-Planck-Institut für biologische Kybernetik
Die Abbildung von Gehirnfunktionen über einzelne Blutgefäße mit einer multi-modalen fMRT-Plattform
Mit der Magnetresonanztomographie (MRT) werden physikalische Eigenschaften von Protonen, die sich in einem magnetischen Feld wie ein Kreisel bewegen, detektiert. Wassermoleküle besitzen zwei Wasserstoffprotonen - daher können, da der menschliche Körper seinerseits einen hohen Wassergehalt aufweist, insbesondere von weichem Gewebe wie dem Gehirn gute MRT-Signale erhalten werden. Die funktionelle bildgebende MRT (fMRT) wurde entwickelt, um spezifische Änderungen im MR-Signal in aktiven Gehirnregionen zu detektieren. In Folge neuronaler Aktivität im Gehirn erweitern sich arterielle Blutgefäße und Kapillaren und führen somit zu einem erhöhten Blutfluss. Dadurch fließt mehr oxygeniertes Blut von der Seite der Arteriolen zur Seite der Venolen und verändert dort das Verhältnis von oxygeniertem zu desoxygeniertem Blut. Konventionelle fMRT-Methoden detektieren neurovaskulär gekoppelte, hämodynamische Veränderungen, wie Schwankungen im zerebralen Blutvolumen (CBV), im zerebralen Blutfluss (CBF) und das Blutsauerstoffgehaltabhängige Signal (blood-oxygen-level-dependent BOLD signal) [1-3]. Es wurde und wird intensiv daran gearbeitet, das fMRT-Signal, insbesondere im Gehirn von Tieren, besser zu verstehen [4, 5]. Da die Voxelgröße der fMRT-Bilder in der Regel der Interpretation des fMRT-Signals zugrunde liegt, erlauben hohe Magnetfeldstärken durch bessere Auflösung in die größeren dreidimensionalen Datenelemente (Voxel) „hineinzusehen“ und den Beitrag einzelner vaskulärer Komponenten zum Signal zu entschlüsseln.
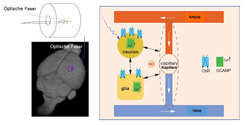
Zusätzlich zur Verwendung von Hochfeld-MRT wurde eine multi-modale fMRT-Plattform entwickelt, die sowohl für anästhesierte als auch wache Tiere verwendet werden kann (Abb. 1). Dabei werden optische Fasern in die zu untersuchenden Gehirnregionen eingeführt. Hier wurden zuvor mit gentechnischen Methoden Kalziumindikatoren (GCaMP6f) in Neuronen und Astrozyten (verzweigten Gliazellen) eingeführt und exprimiert. Gleichzeitig mit GCaMP6f kann auch ChannelRhodopsin-2 (ChR2) exprimiert werden. Über ChR2 lassen sich einzelne Gehirnregionen optogenetisch aktivieren. Diese optogenetische Aktivierung wird dazu verwendet, um über die Astrozyten eine Glio-Vaskuläre Kopplung (funktionelle Kopplung zwischen Gliazellen/Astrozyten und Blutgefäßen) hervorzurufen. Mit ihrem Potential, Zell-spezifische dynamische Signale zu detektieren, macht es diese multi-modale fMRT Plattform möglich, die Grundlagen der Neuro-Glio-Vaskulären Koppelung zu identifizieren, die dem fMRT-Signal zugrunde liegen.
Möglicherweise können die so erhaltenen Erkenntnisse über das fMRT-Signal auch auf andere Forschungsfragen übertragen werden, um fMRT-Methoden für bildgebende Verfahren des menschlichen Gehirns weiterzuentwickeln. Diese können insbesondere genutzt werden, um prognostische Biomarker für vaskuläre Demenz bei Patienten mit Mikroangiopathien oder Alzheimer-Demenz zu identifizieren.
Entwicklung der single-vessel fMRI-Methode im Hochmagnetfeld
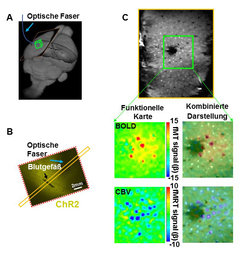
Das fMRT-Signal des Rattengehirns wurde mit einem 14T-Kernspintomographen untersucht. Basierend auf einer Pionierarbeit [6] wurde eine Rasterscanmethode [7] entwickelt. Zur Konstruktion der MR-Bilder wurde jede einzelne k-Raum-Linie nacheinander im Block-Design Paradigma aufgenommen und die Stimulations-Einheiten (an/aus) entsprechend der Anzahl an phasen-kodierenden Schritten wiederholt [8, 9]. Für die anatomischen Darstellungen individueller Arteriolen und Venolen, welche die mittleren kortikalen Schichten mit einem Durchmesser von 30 bis 70µm durchdringen, wurde eine multi-gradienten Echo-(MGE)-Sequenz verwendet. Arteriolen und Venolen konnten voneinander, wie auch vom umgebenden Gewebe, mittels T1-gewichteter multi-echo- Methodik unterschieden werden. Die Rasterscan-fMRT-Methode ermöglichte es, sowohl das Blutsauerstoffgehalt (BOLD-Signal) als auch die Schwankungen des zerebralen Blutvolumens (CBV-Signal) mit einer Flächenauflösung von 100x100µm und einer Aufnahmerate von 100ms aufzunehmen. Nach Stimulation der Vorderpfote bei Ratten zeigten sowohl BOLD als auch CBV maximale Signaländerungen an bestimmten, voneinander unterschiedlichen Regionen im somatosensorischen Kortex.
In Abbildung 2 ist zu sehen, dass der BOLD-Signalpeak in erster Linie mit den Venolen überlappte, der CBV-Signalpeak mit den Arteriolen. Diese Arbeit zeigt, dass der intrinsische vaskuläre Ursprung des fMRT Signals direkt sichtbar gemacht werden kann, wenn die räumliche Auflösung der fMRT Bilder soweit erhöht wird, bis einzelne Blutgefäße im Gehirn unterschieden werden können.

Aufzeichnung des optogenetisch induzierten fMRT Signals von einzelnen Blutgefäßen
ChR2 ist ein lichtempfindlicher Membran-Kationen-Kanal [10], der mit entsprechenden spezifischen Promotoren in verschiedenen Zelltypen des tierischen Gehirns exprimiert werden kann. Für die optogenetische Stimulation (480nm Laserlichtpuls, 5-20ms Pulsdauer, 10Hz, Lichtstärke 1-5mw) wurde eine optische Faser (Durchmesser: 200µm) in die Tasthaar-spezifische Region des Barrel-Kortex eingeführt, in der ChR2 exprimiert war. Ein zweidimensionaler, virtueller Schnitt eines fMRT-Scans wurde so ausgerichtet, dass er den aktivierten Kortex nahe der Faserspitze abdeckte, so dass das BOLD- und CBV-fMRT-Signal einzelner, individueller Arteriolen und Venolen aufgezeichnet werden konnte (Abb. 3). Ähnlich wie im Falle sensorischer Stimulation war das optogenetisch durch Licht hervorgerufene BOLD-fMRT-Signal vorrangig an den Venolen assoziierten Voxeln lokalisiert, das CBV-fMRT-Signal an Arteriolen-Voxeln. Die Arbeiten zeigen also, dass es möglich ist, durch optogenetische Stimulation fMRT-Signale von einzelnen Blutgefäßen zu erhalten.
Ausblick
Das dynamische vaskuläre Signal kann mit fMRT nicht-invasiv und mit hoher räumlich-zeitlicher Auflösung sowohl bei Tieren als auch bei Menschen detektiert werden. Darüber hinaus wurde eine Methode mit freier Präzession im Gleichgewichtszustand entwickelt, um das fMRT Signal von einzelnen Gefäßen aufzuzeichnen. Neben der Aufzeichnung bewusst hervorgerufener fMRT-Signale kann auch das fMRT-Signal einzelner Gefäße im Ruhezustand analysiert werden, um die dynamischen Verbindungen des vaskulären Netzwerks darzustellen. Diese Methodik besitzt ein einzigartiges Potential für die klinische Anwendung, um vaskuläre Demenzen wie Mikroangiopathien oder Alzheimer Demenz zu untersuchen. Zusätzlich kann das neuronale und astrozytäre Kalziumsignal gleichzeitig mit dem fMRT-Signal subkortikaler Regionen (wie dem Hippocampus) aufgenommen werden. Diese multi-modale fMRT-Plattform ist essentiell für die kombinierte Untersuchung von Gehirnfunktionen auf zellulärer Ebene, im Bereich neuronaler Netzwerke bis hin zum systemischen Level.


