Forschungsbericht 2015 - Max-Planck-Institut für biologische Kybernetik
Dem Langzeitgedächtnis auf der Spur
Wenn wir denken, arbeiten die Hirnregionen nicht getrennt voneinander, sondern über sogenannte Netzwerke. Kleine lokale Netzwerke bestehen aus Neuronengruppen und sind in Mikroschaltungen organisiert. Auf einer höheren Ebene sind ganze Hirnstrukturen durch Nervenfaserbündel miteinander verbunden und dadurch stark miteinander vernetzt.
Die Aktivität dieser zahlreichen Nervenzellen und der unterschiedlichen Hirnstrukturen muss koordiniert werden. Würden sie alle zur selben Zeit miteinander interagieren, entstünde Chaos und kein klarer Gedanke wäre mehr möglich. Diese Koordination ist die Grundvoraussetzung, damit ein Organismus sinnvoll auf die Umwelt reagieren kann, und wird durch das Zusammenspiel der hochkomplexen Gehirnnetzwerke umgesetzt.
Die Gehirnnetzwerke sind sehr dynamisch: Verbindungen zwischen einzelnen Zellen oder ganzen Hirnbereichen werden gestärkt oder wieder abgebaut. Durch diese anatomischen Voraussetzungen einerseits und die Selbstorganisation der Hirnstrukturen andererseits werden zusammenhängende Verhaltensweisen erzeugt, die es dem Organismus erst ermöglichen, in einer sich schnell verändernden Umgebung effizient zu handeln und zu lernen.
Netzwerkzustände im Gehirn
Durch die Selbstorganisation der miteinander kommunizierenden Hirnareale entstehen verschiedene sogenannte „Netzwerkzustände“. Darunter verstehen wir die neuronale Aktivität in verschiedenen Hirnstrukturen zu einem bestimmten Zeitpunkt sowie die Konsequenzen, die sie auf das Verhalten eines Organismus hat. Ein typisches Beispiel für Netzwerkzustände sind die Schlafphasen des Menschen. Anhand des neuronalen Aktivitätsmusters und der Augenbewegungen unterscheidet man zwischen Tiefschlaf- und REM-Schlafphasen (Rapid Eye Movement).
Grundsätzlich ist die Klassifikation von Hirnzuständen bisher noch nicht ganz eindeutig zu treffen und bedarf weiterer Forschung. Vieles weist jedoch darauf hin, dass das Repertoire der verschiedenen Zustände dazu genutzt wird, entsprechendes Verhalten zu erzeugen, das das Überleben sichert. So etwa die Suche nach Essbarem oder nach Schutz. Würde man die verschiedenen Netzwerkzustände kennen und verstehen, käme man dem Verständnis der informationsverarbeitenden Mechanismen des Gehirns einen Schritt näher.
Eine Nervenzelle arbeitet nicht gern allein
Um solche Netzwerkzustände erkennen zu können, muss die Anzahl der Netzwerk-Interaktionen auf unterschiedlichen räumlichen Ebenen gemessen werden. Daraus ergibt sich wiederum, dass unterschiedliche Signalarten gemessen werden müssen. Will man die Hirnaktivität unmittelbar messen, so ist die Ableitung von Aktionspotenzialen einiger weniger Neurone durch Elektroden innerhalb der Schädelhöhle (intrakraniell) das Mittel der Wahl.
Diese Aktionspotenziale oder neuronalen Spikes sind ein wichtiges Merkmal der Informationsverarbeitung auf zellulärem Level. Das Signal einer einzelnen Nervenzelle muss jedoch immer im Zusammenhang gesehen werden: Wenn sie nämlich gleichzeitig mit anderen Zellen aktiv ist, wird die Information vom Gehirn mitunter vollkommen anders interpretiert – die Nachricht bekommt auf Systemebene eine andere Bedeutung. So aktiviert ein Telefonklingeln beispielsweise eine Nervenzelle im auditorischen System – die Zelle selbst unterscheidet dabei aber nicht, ob dies nun im eigenen Haus oder im Haus eines Freundes stattfindet. Nur gemeinsam mit den Informationen anderer Gehirnbereiche kann die Aktivität der einzelnen Zelle in einen sinnvollen Zusammenhang gestellt und das adäquate Verhalten generiert werden: Soll die Hand zum Hörer greifen oder lieber nicht?
Bei der Messung der Gehirnaktivität im Versuchsaufbau ist die Ableitung der Aktivität einzelner Nervenzellen naturgemäß eingeschränkt – es lässt sich nur eine begrenzte Anzahl an Zellen gleichzeitig aufnehmen. Wie kann man aber die übrigen Nervenzellaktivitäten aufzeichnen, um den Zusammenhang auf Systemebene zu entziffern und zu verstehen, was das Signal des einzelnen Neurons bedeutet? Hier hilft die Messung des lokalen Feldpotenzials (LFP) weiter: Mikroelektroden nehmen Signale aus den Zellzwischenräumen auf, die in der Nähe der Elektrodenspitze ablaufen, und liefern damit aussagekräftige Informationen über die Aktivität von Neuronenpopulationen [1]. Dies ermöglicht eine Aussage über die Aktivität kleiner Netzwerke: Die elektrische Aktivität der einzelnen am Netzwerk beteiligten Zellen summiert sich zu messbaren Änderungen im elektrischen Feld.
Beziehungen zwischen in verschiedenen Strukturen erfassten LFPs können zudem zur Identifizierung von Interaktionen im Gesamtgehirn verwendet werden. Ausschließlich durch diese lokalen Feldpotenziale können Netzwerkzustände aber auch nicht in großem Maßstab erfasst werden. Zu diesem Zweck ermöglicht eine Messung der Abhängigkeit des Signals vom Sauerstoffgehalt des Bluts (Blood Oxygen Level Dependent - BOLD) mit Hilfe der funktionellen Magnetresonanztomographie die simultane Messung des lokalen Stoffwechsels im Gesamtgehirn bei einer räumlichen Auflösung von einigen Kubikmillimetern.
BOLD-Signale sind trotz allem mit Nachteilen behaftet – dies liegt an ihrer geringen zeitlichen Auflösung und ihrer abweichenden Beziehung zur elektrischen Hirnaktivität [2]. Um zu verstehen, welche Strukturen an bestimmten Hirnfunktionen beteiligt sind und vor allem wie, ist deshalb eine Kombination mehrerer Methoden notwendig. So kann die Netzwerkaktivität auf mehreren räumlichen Ebenen gleichzeitig beobachtet werden.
Die Welle des Hippocampus
Wenn wir uns an eine kürzlich gemachte Erfahrung erinnern, kommen uns Momentaufnahmen von dem, was wir gehört und gesehen haben, in den Sinn. Dadurch sind wir in der Lage, sehr konkrete Probleme zu lösen. So zum Beispiel, wenn wir versuchen, uns daran zu erinnern, wo wir das Portemonnaie hingelegt haben.
Neurowissenschaftler gehen davon aus, dass beim Kramen im Gedächtnis dieselben Neuronenverbindungen im Neokortex wieder aktiviert werden, die beim Blick auf das Portemonnaie aktiv waren. Während dieser sogenannten "Replays" sind dieselben Neuronenverbände aktiv wie beim Erlebnis selbst. Um sich zu erinnern, muss deshalb das Gehirn seinen Zustand ändern: Es muss von einem Zustand, in dem es von externen Stimuli angeregt wird, in einen Zustand übergehen, in dem es eine interne Netzwerkaktivität generieren kann, die eine Erinnerung aufruft.
Es wird vermutet, dass der Hippocampus – eine phylogenetisch alte Hirnstruktur innerhalb des Schläfenlappens jeder Gehirnhälfte – eine entscheidende Rolle im Abruf von Erlebnissen als auch in der Überführung dieser Erlebnisse ins Langzeitgedächtnis spielt [3, 4]. Um eine Gedächtnisspur zu reaktivieren, erzeugt der Hippocampus eine intensive Hirnwelle, die sich im LFP-Signal beobachten lässt, und die als Sharp-Wave-Ripple-Komplex (SWR) bezeichnet wird. Dabei ist ein sehr schneller Ripple, Hochfrequenzschwingung (über 100 Zyklen pro Sekunde) mit einer langsameren "scharfen" Potenzialänderung, der Sharp Wave, kombiniert (Abb. 1, links). Die Signale mehrerer einzelner Nervenzellen werden präzise synchronisiert und in Form dieses Ripples zu den Neuronen der Hirnrinde gesendet, um einen Replay hervorzurufen. Diese Zielneuronen können in mehreren spezialisierten Hirnarealen sitzen. Denn eine Gedächtnisspur enthält ja nicht nur eine Information, sondern meist visuelle, auditorische und emotionale Eindrücke.
Das Auftreten der SWR ist entscheidend für das Abspeichern einer Erinnerung – und macht es möglich, dass wir uns über Monate, Jahre oder sogar unser ganzes Leben lang an Ereignisse oder an Fakten erinnern. Während des Tiefschlafs tauchen die SWRs regelmäßig auf. Durch die synchronisierte Informationsweiterleitung zum Kortex werden synaptische Verbindungen ausgebaut und verstärkt. So entstehen feste Verbindungen zwischen den Neuronen eines definierten Netzwerks – und damit die Gedächtnisspur. Ist eine dieser so vernetzten Nervenzellen aktiv, aktiviert sie durch die starke Verbindung zu den anderen das gesamte Netzwerk. Wenn wir zum Beispiel das Gesicht eines Freundes sehen, fällt uns dadurch ein, was wir zusammen erlebt haben und was für eine Persönlichkeit er hat.
Was passiert im restlichen Gehirn, während eine Erinnerungsspur abgerufen wird?
Zur Untersuchung der Wiedergabe-Eigenschaften auf multiplen Ebenen wurde im MPI für biologische Kybernetik eine Versuchseinrichtung entwickelt, mit der sich elektrophysiologische und BOLD-Signale in nicht-menschlichen Primaten simultan erfassen lassen [5]. Damit wurde es erstmals möglich aufzuzeichnen, was im Gesamtgehirn abläuft, während eine spezifische Struktur elektrisch aktiv ist: der Hippocampus. Durch Mikroelektroden erfassen die Forscher die Hippocampus-Aktivität simultan zur BOLD-Aktivität vom Gesamtgehirn. Mit Hilfe automatisierter multivariater Analysetechniken identifizierten sie neuronale Ereignisse mit grundlegenden elektrophysiologischen Merkmalen von Sharp Wave Ripples. Durch die Messung von BOLD-Reaktionen in vielen Hirnstrukturen konnte man herausfinden, was während dieser Ereignisse im Gesamtgehirn passiert.
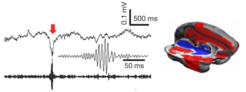
Es zeigte sich, dass während eines SWRs die Stoffwechselaktivität der Hirnrinde stärker wird, während die der Strukturen im Zwischenhirn, wie etwa des Thalamus, heruntergefahren wird (Abb. 1, rechts). Der Thalamus leitet normalerweise Eindrücke aus der Umwelt an die Hirnrinde weiter. Wird dies aber während der SWRs unterbunden, wäre freie Bahn für die Kommunikation zwischen dem Cortex und anderen Hirnregionen – wie dem Hippocampus. Das Gehirn ändert also offenbar seine Gesamtaktivität – den sogenannten Netzwerkzustand, um das Abrufen der Gedächtnisspur zu ermöglichen.
Koordination der Gehirnaktivität
Ursprünglich ging man davon aus, dass die erneute Aktivierung einer Gedächtnisspur nur für die Gedächtniskonsolidierung während des Schlafs genutzt wird. Inzwischen kommen Neurowissenschaftler immer mehr zu dem Schluss, dass die Replays von Gedächtnisspuren auch in vielen anderen Situationen auftreten. So etwa, wenn wir eine Aufgabe in einer neuen Umgebung erlernen.
Das Gehirn nutzt die Ripples vermutlich auch, um Erinnerungen abzurufen. Währenddessen kann sich das Gehirn in ganz unterschiedlichen Netzwerkzuständen befinden. Je nach Zustand ist es immer eine andere Hirnregion, die ihre Aktivität mit dem Hippocampus koordiniert.
Um diese Hypothese zu überprüfen, haben sich die Forscher am MPI für biologische Kybernetik die Aktivierungsmuster angeschaut, die gleichzeitig mit einem Ripple auftreten. Zudem haben sie Mustererkennungstechniken verwendet, um die Existenz sehr ausgeprägter Unterarten von Sharp Wave Ripples nachzuweisen, die jeweils eine spezifische Phasenbeziehung zu den Ripple-Hochfrequenzschwingungen aufweisen: Hochfrequenzschwingungen können der Sharp-Wave-Spitze vorangehen, ihr folgen oder mit ihr zusammenfallen und als Welle ohne deutliche Sharp-Wave-Signatur auftreten (Abb. 2, [6]). Entscheidend ist dabei, dass diese Unterarten mit verschiedenen Änderungen im Gesamtgehirn assoziiert waren, wie aus den Zeitverläufen von BOLD-Aufzeichnungen über mehrere Gehirnregionen während des Auftretens jedes Ereignisuntertyps zu ersehen war. Insbesondere waren Untertypen mit Differenzen in der BOLD-Reaktion in mehreren neuromodulatorischen Zentren verbunden, die für die Regulierung der Aktivität vieler Gehirnstrukturen verantwortlich sind, um beabsichtigte Ergebnisse wie Lernen, Wachzustand oder Belohnung zu erreichen (Abb. 2). Insgesamt deuten diese Ergebnisse darauf hin, dass das Gehirn die Aktivität kortikaler und subkortikaler Strukturen unterschiedlich orchestrieren kann, da Erinnerungen durch den Hippocampus aufgerufen werden – eine Eigenschaft, die zur Umsetzung verschiedener Funktionen verwendet werden kann.

Die Beschreibung der Gehirnaktivität auf multiplen Ebenen
Die obigen Ergebnisse zeigen, dass elektrophysiologische Ereignisse wie Sharp-Wave-Ripple-Komplexe auf Korrelate zurückzuführen sein können, die sich über ihre Messstelle hinaus ausdehnen, was zeigt, wie großangelegt die neuronale Informationsverarbeitung ist. Die gleichzeitige Aufzeichnung von mehrkanaligen elektrophysiologischen Ableitungen und BOLD-Signale für das Gesamtgehirn stellen beispiellose Möglichkeiten dar, neuronale Mechanismen auf der Ebene des gesamten Systems zu untersuchen.
Vor allem die subkortikalen Strukturen – wie z. B. der Thalamus – haben häufig einen wichtigen Einfluss auf die Aktivität der Hirnrinde. Analysiert man die Aktivität des gesamten Gehirns auf mehreren Ebenen, bekommt man einen besseren Eindruck davon, welche Rolle diese Interaktionen für die Funktionsweise des ganzen Gehirns spielen.
Ein wichtiger Aspekt für zukünftige Studien ist, dass man von einer Aktivität auf einer Ebene auf die einer anderen schließen kann. Dies würde es ermöglichen, die elektrische Aktivität in den Hirnregionen nur auf Basis der Magnetresonanztomographie-Aufnahmen abzuschätzen. Eine solche Methode könnte in der Anwendung kognitive und pathologische Zustände im menschlichen Gehirn nicht-invasiv nachvollziehen.

