Forschungsbericht 2015 - Max-Planck-Institut für chemische Ökologie
Zur Chemie der Blüten und ihrer ökologischen Rolle
DOI
10.17617/1.CBlüten gehören zu den faszinierendsten Erscheinungen in der belebten Natur und wir erfreuen uns an ihren Farben, ihren Formen und ihren Düften. Blüten sind Medium zur Entspannung, schmücken unsere Umgebung, gelten als willkommenes Geschenk für viele Anlässe und inspirieren zu künstlerischer Arbeit. Darüber hinaus erkennen wir in Blüten die Vorstufe zu den Früchten und Samenkörnern, die eine der Grundlagen unserer Landwirtschaft sind bzw. selbst einen wesentlichen Teil unserer Nahrung ausmachen.
Blüten wurden von der Evolution jedoch keineswegs mit der Absicht hervorgebracht, unser Leben zu sichern und unsere Umgebung zu dekorieren. Eigentlicher Zweck dieser reproduktiven Organe ist die Erhaltung und Verbreitung der jeweiligen Pflanzenart. Die in der Evolution optimierten artspezifischen Ausprägungen der Blütenform und Farbigkeit und die Chemie der verschiedenen Blütenbestandteile dienen der Kommunikation mit Bestäubern und dem primären Ziel der Übertragung von Pollen. Aber nicht nur die Pflanze profitiert von ihrem chemischen Potenzial, indem sie ihren Pollen vom Bestäuber verbreiten lässt bzw. bestäubt wird. Bestäuber, wie z. B. Insekten, Vögel und Fledermäuse, werden für Ihre Dienste mit Nektar, Pollen bzw. auch Blütenwachsen oder -ölen belohnt, die sie für ihre Ernährung nutzen. Die Erforschung der dieser Kommunikation zugrunde liegenden Chemie ist ein wichtiges Anliegen der chemischen Ökologie. Auf die chemische Zusammensetzung von Blütenfarbstoffen, Duftprofilen und Nektaren sowie ihre Rolle als Vermittler der Beziehungen zwischen Pflanzen und Bestäubern soll im Folgenden eingegangen werden.
Die verbreitetsten farbgebenden Naturstoffe in Blüten gehören zur Gruppe der Anthocyane [1]. Anthochlore, Betalaine, Carotinoide und die hier näher betrachteten Phenylphenalenone und Nudicauline sind weitere Gruppen von Blütenfarbstoffen. Neben der Eigenschaft, Bestäuber anzulocken, haben diese Verbindungen jedoch auch antioxidative Eigenschaften und schützen die Blüten vor UV-Strahlung und oxidativem Stress.
Phenylphenalenone in Blüten der Blutwurzler
Phenylphenalenone [2] sind eine Gruppe von pflanzlichen Naturstoffen aus Bananengewächsen (Musaceae) und sogenannten Blutwurzlern (Haemodoraceae). Sie kommen nicht nur als Abwehrstoffe in vegetativen Pflanzenteilen, sondern auch in Blüten vor und dienen dort wegen ihrer Farbigkeit der Anlockung von Bestäubern. Die Blütenfarben und -formen der Haemodoraceae weisen als Folge der Anpassung an die jeweiligen Bestäuber deutliche familienspezifische Unterschiede auf. Die Blüten der westaustralischen Gattung Anigozanthos besitzen eine Kronröhre, die sie als ornithophil ausweist, das heißt ihr Blütenstaub wird durch Vögel übertragen. Es ist bekannt, dass sie durch Honigfresser (Meliphagidae) bestäubt werden. Die Farbigkeit der Anigozanthos-Blüten geht jedoch nicht auf die Kronröhre, sondern auf zahlreiche verzweigte farbige Pflanzenhaare auf deren Oberfläche zurück (Abb. 1). Analysen zeigten, dass darin Phenylphenalenone als farbgebende Komponenten vorkommen. Daneben lassen sich farblose Flavonoide finden, während die als Blütenfarbstoffe sonst am weitesten verbreiteten Anthocyane nicht nachgewiesen wurden. Phenylphenalenone ersetzen demnach in Anigozanthos die Anthocyane als Blütenfarbstoffe.

Im Unterschied zu den Blüten der durch Vögel bestäubten Anigozanthos-Arten weisen die gelben Blüten der von Insekten bestäubten Wachendorfia-Arten aus der südafrikanischen Kapregion separate Kronblätter auf. Die Blütenfarbe von W. thyrsiflora stammt von Phenylphenalenonen, zum Beispiel Thyrsiflorin (Abb. 1). Ebenfalls nachgewiesene Flavonoide tragen nicht primär zur Farbigkeit bei. Auch die Blüten von Xiphidium caeruleum, einer südamerikanischen Haemodoraceae, enthalten Verbindungen des Phenylphenalenon-Typs, ebenfalls begleitet von Flavonoiden. Jedoch absorbieren weder die hier in oxidierter Form auftretenden Phenylphenalenone noch die Flavonoide im sichtbaren Spektralbereich, was die Blüten weiß aussehen lässt. Die beiden Gruppen von phenolischen Blütenstoffen dienen hier vermutlich dem UV-Schutz. Die Blütenstände von Xiphidium caeruleum tragen eine Vielzahl kleiner nektarloser Blüten. Das helle Erscheinungsbild und eine vermutliche Duftemission der Pflanze locken bestimmte Bienenarten an. Die Schallfrequenz des anfliegenden Insekts löst eine Vibrationsbestäubung aus, wobei dem Insekt anstelle von Nektar ein Teil der Pollen als Belohnung überlassen wird [3].
Die unterschiedliche Rolle der Phenylphenalenone in Blüten (und anderen Teilen der Pflanzen) – als Farbstoff, UV-Schutz und zur Abwehr von Krankheitserregern – wirft Fragen nach der evolutionären Ausprägung dieser Funktionen auf, die Gegenstand zukünftiger Untersuchungen sein werden.
Nudicauline und Indol in Blüten von Papaver nudicaule
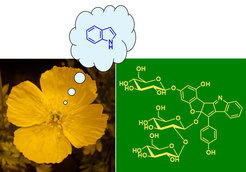
Die Nudicauline sind indolhaltige Naturstoffe mit ungewöhnlicher chemischer Struktur [4]. Im Unterschied zu fast allen anderen Indolalkaloiden leiten sie sich nicht von Terpenen, sondern von Flavonoiden ab. Die prächtige Farbe der Blütenblätter des gelben Islandmohns (Papaver nudicaule) ist auf die Nudicauline zurückzuführen (Abb. 2). Wie in den Haemodoraceae werden auch in P. nudicaule die Blütenfarbstoffe von farblosen Blütenstoffen begleitet. Im Islandmohn sind das vor allem Kaempferol-Derivate mit UV-protektiver Funktion. Eine weitere mögliche Rolle der Begleitstoffe wird in der Modifizierung der Lichtabsorption der Blütenfarbstoffe gesehen. Diese Hypothese lässt sich am Modell des Islandmohns besonders gut untersuchen, denn anders als bei den Phenylphenalenonen in den Blüten der Haemodoraceae ist hier die Zahl der Nudicaulin-Derivate begrenzt. Es eröffnet sich deshalb die Möglichkeit, die Wechselwirkung zwischen einzelnen chemischen Komponenten der Blüte sowie deren Einfluss auf die Lichtabsorption und die Interaktion mit den Bestäubern zu untersuchen.
Gemeinsam mit der Blütenfarbe spielt der Duft eine wichtige Rolle bei der Anlockung von Bestäubern. Im Unterschied zu den Blütenfarbstoffen bestehen Duftkomponenten aus leicht flüchtigen Verbindungen [5; 6] wie beispielsweise Terpenen, Carotinoid-Abbauprodukten, Phenolabkömmlingen, Aliphaten und Indolen. Es wäre effizient für die Pflanze, Farbstoffe und Duftkomponenten der Blüten über gemeinsame Biosynthesewege zu generieren. Es ergibt sich daher die Frage, wie die Kanalisierung von biosynthetischen Vorstufen in den sich verzweigenden Syntheseweg von Duft- und Farbkomponenten reguliert wird. Weitere Fragen betreffen den Synergismus zwischen der Gesamtheit der Farbstoffe einer Blüte und dem Duftbouquet bei der Anlockung von Bestäubern bzw. die Rolle der subtilen Mischungsverhältnisse innerhalb dieser beiden kommunikativen Naturstoffgruppen in der Koevolution mit den Bestäubern. Passend dazu wird in der Literatur das Wechselspiel zwischen der wirtsspezifischen Signatur aus Duft und Farbe auf der Seite der Pflanze und der Sinneswahrnehmung auf Seiten der Bestäuber diskutiert [7]. Die biosynthetischen Beziehungen zwischen Indol als einem Bestandteil des Blütendufts von Papaver nudicaule und den indolhaltigen Nudicaulin-Farbstoffen sind Gegenstand eines Projekts, in dem auch die Assoziation von Duft und Farbe in der Interaktion zwischen Pflanze und der Honigbiene als Bestäuber untersucht wird.
Nektar und Pollen sind mehr als ein Entgelt für die Bestäubung
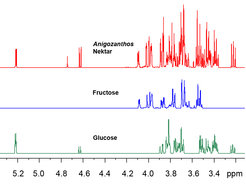
Blütenfarbstoffe und Duftkomponenten sind sogenannte Infochemikalien. Sie dienen der Kommunikation, sind nur in geringen Mengen vorhanden, haben aber selbst kaum Nährwert und eignen sich deshalb nicht als Entgelt für die Dienste der Bestäuber. Die meisten Nektare dagegen enthalten hauptsächlich Fruktose, Glukose (Abb. 3) und Saccharose sowie Aminosäuren und sind daher sehr nahrhaft. Pollen ist oft reich an Proteinen und/oder Lipiden und stellt deshalb in Kombination mit Nektar eine wichtige Nahrungs- und Energiequelle für Bestäuber dar.
Welche ökologische Rolle aber spielt die unterschiedliche chemische Zusammensetzung von Nektaren aus den Blüten verschiedener Pflanzen? Es ist bekannt, dass der Zuckergehalt von Nektar auf die unterschiedlichen Präferenzen der Bestäuber abgestimmt sein kann [8; 9]. Damit muss dem Nektar neben seiner Funktion als Gegenleistung für die Bestäubung auch eine kommunikative Funktion zugeschrieben werden. Noch ausgeprägter zeigt sich die Signalwirkung bei farbigen Nektaren mancher Pflanzen. Ein eindrucksvolles Beispiel ist dabei Leucosceptrum canum, auch „Bird’s Coca Cola Tree“ genannt. Luo et al. [10] haben im Blütennektar dieser Bäume ein neuartiges farbiges Prolin-Benzochinon-Konjugat entdeckt (Abb. 4). Die Struktur wurde mit spektroskopischen Methoden aufgeklärt und durch chemische Synthese bestätigt. Bioassays mit dem Japanbrillenvogel (Zosterops japonicus), einer ostasiatischen Art, die den „Bird’s Coca Cola Tree“ häufig besucht, ergaben eine klare Präferenz für den farbigen Nektar gegenüber einer farblosen Kontrolle.
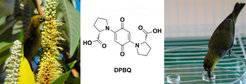
Abb. 4: Das Prolin-Chinon-Konjugat DPBQ verleiht dem Nektar des “Bird’s Coca Cola Tree”, Leucosceptrum canum (Labiatae), seine dunkle Farbe und lockt damit Vögel als Bestäuber an.
Zukünftige Entwicklungen
Die Frage nach der Herausbildung spezifischer chemischer Wechselwirkungen zwischen Pflanzenblüten und ihren Bestäubern ist ein aktueller Gegenstand der ökologischen Grundlagenforschung. Blütenfarbstoffe und Duftkomponenten zur visuellen bzw. olfaktorischen Erkennung durch die Bestäuber, einschließlich der Biosynthese und ihrer Regulation, sind dabei von besonderem Interesse. Vielversprechende Forschungsfelder sind auch Aspekte der Verwertbarkeit von Nektar und Pollenbestandteilen als Nahrung und die Beteiligung der Darmflora der Bestäuber als weitere Gruppe von Organismen im bezeichneten System. Zudem bekommt die Erforschung von chemischen Wechselwirkungen zwischen Pflanzenblüten und ihren Bestäubern in Zeiten zurückgehender Bienenbestände und einer deshalb drohenden Bestäubungskrise bei Nutzpflanzen zunehmende Bedeutung für die landwirtschaftliche Praxis. Für die instrumentelle chemische Analytik stellen derartigen Studien eine nicht zu unterschätzende Herausforderung dar.
Literaturhinweise
Annual Review in Plant Biology 57, 761-80 (2006)
Proceedings of the National Academy of Sciences of the USA 111, 105-110 (2014)
Journal of the Kansas Entomological Society 53, 685-699 (1980)
Organic Letters 15, 156-159 (2013)
The Botanical Review 72, 1-120 (2006)
Plant, Cell and Environment 37, 1936-1949 (2014)
PLoS ONE 10, e0128577
Biotropica 38, 3-15 (2006)
Experientia 48, 544-551 (1992)
Organic Letters 14, 4146-4149 (2012)



