Gene und ihre Metaboliten
Die Firma metanomics ermittelt Stoffwechselprofile und füttert damit riesige Datenbanken. Diese eröffnen der Pflanzenbiotechnologie, aber auch der Medizin und der pharmakologischen Forschung ganz neue Dimensionen.
Text: Catarina Pietschmann
Sie hatten eine ungewöhnliche Idee und den Weg gefunden, sie zu realisieren. Sie hatten den proof of concept erbracht – und es funktionierte. Und dann rechneten sie hoch: Wie lange würde es dauern, alle rund 30 000 Gene der Ackerschmalwand Arabidopsis thaliana einzeln abzuschalten und zu gucken, wie sich ihr Stoffwechsel dadurch verändert? Selbst bei kühnsten Schätzungen wären es Jahre gewesen. Was nun?

Lothar Willmitzer, Direktor am Max-Planck-Institut für molekulare Pflanzenphysiologie in Golm bei Potsdam, stand 1996 vor einer heiklen Frage: Ist es wirklich die Aufgabe einer Grundlagenforschungseinrichtung wie der Max-Planck-Gesellschaft, ein Hochdurchsatzverfahren zu entwickeln? Die Antwort war ein klares Nein. Das Parallelisieren von Prozessen ist Sache der Industrie, entschied er. Und so entstand die Idee, dafür eine Firma zu gründen.
Was ist so interessant am pflanzlichen Stoffwechsel? Wenn Mensch und Pflanze etwas gemeinsam haben, dann die Tatsache, dass beide über einen ziemlich komplizierten Metabolismus verfügen. Der menschliche ist gut erforscht. Vorwiegend deshalb, weil Veränderungen zu schweren Erkrankungen führen können – oder umgekehrt deren Folge sind, wie etwa Diabetes. Der menschliche Stoffwechsel verfügt außerdem nicht über die Vielzahl sekundärer Inhaltsstoffe wie Pflanzen.
Über die Stoffwechselvorgänge von Pflanzen ist dagegen längst nicht so viel bekannt. Erschwerend kommt hinzu, dass die Artenvielfalt riesig ist und sich die Metaboliten von Spezies zu Spezies teilweise erheblich unterscheiden: Einige produzieren hochwertige Öle, andere sind reich an Vitaminen und Aromastoffen, und wieder andere bilden vorrangig Zucker oder Stärke. Was auch gut ist, denn Pflanzen sind die Hauptgrundlage unserer Ernährung. Und es wäre ein Jammer, wenn Maiskolben, Thymian, Erdbeeren und Grapefruits gleich schmecken würden. Man könnte den Unterschied zwischen Knoblauch und Vanille vielleicht an der Form, nicht aber am Geruch erkennen.
Nicht auszudenken, was die Folgen wären: Die Küche Thailands wäre dieselbe wie in Italien. Restaurants gäbe es nicht. Wozu auch? Essen wäre kein Genuss, sondern schlicht Nahrungsaufnahme – ein lästiger, notwendiger Prozess. Statt Lebensmittelläden stünden vielleicht überall Depots, an denen wir regelmäßig anhalten und freudlos einen pürierten Einheitsbrei aufnehmen müssten. Vielleicht hätte die Evolution uns zu diesem Zweck sogar längst einen praktischen Saugrüssel spendiert. Glücklicherweise kam das anders: Eine Erdbeere ist eine Erdbeere. Und ihre Inhaltsstoffe sind eben völlig anders zusammengesetzt als die eines Maiskorns.
Metaboliten-Profiling liefert Muster aller Stoffwechselprodukte eines Gens
Durch Züchtung lassen sich Nährstoffgehalt, Aroma, Form, Farbe, Größe und Ertrag einer Pflanze beeinflussen. Doch das ist ein langwieriger Prozess. Zu langwierig, um bei einer stetig wachsenden Weltbevölkerung den Hunger auf der Erde in den Griff zu bekommen. Die Pflanzenbiotechnologie erlaubt es, sehr viel schneller Nutzpflanzensorten zu entwickeln, die ertrag- oder nährstoffreicher sind. Oder gar stressresistent, also beispielsweise auch auf kargen oder salzhaltigen Böden gedeihen, längere Trockenperioden überstehen, mit Kälte oder wenig Licht gut klarkommen.

Aber warum gleich das ganze Genom einer Pflanze dafür durchdeklinieren? Das Max-Planck-Institut für molekulare Pflanzenphysiologie war erst kurz zuvor, 1994, gegründet worden mit dem Ziel, die Biosynthesewege in Pflanzen zu untersuchen. Um zu verstehen, wie Bildung und Transport von Stoffwechselprodukten sowie deren Speicherung in Blatt, Blüte oder Frucht funktionieren. „Wir haben uns damals auf die Stärkebiosynthese bei der Kartoffel konzentriert und Gene identifiziert, die dafür wichtig sind“, erzählt Willmitzer. Die Forscher veränderten die Aktivität dieser Gene – in der Hoffnung, dass Pflanzen der folgenden Generation mehr und qualitativ hochwertigere Stärke produzieren. Aber sie erzeugten weniger und machten noch ganz andere Zicken. Doch warum?
Forschen an den Grenzen des Wissens – so die Devise der Max-Planck-Gesellschaft. Und genau hier war so eine Grenze. „Gene beeinflussen sich gegenseitig. Uns wurde klar, dass wir, um weiterzukommen, eine Pflanze erst mal komplett auf der metabolischen Ebene charakterisieren mussten.“ Die vollständige Sequenzierung des Genoms von Arabidopsis, jenem unscheinbaren Unkraut, das Biologen als Modellpflanze dient, stand kurz bevor. Und die spannendste Frage in der Wissenschaft lautete damals: Welches Gen hat welche Funktion? „Das ist toll, dachten wir uns. Da können wir nachsehen, wie sich der Stoffwechsel ändert, wenn wir jedes Gen einzeln ausschalten“, erinnert sich Willmitzer.
Bis dato war es üblich, alle biochemischen Ebenen komplett abzuarbeiten: Vom Gen über die DNA, die Boten-RNA, die Proteinbiosynthese bis hinunter zu den Stoffwechselprodukten. Doch Willmitzer schlug einen neuen Weg ein. Der war nicht nur kürzer, sondern brachte, wie sich herausstellen sollte, viel umfassendere Erkenntnisse. Sie stiegen oben ein – beim Gen – und sahen sich nur an, was am Ende herauskam. Den chaotischen Cocktail der Metaboliten: Zucker, Zuckeralkohole, Aminosäuren, Fettsäuren, Enzyme, Aroma- und Farbstoffe und vieles mehr.
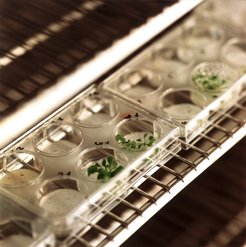
Die Prozedur klingt vergleichsweise simpel: Das entsprechende Gen wird mit molekularbiologischen Methoden ausgeschaltet. Dazu wird es vervielfältig und mithilfe eines Transporters, einem Bakterium, in die blühende Pflanze eingeschleust. Später wird ein kleines Blatt der Tochterpflanze, die nun das ausgeschaltete Gen trägt, fein zerkleinert, die Inhaltsstoffe extrahiert und schließlich mit einer Kombination aus Gaschromatographie und Massenspektrometrie (GC-MS) analysiert. Fertig. Das Ergebnis: Ein Diagramm mit über 350 Peaks, die für entsprechend viele verschiedene Substanzen stehen. Für jeden Peak gibt es zusätzlich noch ein Massenspektrum, aus dem sich unter anderem das Molekülgewicht ablesen lässt.
Ein Paradigmenwechsel in der Analytik stand an. Denn es ging ja nicht darum, all diese Substanzen zu isolieren, sondern um das Gesamtbild. Ein einzigartiges Metaboliten-Muster, das genau mit dem ausgeschalteten Gen korrespondiert. Nur 60 Prozent der Substanzen sind überhaupt erst bekannt. Aber das macht nichts. Will man wissen, ob ein bestimmtes Vitamin oder eine besondere Aminosäure dabei ist, lässt man einfach die entsprechende Referenzsubstanz mitlaufen. Metaboliten-Profiling nennt sich das Verfahren. Die neue Methode war entwickelt.
metanomics - eine Ausgründung der Max-Planck-Gesellschaft
Wie ging es weiter? Die Max-Planck-Gesellschafft gab grünes Licht für die Ausgründung. 1997 entwickelten Willmitzer und Trethewey einen Businessplan. „Wir rechneten anfangs mit einem Investitionsbedarf von 30 Millionen D-Mark für fünf Jahre.“ Dann begannen die Gespräche mit potenziellen Investoren. Willmitzer, der bereits früh das Potenzial der Methode erkannt hatte, war klar, dass es bis zur kommerziellen Nutzung noch ein sehr langer Weg sein würde.

Das erste Ziel der Firma musste die Entwicklung einer hocheffizienten Technologieplattform sein, das zweite die systematische Analyse des Arabidopsis-Genoms und der Aufbau der Metaboliten-Datenbank. Erst in Phase drei war an verkäufliche Produkte zu denken: Die Übertragung des Know-how auf Nutzpflanzen – sprich die Untersuchung von ausgewählten Genen in Mais, Reis, Soja, Raps oder Baumwolle – und das Schnüren von individuellen „Wissens-Paketen“ für Kunden aus der Industrie.
War es Mut zum Risiko oder Weitsicht? Vielleicht eine Kombination aus beidem: Die BASF sagte 50 Millionen D-Mark zu. Dann sprachen sie mit dem Bundesforschungsministerium. Auch hier sagte man ja und legte noch ein paar Millionen für die Technologieentwicklung drauf. Die Max-Planck-Gesellschaft prüfte die Verträge, ein Standort wurde gesucht und 1998 ging metanomics in Berlin-Charlottenburg an den Start: Vier Forscher vom Golmer Institut, einige wenige technische Assistenten (TA) und Arno Krotzky, der Geschäftsführer, den die BASF einbrachte.
Selbst mit einsteigen wollte die Max-Planck-Gesellschaft nicht. Willmitzer hätte sie zwar gern mit im Boot gehabt – sozusagen als Neutralisator – „Aber sie hat etwas anderes, ganz Wesentliches für uns getan: Bereits mit der Gründung des Instituts in Golm gab sie uns freie Hand, Neues zu erforschen, und stellte umfangreiche Mittel dafür bereit.“ An einem universitären Institut wären sie wohl nie so weit gekommen: Finanziell zu riskant. „In der Max-Planck-Gesellschaft hatten wir ein Umfeld, wo das keine Rolle spielte.“ Allein die Tatsache, dass sie überhaupt ausgründen durften, schätzt Willmitzer hoch ein. „Denn das geht nicht abends nebenbei. Anfangs ging schon ein Arbeitstag pro Woche dafür drauf.“
Heute beschäftigt metanomics 110 Mitarbeiter, ein Drittel von ihnen sind Wissenschaftler. Das Konzept ist aufgegangen. Der Aufbau der Technologieplattform ging zügig voran; Geräte musste man nicht neu entwickeln, aber Abläufe und jede Menge Software. Denn das meiste sollte automatisiert werden – von der Klonierung über die Extraktion, die Analyse bis zum Einfüttern der umfangreichen Dateien in die Datenbank. „Bereits nach einem Jahr schafften sie es, knapp hundert Gene pro Woche abzuarbeiten. Aber nicht hundert Leute – sondern ein Wissenschaftler zusammen mit vier technischen Assistenten!“, sagt Willmitzer, der metanomics noch eine Weile als Berater zur Seite stand, nicht ohne Stolz.

Inzwischen wurden 55000 Gene untersucht – sowohl durch Ausschalten als auch durch Einsetzen neuer Gene in Arabidopsis. „Letzteres ist sehr interessant, denn dadurch lassen sich neue nützliche Eigenschaften in die Pflanze einbringen. Zum Beispiel die Fähigkeit, neue Stoffwechselwege zu aktivieren oder zusätzliche Inhaltsstoffe zu produzieren“, erklärt Trethewey. Nun wendet man sich den Nutzpflanzen zu. Warum haben sie eigentlich nicht gleich Mais genommen? Aus praktischen Gründen: Arabidopsis ist klein und lässt sich gut im Gewächshaus züchten, und anders als bei Mais dauert es von der Keimung bis zur Samenbildung nur wenige Wochen. Leider sind die Gene unterschiedlicher Pflanzenarten nicht identisch. Die Herausforderung ist nun, anhand bisheriger Daten und dessen, was die Fachliteratur hergibt, die interessantesten Gene der Nutzpflanzen zu identifizieren und deren metabolische Profile zu erstellen.
Jeder Patient hat ein individuelles Metabolitenprofil
Mal abgesehen von der Effizienz: Was unterscheidet die Arbeit in der Firma von der in einem Institut oder in der Universität? Trethewey überlegt kurz. „Wenn wir ein unerwartetes Ergebnis bekommen, müssen wir es immer im Kontext mit unserem Ziel sehen: Ist das Risiko, das zu erreichen, nun gestiegen, oder ist es sinnvoll, einen Seitenpfad mit anderer Zielsetzung zu verfolgen? In der Industrie sind solche Prozesse sehr bewusst – in der Grundlagenforschung nicht immer.“

„Nicht alle Menschen reagieren auf ein Arzneimittel gleich. Für klinische Prüfungen wäre es hilfreich, vorher zu wissen, ob ein Proband zu den Respondern gehört oder nicht“, beschreibt Trethewey die Idee. Anhand eines Metaboliten-Musters im Blut oder Urin des Patienten lässt sich das testen. Das Prozedere ist das gleiche, nur in der Probenvorbereitung unterscheidet sich das rote Profiling vom grünen.
„Die Stoffwechselprodukte sind ja das, was am dichtesten am Phänotyp ist – groß oder klein, gesund oder krank, gelb, grün oder gesprenkelt“, erklärt Willmitzer. Gerade in der Medizin ist es wichtig, zwischen Zustand A und B unterscheiden zu können. „Und es hat sich gezeigt, dass man das mit metabolischen Profilen erstaunlich gut kann.“ Zusammen mit der Charité Berlin hat sein Max-Planck-Team Profile von 100 Nierenkrebspatienten erstellt – von Tumor- sowie gesundem Nierengewebe. „Es war nicht überraschend, dass es mit der Methode klar unterschieden werden kann“, erzählt er. Verblüffend aber war, dass zwei Substanzen aus Hunderten dafür genügten. Und dass das welche sind, die man vorher nie als Krebsmarker in Betracht gezogen hatte. Inzwischen gibt es viele andere Beispiele aus der Medizin.
Doch auch für die alltägliche Labormedizin könnte diese Methode einen großen Fortschritt bedeuten. „Bei Blut-Untersuchungen sieht der Arzt heute nur wenige Metaboliten wie Glukose und Cholesterin. Die Aussagekraft ist relativ gering. Wir aber sehen Tausende solcher Verbindungen! Regelmäßig gemessen, ließen sich krankhafte Veränderungen erkennen, lange bevor sie sich manifestiert haben.“ Ein regelmäßiger Metaboliten-Check beim Hausarzt? Warum nicht? Und wer gesund ist, erhielte Tipps, wie er sich noch besser fühlen könnte.
In der Wissenschaft ist die Methode längst etabliert. Weltweit nutzen Forscher sie, um tief in die Systembiologie unterschiedlicher Lebewesen einzusteigen. Am Max-Planck-Institut in Golm verfolgt man damit im Minutentakt, wie sich der Stoffwechsel einer Pflanze verändert. Vom Sonnenaufgang bis in die dunkle Nacht. Bei Hitze, Frost oder Nährstoffmangel.
Richard Tretheweys Vision für die Zukunft beinhaltet unter anderem auch neue Medikamente, die auf einem tieferen Verständnis des Stoffwechsels basieren. „Die Stoffwechselanalyse hat ein enormes Potenzial und war historisch unterschätzt. Wir erleben im Moment eine absolute Renaissance der medizinischen Wissenschaft. Trotzdem ist es nach wie vor eine Herausforderung, von der wissenschaftlichen Erkenntnis zu einem Produkt zu gelangen.“
Ob grünes oder rotes Profiling – der Weitblick von Wissenschaft und Industrie wird sich auszahlen. Denn wie sagte schon Victor Hugo: „Nichts ist mächtiger als eine Idee, deren Zeit gekommen ist.“
GLOSSAR
Gaschromatografie
Das Verfahren trennt Gemische von Stoffen: Abhängig von ihrem Siedepunkt und ihrer Polarität werden verschiedene Substanzen unterschiedlich lange an der speziellen Beschichtung einer bis zu 60 Meter langen Kapillare gebunden. Anschließend können die Stoffe massenspektrometrisch analysiert werden.
Massenspektrometrie
Die Methode gibt Auskunft über die Masse, genauer gesagt über das Verhältnis von Ladung und Masse in ionisierten Molekülen und ihren Bruchstücken. Abhängig von diesem Verhältnis werden verschiedene Teilchen in einem elektrischen Feld unterschiedlich beschleunigt und treffen getrennt auf einen Detektor.
Klonierung
Um eine DNA-Sequenz zu vervielfältigen, wird sie in Bakterien eingeschleust, vermehrt sich mit den Bakterien und wird anschließend isoliert.
Extraktion
Methode, mit der Stoffe aus Gemischen isoliert werden. Zu diesem Zweck werden Pflanzen mechanisch zerkleinert und die Stoffwechselprodukte mit Lösungsmitteln ausgewaschen.

















