Forschungsbericht 2014 - Max-Planck-Institut für Pflanzenzüchtungsforschung
Die Rolle posttranslationaler Protein-Modifikationen bei der Regulation des pflanzlichen Stoffwechsels
Proteom-Analysen bilden die Grundlage zum Verständnis sowohl des pflanzlichen Stoffwechsels als auch der Produktion von nutzbaren Inhaltsstoffen

Pflanzliche Stoffwechselprodukte sind ein essentieller Bestandteil des täglichen Lebens. Wir nutzen sie als Cellulose im Papier, als Öl im Salat, als Arzneimittel, in der Kosmetik, als Genussmittel, als Vitamin-Ressource, als Lieferant von Zuckern, Proteinen und Stärke, als Latex im Gummi, als Energieträger beim Heizen und für die Produktion von Strom und anderen Energieressourcen. Die mehr als 300.000 verschiedenen Pflanzenarten weltweit (http://www.theplantlist.org/) sind somit eine unverzichtbare Quelle tausender pflanzlicher Inhaltsstoffe, wobei viele davon bis heute noch gar nicht oder nur kaum beschrieben sind und die Regulation ihrer Biosynthese oft noch unbekannt ist.
Dank der enormen technischen Fortschritte in der DNA-Sequenzierung können heutzutage Genome von bisher unerforschten Spezies innerhalb weniger Wochen sequenziert werden. Die Genominformation bildet wiederum die Grundlage für die Identifizierung von Proteinen, die in den verschiedenen pflanzlichen Geweben synthetisiert werden. Die exakte Aminosäuresequenz dieser Proteine wird mittels neuester hochauflösender Massenspektrometer und durch den Vergleich mit der kodierenden Genomsequenz bestimmt. Diese Forschungsrichtung wird Proteomik genannt; die Bestimmung von Proteinsequenzen einer Zelle oder eines Gewebes wird als Proteomanalyse bezeichnet.
Die großen Fortschritte in der Genomik- und Proteomik-Technologie haben dazu geführt, dass auch kleine Unterschiede im Proteinaufbau, abhängig von der Spezies oder auch in derselben Spezies, unter verschiedenen Umwelteinflüssen erkannt werden können.
Flexible Anpassung von pflanzlichen Stoffwechselreaktionen als Folge von Umwelteinflüssen und posttranslationalen Modifikationen
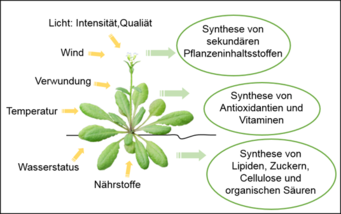
Pflanzen sind durch ihre ortsgebundene Lebensweise oft extremen Umweltbedingungen ausgesetzt. Sie müssen sich innerhalb kürzester Zeit an Trockenheit oder Überflutung, an Wind und Sonneneinstrahlung und an veränderte Nährstoffbedingungen im Boden anpassen, ebenso müssen sie sich gegen Schädlinge und Pflanzenkrankheiten wehren (Abb. 1). Nur flexible Anpassungsmöglichkeiten erlauben einer Pflanze, unter all diesen veränderlichen Umständen zu gedeihen. Diese Anpassungen schließen auch Stoffwechselreaktionen und die Synthese von unter den jeweiligen Bedingungen benötigten Stoffwechselprodukten mit ein.
So wird beispielsweise in Tabakpflanzen (Nicotiana sylvestris) die Produktion von Nikotin, das sie als Nervengift gegen Schadinsekten einsetzt, erst nach Verwundung induziert [1]. Auch Enzyme im Primärmetabolismus, das heißt solche Proteine, die für die Synthese essentieller Stoffwechselprodukte verantwortlich sind, können durch veränderte Umweltbedingungen in ihrer Aktivität reguliert werden. Das klassische Beispiel hierfür sind die enzymatischen Reaktionen innerhalb der Photosynthese, die die dafür notwendigen Zwischenprodukte für die Herstellung von Zuckern und Stärke liefern. Die photosynthetisch aktiven Enzyme sind weitestgehend nur im Licht aktiv, sobald die Pflanze die Lichtenergie zur Herstellung von energiereichen Stoffwechselintermediaten durch die Spaltung von Wassermolekülen nutzt [2].
Die Aktivität von Stoffwechselenzymen kann zum einen durch eine sich ändernde Proteinmenge im Gewebe gesteuert werden. Zum anderen können durch chemische Modifikation einzelner Aminosäurereste Enzymaktivitäten an- oder abgeschaltet werden. Solche posttranslationalen Modifikationen von Aminosäureresten sind zumeist reversibel und wiederum selbst durch regulatorische Enzyme gesteuert, die unter verschiedenen Umweltbedingungen gezielt aktiviert oder deaktiviert werden [3]. Posttranslationale Modfikationen erlauben im Allgemeinen eine schnelle Anpassung von Proteinfunktionen an einen veränderten Stoffwechselbedarf der Zelle. Insgesamt wurden schon mehr als 200 verschiedenste solcher Modifikationen an Proteinen beschrieben. Zu den bekanntesten gehören die Phosphorylierung, Ubiquitinylierung, Glykosylierung, oxidative Modifikationen und die Acetylierung.
Acetylierungen können an zwei unterschiedlichen Positionen innerhalb eines Proteins auftreten: an der Nα-Aminogruppe der N-terminalen Aminosäure eines Proteins und an den NƐ-Aminogruppen von Lysinresten. Die zweitgenannte Modifikation wurde in den späten 1960er-Jahren erstmals an Histon-Proteinen entdeckt [4] und steht im Fokus unserer Forschung.
Die Rolle der Lysin-Acetylierung bei Stoffwechselenzymen

Die Acetylierung von Lysinresten wird reversibel durch zwei entgegengesetzt arbeitende Enzyme reguliert, den Acetyltransferasen und den Deacetylasen (Abb. 2). In verschiedenen Organismen konnte gezeigt werden, dass die Lysin-Acetylierung wie ein Ein / Aus-Schalter für Enzymaktivitäten oder andere Protein-Funktionen wirkt und auch die Lokalisation von Proteinen innerhalb der Zelle verändern kann. Für Pflanzen ist die Bedeutung der Lysin-Acetylierung bisher nur sehr wenig erforscht. Das Ziel unserer Untersuchungen ist es, die Funktion der Lysin-Acetylierung an Proteinen des Energiestoffwechsels und der Signaltransduktion zu untersuchen.
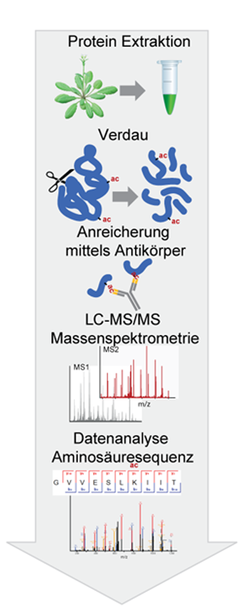
Für die Erforschung der Lysin-Acetylierung aller Proteine eines Organismus – dem sogenannten Acetylom – war die Entwicklung von Antikörpern zur spezifischen Anreicherung von Lysin-acetylierten Proteinen ein wichtiger Schritt. Die angereicherten Peptide können nachfolgend mithilfe hochauflösender Massenspektrometrie identifiziert und quantifiziert werden [5]. Im Jahr 2011 wurden dann auch die ersten Lysin-Acetylom-Studien mit der Modellpflanze Ackerschmalwand (Arabidopsis thaliana) publiziert. Hier konnte erstmals gezeigt werden, dass in Pflanzen nicht nur Histone, sondern auch plastidäre, also in Chloroplasten enthaltene, und mitochondriale Proteine Lysin-acetyliert werden [6, 7]. Besonders auffällig war, dass viele Enzyme des primären Stoffwechsels diese Modifikation tragen und dass die Acetylierung einen Einfluss auf die Enzymaktivität von Photosyntheseproteinen haben kann (Abb. 3). Dies war ein erster Hinweis darauf, dass Lysin-Acetylierung nicht nur bei der Genexpressions-Regulation eine entscheidende Rolle spielt, sondern dass diese Modifikation wahrscheinlich auch mit dem Energiestoffwechsel von pflanzlichen Zellen verknüpft ist.
Diese Ergebnisse deuten darauf hin, dass die Lysin-Acetylierung eine wichtige Rolle bei der Regulation von metabolischen Enzymen und Signalprozessen spielt. Weitere Proteine wurden identifiziert, die durch Lysin-Acetylierungen modifiziert werden können; sie sind für Signaltransduktion, Protein-Turnover, Transportprozesse sowie Entwicklung und Zellzyklusregulation verantwortlich. Vermutlich muss auch bei diesen entscheidenden zellulären Prozessen mit einer regulatorischen Funktion der Lysin-Acetylierung gerechnet werden (Abb. 4). Diese und weitere Proteom-Analysen in Pflanzen haben gezeigt, dass Lysin-Acetylierung eine bis dato eher unterschätze post-translationale Modifikation zu sein scheint [8, 9, 10].

Abb. 4: Vermutete regulatorische Funktionen der Lysin-Acetylierung in Pflanzen.
Auch bei der biotechnologischen Produktion von primären oder sekundären Naturstoffen in Pflanzen könnte die Steuerung von Stoffwechselwegen durch die gezielte Modulation von Lysin-Acetylierungen hilfreich sein, um den Stoffwechsel in eine bestimmte, ertragsfördernde Richtung zu lenken. Vor diesem Hintergrund ist die detaillierte Analyse der Funktion und Manipulierbarkeit von Lysin-Acetylierungen von Bedeutung und bietet ein großes Potenzial weiterer, intensiver Forschung.
Literaturhinweise
Planta 201, 397-404 (1997)
Annual Review of Plant Biology 56, 187-220 (2005)
Plant Physiology 155, 1779-1790 (2011)
Mitochondrion 19, 252–260 (2014)
Plant Physiology 164, 1401-1414 (2014)