Forschungsbericht 2013 - Max-Planck-Institut für medizinische Forschung
Stress bei Zebrafischen
Die Stressantwort ist Ausdruck einer komplexen, physiologischen Anpassungsreaktion eines Tieres auf Umweltreize, welche die Homöostase – den Gleichgewichtszustand des Körpers – gefährden. Während die Stressantwort für ein Tier kurzfristig überlebenswichtig ist, steht eine anhaltende Stressantwort bei Menschen im Zusammenhang mit einer Reihe von Störungen wie Adipositas, Schlaflosigkeit, Herzerkrankungen, Gedächtnisstörungen, Angst und Depressionen. Angesichts der enormen Kosten, die der Gesellschaft durch stressbedingte Beschwerden entstehen, geht es beim Verständnis der Wirkungsweise von Stress auf molekularer und zellulärer Ebene nicht nur um eine grundlegende biologische Frage, sondern auch um eine dringende medizinische und gesellschaftliche Notwendigkeit. Aufgrund der Komplexität des Stresssystems ist die Analyse der Mechanismen, die der Wirkungsweise von Stress zugrunde liegen, eine große Herausforderung. Die von Soojin Ryu geleitete Forschungsgruppe am Max-Planck-Institut für medizinische Forschung hat Zebrafischlarven als neues und einfacheres Modell für die Stressforschung etabliert.
Warum Zebrafische?
Der Zebrafisch (Danio rerio) ist ein kleiner Knochenfisch, der in jüngster Zeit in der neurobiologischen Forschung zunehmende Verbreitung gefunden hat [1]. Das Zebrafischsystem hat den Vorteil, dass es quasi ein kleineres Wirbeltier-Modell ist. Das bedeutet, dass sich im Zebrafisch viele wirbeltierspezifische Eigenschaften finden, die jedoch durch eine geringere Anzahl von Zellen abgebildet und gesteuert werden und damit einfacher zu untersuchen sind. Weiterhin sind Zebrafischlarven transparent und genetisch hervorragend zugänglich (Abb. 1). Dadurch kann eine zelltypspezifische Manipulation auf einfache Weise mit einer Untersuchung des Nervensystems kombiniert werden [2]. Ferner gleichen viele Aspekte des Stressantwortsystems von Zebrafischlarven denen in Säugetieren, so dass die bei Zebrafischen gewonnenen Informationen genutzt werden können, um den Stress bei Säugetieren besser zu verstehen.
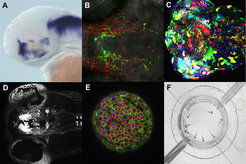
Abb. 1: Beispiele für verschiedene Färbemethoden in Zebrafischlarven
A. Genexpression kann auf einfache Weise mit In-situ-Hybridisierung in komplett gefärbten Zebrafischlarven analysiert werden.
B. Synapsen können in transgenen Larven durch synaptische Marker sichtbar gemacht werden, wie z. B. Synaptophysin verbunden mit grün fluoreszierendem Protein.
C. Eine transgene Zebrafischlarve, die Brainbow exprimiert – Brainbow ist eine Gentechnik, die es erlaubt, Kombinationen von unterschiedlich gefärbten fluoreszierenden Proteinen in verschiedenen Zellen zu erzeugen, um diese besser unterscheiden zu können.
D. Die Lage des Hypothalamus kann auf einfache Weise in transgenen Larven sichtbar gemacht werden, indem man hypothalamische Genpromotoren benutzt, um die Expression von grün fluoreszierendem Protein anzuschalten.
E. Verschiedene Zellkompartimente können leicht im ganzen Embryo dargestellt werden.
F. Die Abbildung zeigt eine spezielle Kammer zum Verfolgen des Verhaltens.
Stressbewältigung – das Verhalten von Zebrafischlarven unter Stress
Bei Gefahr oder Bedrohung muss ein Tier schnelle Verhaltensentscheidungen treffen, um zu überleben. Diese Entscheidungen dienen zum einen dazu, die Bedrohung zu vermeiden. Je nach den Umständen kann ein Tier beispielsweise entscheiden, vor der Bedrohung zu flüchten oder sich zu verstecken. Zum anderen werden unter Stress jene Verhaltensweisen gewählt, die nützlich sind, um mit dem Stressfaktor, dem sog. Stressor, zurechtzukommen. Dabei werden die Verhaltensweisen, die nicht sofort benötigt werden, unterdrückt. Wir alle haben schon die Erfahrung gemacht, unter Stress nicht mehr schlafen zu können oder appetitlos zu sein. Zeigen Zebrafischlarven solche Stressreaktionen?
Die Forschung am Max-Planck-Institut für medizinische Forschung zeigt erstmals, dass Zebrafischlarven ihre Verhaltensstrategien genauso wie Säugetiere anpassen, um mit Stress zurechtzukommen. In Gegenwart einer Bedrohung zeigen Zebrafischlarven schnelle Vermeidungsreaktionen. Zum Beispiel entfernen sie sich rasch von der Quelle einer konzentrierten Säure, von Salz oder auch von einer mechanischen Bewegung. Wenn sie solchen Stressoren ausgesetzt sind, verändert sich ihre Reaktivität auf verschiedene sensorische Reize in erheblicher Weise. Zum Beispiel reagieren gestresste Zebrafischlarven unterschiedlich auf verschiedene sensorische Reize wie Licht, mechanische Reize oder Temperatur. Diese Veränderung ist nicht spezifisch in Bezug auf die sensorischen Modalitäten, sondern dient eher der Verbesserung ihrer Fähigkeit, die Umgebung wahrzunehmen und mit ihr zu interagieren: eine extrem nützliche Eigenschaft in „Krisenzeiten“. Im Gegensatz dazu werden jene Verhaltensweisen unterdrückt, die nicht unmittelbar benötigt werden, um mit Stresssituationen umzugehen, wie zum Beispiel die Nahrungsaufnahme.
Die hier beschriebenen kurzfristigen Auswirkungen von Stress auf das Verhalten korrespondieren in bemerkenswerter Weise mit Beobachtungen von Stressantworten in anderen Tierarten und belegen, dass Zebrafischlarven ein vielversprechendes Modell zum Verständnis dieser Prozesse sind.
Den Schalter umlegen – optogenetische Steuerung von Verhalten unter Stress
Wie werden nun die kurzfristigen Auswirkungen von Stress auf das Verhalten vermittelt? Bei der Steuerung der Stressantwort sind hauptsächlich zwei Systeme beteiligt: die Hypothalamus-Hypophysen-Nebennieren-Achse (Hypothalamus-Pituitary-Adrenal-Achse HPA) und der Sympathikus, sprich das sympathische Nervensystem. Im Allgemeinen geht man davon aus, dass die schnelle fight-or-flight-Reaktion auf die Bedrohung durch den Sympathikus vermittelt wird, während die Hypothalamus-Hypophysen-Nebennieren-Achse verschiedene Aspekte der Stressantwort steuert [3]. Bei physiologischem, emotionalem oder psychischem Stress werden Stresshormone vom Hypothalamus ausgeschüttet, die auf den Hypophysenvorderlappen wirken und dort zur Ausschüttung eines anderen Stresshormons (Adrenocorticotropin) in den allgemeinen Blutkreislauf führen. Dies wiederum führt zur Ausschüttung von Glucocorticoiden aus der Nebennierenrinde. Glucocorticoide sind finale Effektoren der Stressachse mit zahlreichen Zielen sowohl im zentralen wie im peripheren Nervensystem [4]. In allen Wirbeltieren stellt die sogenannte HPA-Achse ein Schlüsselelement der Stressantwort dar, welches unzählige Stressreaktionen vermittelt.
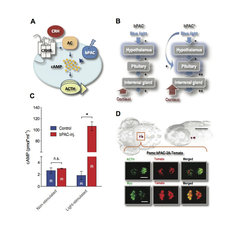
Abb. 2: Optogenetik: Ein neuartiger Ansatz zur Manipulation der Stressachse mit Licht. A. Erhöhte Cortisolausschüttung in transgenen Larven, die PAC exprimieren, nach Stimulation mit blauem Licht. B. Die Spezifität der transgenen Linie, demonstriert durch In-situ-Hybridisierung
Aufgrund der Vielfalt und Komplexität der Stressantwort ist es überaus wichtig, spezifische Auswirkungen von individuellen Stresshormonen zu entschlüsseln. Da Stressbedingungen jedoch alle drei Ebenen der HPA-Achse aktivieren, war es schwierig, die spezifische Auswirkung eines einzelnen Stresshormons zu erfassen. Hierfür wird eine Methode benötigt, mit der ein spezifisches Stresshormon in seinem endogenen Bereich selektiv untersucht werden kann. Durch die gezielte Genmodifikation von optogenetischen, lichtgesteuerten Proteinen für die spezifischen Komponenten der Stressachse gelang den Max-Planck-Forschern in Heidelberg eine temporär präzise und nicht-invasive Manipulation der Stressantwort. Die Optogenetik ist eine neue spannende Technik in den Neurowissenschaften, bei der optische und genetische Verfahren eingesetzt werden, um die Zellaktivitäten von lebenden Tieren zu steuern. Diese Technik wurde bislang in großem Umfang für die Steuerung zahlreicher physiologischer Prozesse verwendet, jedoch noch nicht bei der Stressreaktion.
Am Zebrafisch zeigt Ryus Forschungsgruppe erstmalig, dass eine optogenetische Steuerung der Stressreaktion möglich ist. In einem Fall exprimierten sie photoaktivierbare Adenylatzyklase in Hypophysenzellen, um mit Hilfe von blauem Licht die Ausschüttung von Adrenocorticotropin zu stimulieren, und erzielten anschließend die Erhöhung des Glucocorticoid-Werts (Abb. 2) [5]. Mit dieser Methode konnten sie verschiedene Stressreaktionen sowohl induzieren als auch modulieren und auf diese Weise zeigen, dass eine optogenetische Steuerung von Stressreaktionen möglich ist.
Stresssteuerung – Steuerung der neuronalen Schaltkreise durch ein Stresshormon

Abb. 3: Karte von Zelltypen in der neurosekretorischen präoptischen Region von Zebrafischen
Die genauen Grenzen und die Ausdehnung der neurosekretorischen präoptischen Region in Zebrafischlarven als homologe Region zum Nucleus paraventricularis der Säuger wurde auf Grund von angrenzenden molekularen Markern und beinhalteten Neuropeptid-Zelltypen identifiziert. Mit Hilfe von In-situ-Hybridisierung mit mehreren Farben und anschließender 3D-Segmentierung und -Registrierung wird hier eine erste Karte der Anordnung von neurosekretorischen Zelltypen in Zebrafischlarven gezeigt.
Eines der Schlüsselziele von Glucocorticoiden sind die neuronalen Schaltkreise, welche die Stressantwort steuern. Hierbei dient sogenanntes negatives Feedback durch Glucocorticoide nicht nur dazu, die fortgesetzte Stressreaktion zu begrenzen, sondern auch zu beeinflussen, wie diese Schaltkreise bei zukünftigen Stressbedingungen reagieren. Zwar liegen umfangreiche In-vitro-Daten vor, aber die In-vivo-Wirkung von Glucocorticoiden ist komplex und erfordert ein Modell, das die In-vivo-Dynamik des veränderlichen Glucocorticoid-Werts nachbildet. Soojin Ryu und ihr Team konnten zeigen, dass Glucocorticoide die neuronale Genexpression im Hypothalamus kurzfristig steuern und auch ihre langfristige Entwicklung in den wichtigsten stressrelevanten Regionen im Hypothalamus beeinflussen. Hierzu identifizierten sie zunächst den genauen Ort in den entsprechenden Regionen im Zebrafisch und zeigten, dass sich die molekularen und zellulären Signaturen in der jeweiligen Region im Zebrafisch und bei Nagetieren auffallend ähneln (Abb. 3) [6, 7]. Das deutet darauf hin, dass die in Zebrafischen gewonnenen Erkenntnisse über die Stressmechanismen eine hohe Relevanz für das Säugetiersystem haben werden. Anschließend untersuchten die Forscher die Auswirkung einer Manipulation des Glucocorticoid-Werts auf diverse Typen von Nervenzellen in dieser Region. In Zusammenarbeit mit Johann Bollmann, Forschungsgruppenleiter am Max-Planck-Institut für medizinische Forschung, werden darüber hinaus auch die funktionellen Veränderungen in spezifischen Zellpopulationen mit Hilfe von fluoreszenzmikroskopischen Messungen der Nervenzellaktivität untersucht. Diese unterschiedlichen experimentellen Ansätze zusammengenommen werden neue Erkenntnisse bringen, wie Stress die Funktionsweise neuronaler Schaltkreise und die Entwicklung im Hypothalamus beeinflusst.


