Forschungsbericht 2013 - Max-Planck-Institut für biologische Kybernetik
Magnetresonanztomografie bei ultrahohen Feldstärken
Abteilung Hochfeld-Magnetresonanz
Was ist Magnetresonanztomografie?
Die Magnetresonanztomografie (MRT) ist ein bildgebendes Verfahren, das es ermöglicht, dreidimensionale Bilder des menschlichen Körpers zu generieren, die zur medizinischen Diagnostik verwendet werden können. Neben dieser Anwendung gibt es noch eine Vielzahl von anderen Bereichen, wie beispielsweise die biologische und neurowissenschaftliche Grundlagenforschung, in denen die MRT zum Einsatz kommt. Ein wesentlicher Vorteil gegenüber anderen bildgebenden Verfahren, die Röntgenstrahlen oder Radioaktivität verwenden, besteht darin, dass nur nicht-ionisierende, statische und dynamische Magnetfelder benötigt werden. Durch ein starkes statisches Magnetfeld wird das magnetische Moment der Kerne bestimmter chemischer Elemente (beispielsweise des Wasserstoffs) entlang des Feldes ausgerichtet. Aufgrund von thermischen Bewegungen werden allerdings nicht alle Momente ausgerichtet und so ist die entstehende Magnetisierung der Probe abhängig von der Temperatur und vom statischen Feld. Mit elektromagnetischen Feldern im Radiofrequenzbereich kann die Magnetisierung der Probe manipuliert werden und über zusätzlich angelegte Magnetfeldgradienten können räumliche Informationen erlangt werden. Typische Frequenzen für die Radiofrequenzfelder liegen im Bereich der sog. Larmorfrequenz, mit der die Magnetisierung um das statische Feld oszilliert. Speziell entwickelte Radiofrequenzspulen werden dabei für die Detektion und Manipulation der Magnetisierung verwendet. Da sich die Larmorfrequenz für verschiedene Atome unterscheidet, müssen die Spulen auf das jeweilige Element und die Magnetfeldstärke angepasst werden. In den meisten Untersuchungen wird das Wasserstoffatom verwendet.
Warum Hochfeld-Magnetresonanztomografie?
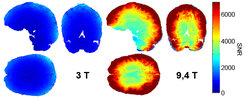
Das gemessene Signal der Detektionsspule ist proportional zu der Magnetisierung der Probe. Die Magnetisierung wiederum ist proportional zum statischen Magnetfeld, das heißt je stärker das Feld, desto größer das gemessene Signal. Aus diesem Grund besteht in der aktuellen Forschung der Trend, MRT-Experimente bei immer höheren Feldstärken zu betreiben. Ein stärkeres Signal bedeutet, dass sich Messzeiten verkürzen, beziehungsweise die Auflösung der Bilder sich erhöht. Zum Vergleich zwischen einem 3 Tesla (T) und einem 9,4 T-System ist in Abbildung 1 das Signal zu Rausch (SNR)-Verhältnis in einem menschlichen Gehirn gemessen worden. Außerdem werden manche Kontrastmechanismen bei hohen Feldern verstärkt. So skaliert der Kontrast zwischen Materialien, die unterschiedlich auf Magnetfelder reagieren, also eine unterschiedliche Suszeptibilität besitzen, mit der Stärke des statischen Feldes. Dieser Effekt wird insbesondere zur Darstellung von eisenhaltigem Gewebe, wie es im Gehirn oder der Hirnrinde vorkommt, ausgenutzt [1] oder in der funktionellen Bildgebung, in der die Aktivität des Gehirns über die lokale Änderung der Sauerstoffsättigung im Blut untersucht wird.
Am Max-Planck-Institut für biologische Kybernetik verwenden die Wissenschaftler bei ultrahohen Magnetfeldern für Untersuchungen am Menschen ein 3 T- sowie ein 9 T-System und für Kleintierstudien ein 14,1 T-MRT-System. Klinische Systeme, die für die Diagnostik verwendet werden, besitzen in der Regel Magnetfeldstärken von 1,5 oder 3 T.
Warum benötigt man neue Spulen?
Die Verwendung von ultrastarken Magnetfeldern führt jedoch zu neuen technologischen Herausforderungen. Diese werden hauptsächlich durch die höheren Frequenzen der elektromagnetischen Felder verursacht, die für die Manipulation und Detektion der Magnetisierung eingesetzt werden. Die hochfrequenten Magnetfelder besitzen eine geringere Eindringtiefe in die Probe. Zusätzlich treten wesentlich stärkere Überlagerungseffekte der elektromagnetischen Wellen auf, sogenannte Interferenzeffekte, die sich für kurze Wellenlängen verstärken. Im Gegensatz zu konventionellen MRT-Systemen (Feldstärke = 1,5 T), in denen die Wellenlänge innerhalb des Gewebes ca. 75 Zentimeter beträgt, verkürzt sich diese beispielsweise bei 9,4 T auf ca. 12 cm beziehungsweise bei 14,1 T auf ca. 7 cm. Interferenzeffekte treten auf, da die Ausdehnungen der untersuchten Proben, wie beispielsweise das menschliche Gehirn, meist in derselben Größenordnung liegen. Durch die Inhomogenitäten im Sendefeld entsteht eine ungleichmäßige Intensitätsverteilung in den Abbildungen sowie eine unerwünschte räumliche Variation des Kontrastes zwischen verschiedenen Gewebetypen. Intensitätssimulationen eines menschlichen Gehirns in der axialen Ebene zeigen deutlich, wie sich dieser Effekt für steigende Magnetfelder verstärkt (Abb. 2), [2].

Um diesen Effekten entgegenzuwirken, müssen neue Sendestrategien verwendet werden. Eine Möglichkeit besteht in der Verwendung von Mehrkanal-Sende- (Abb. 3a) und -Detektionsspulen (Abb. 3b), [3].

Die einzelnen Spulenelemente können dabei separat angesteuert werden, womit das Radiofrequenzfeld und somit die Magnetisierung im Gewebe mit mehreren Freiheitsgraden manipuliert werden kann. Mit dieser Methode kann zumindest lokal eine homogene Anregung erzeugt werden.
Für die Verwendung dieser Mehrkanalspulen wird jedoch nicht nur eine aufwändige Steuerelektronik benötigt, sondern es müssen auch neue Techniken zur Manipulation der Magnetisierung und zur Analyse der gemessenen Daten entwickelt werden. Des Weiteren geben die hochfrequenten elektromagnetischen Felder Energie in das Gewebe ab, wobei die räumliche Verteilung der Energie je nach Ansteuerung der Spulenelemente variiert. Dies kann zu einer lokalen Erwärmung des Gewebes führen, was insbesondere bei In-vivo- Messungen berücksichtigt werden muss.
Eine alternative Sende- und Detektionsmethode ist das traveling wave imaging [4]. Hier kommt eine einfache Antenne zur Erzeugung einer zirkular polarisierten Welle zum Einsatz. Diese verwendet die Röhre des Magnetresonanztomografen als Wellenleiter und breitet sich fast verlustfrei in der Röhre aus. Es wird dabei automatisch ein relativ homogenes Anregungsprofil über ein großes Volumen erzeugt. Außerdem müssen keine Spulen direkt an der Probe angebracht werden, was den Komfort für Testpersonen wesentlich erhöht. Der Nachteil ist allerdings, dass die detektierten Signale wesentlich schwächer sind als in der bereits vorgestellten Mehrkanalspule.
Die Mehrkanalspule in der Anwendung
Die oben beschriebene Mehrkanalspule ist bereits in ersten diagnostischen Studien verwendet worden. Durch die verschiedenen chemischen Bindungen der Wasserstoffatome in den Molekülen verschiebt sich die Larmorfrequenz um wenige ppm (parts per million). Durch diesen chemical shift, der mit dem statischen Magnetfeld skaliert, können verschiedene biologische Stoffwechselprodukte in einem Spektrum identifiziert werden. In ersten In-vivo-Studien am menschlichen Gehirn wurde die erhöhte spektrale Auflösung von verschiedenen Metaboliten bei ultrahohen Feldstärken ausgenutzt, um zwei Spektren aus In-vivo-Aufnahmen miteinander zu vergleichen [5]. Für das erste Spektrum wurde eine gesunde Region des menschlichen Gehirns ausgewählt (Abb. 4 a, rotes Rechteck), wohingegen für das zweite eine tumoröse Region verwendet wurde (Abb. 4 b, rotes Rechteck). Wie in den Abbildungen zu sehen ist, wurde dem Patienten bereits ein Teil des Tumors entfernt (homogener Bereich in den linken oberen Bildhälften).

MM: Makromoleküle; tCho: Choline; NAA: N-Acetyl-Aspartate; Ins: myo-Inositol; Glu: Glutamat; Gln: Glutamin.
Die Amplituden der Peaks unterscheiden sich dabei in den gesunden und in den tumorösen Regionen. Es ist ein deutlicher Anstieg der Makromoleküle (MM) und der Choline enthaltenden Komponenten (tCho) sowie eine Abnahme der N-Acetyl-Aspartate (NAA) in der tumorösen Region zu erkennen. Diese Metaboliten können auch in konventionellen Systemen identifiziert werden. Mit Hilfe von ihnen kann man den Tumorgrad klassifizieren. Zusätzlich können bei den Ultrahochfeld-Spektren weitere Metaboliten [z. B. myo-Inositol (Ins), Glutamat (Glu), Glutamin (Gln)] identifiziert werden. Dies hilft, den Gewebetyp eines Tumors zu diagnostizieren und schafft dadurch großes Potenzial für medizinische Anwendungen.
Ausblick
Trotz der in den letzten Jahren erzielten Fortschritte in der Ultrahochfeld-MRT besteht immer noch großer Raum für Verbesserungen, sowohl auf technologischer Seite als auch bei der Entwicklung von geeigneten bildgebenden Sequenzen und der Datenanalyse. Die verbesserte Auflösung spielt schon jetzt eine große Rolle für medizinische und neurowissenschaftliche Studien, in denen die Funktionsweise des menschlichen Gehirns durch ultrahochauflösende funktionelle Bildgebung im Submillimeter-Bereich erforscht wird. Aber auch in anderen Anwendungsgebieten, in denen durch das erhöhte Signal verbesserte quantitative Messungen möglich werden, ist das Potenzial der Ultrahochfeld-MRT noch nicht voll ausgeschöpft. Beispiele dafür sind die Detektion von anderen Atomkernen als dem Wasserstoffatom oder die Abbildung von Blutgefäßen [6].



