Forschungsbericht 2012 - Max-Planck-Institut für Kolloid- und Grenzflächenforschung
Wachstum von Knochengewebe unter natürlichen und künstlichen Bedingungen: Geometrie, Struktur und Materialeigenschaften
Biomaterialien
Wachstum von Knochen
In großen Tieren, wie z. B. Schafen oder Rindern, wächst der Knochen sehr schnell und es ist bekannt, dass dies in zwei Stufen abläuft. Dabei wird zunächst ein wenig geordnetes Knochengewebe (Geflechtsknochen) erzeugt und später wächst lamellarer Knochen an und ersetzt teilweise den Geflechtsknochen. Dieser lamellare Knochen mit parallelen Fasern hat vergleichsweise bessere mechanische Eigenschaften als der ungeordnete Knochen. Interessanterweise wurde eine ähnliche Abfolge bei der Ausbildung von Knochenstruktur auch während der Kallusbildung in einem Osteotomie-Modell (Durchtrennung des Knochens mit anschließender Heilung) an Schafen beobachtet [1, 2]. Diese Arbeit wurde in einem gemeinsamen Forschungsprojekt mit dem Julius Wolff Institut an der Charité in Berlin und dem Ludwig Boltzmann Institut für Osteologie in Wien durchgeführt.
Daraus ergibt sich die Hypothese, dass intramembranöse Knochenbildung einen Zwischenschritt erfordert, bei dem Knochen mit einem geringeren Grad an Orientierung als Substrat für knochenaufbauende Zellen – sogenannte Osteoblasten – dient. Darauf erfolgt dann die koordinierte Synthese von lamellarem Gewebe. Einige der Osteoblasten werden in der mineralisierenden Kollagenmatrix eingebettet und differenzieren dabei zu Osteozyten. Diese Zellen bilden mit ihren Zellfortsätzen ein Netzwerk das die gesamte Knochenmatrix durchzieht (Abb. 1, rechts). Die Zellen sitzen dabei in Hohlräumen, genannt Lakunen, und die Zellfortsätze befinden sich in kleinen Röhren (Canaliculi). Das Netzwerk kann auch als Fingerabdruck der Knochenbildung gesehen werden, da dadurch die Lage der Osteoblasten während der Einbettung und ihrer Differenzierung zu Osteozyten abzulesen ist.
Es gibt verschiedene Ansätze das Gewebewachstum zu untersuchen und zu beschreiben: (i) in vivo, das heißt durch Untersuchungen von natürlichem Knochengewebe, (ii) in vitro, also durch Beobachtung von künstlichem Gewebewachstum und (iii) in silico, durch Simulationen des Gewebewachstums.
In vivo: Visualisierung von Knochengewebe und Charakterisierung der Materialeigenschaften
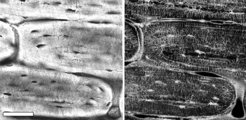
In Abbildung 1 wird das Osteozytennetzwerk von einem Schafsknochen (fibrolamellarer bzw. plexiformer Knochen) gezeigt. Die abwechselnden Schichten mit relativ kleinen Mengen an Geflechtsknochen und größeren Mengen von später gebildetem lamellarem Knochengewebe lassen sich sehr gut mittels konfokaler Laser-Scanning-Mikroskopie (CLSM) visualisieren [3]. Die linke Abbildung zeigt eine normale Lichtmikroskopieaufnahme und das rechte Bild eine CLSM-Aufnahme des Osteozytennetzwerks. Man sieht sehr gut, dass die Osteozytenlakunen und die Canaliculi in den mittleren Schichten ungeordnet sind und jeweils um diese Bereiche herum Schichten mit höherem Orientierungsgrad zu finden sind. Eine Visualisierung von Osteozytennetzwerken in sekundären Osteonen zeigt auch, wie der Umbau von Knochen durch Zellen abläuft: Osteoklasten resorbieren alten Knochen und hinterlassen dabei Hohlräume in Form von Zylindern, und Osteoblasten füllen diese dann wieder mit Schichten von Knochenmatrix.

Abb. 2: Plexiformer Schafsknochen: (A) visualisiert mit konfokaler Laser-Scanning-Mikroskopie (CLSM), (B) Mineralpartikeldicke (T-Paramter in nm), (C) Grad der Orientierung der Mineralpartikel (Rho-Parameter) und (D) Ausichtung der Mineralpartikel auf ein CLSM-Bild überlagert (Maßstabsleiste = 50 µm).
In biologischen Geweben, wie Knochen, beeinflussen sich die physikalischen Eigenschaften der extrazellulären Matrix sowie Zellfunktion und Zellaktivität gegenseitig. Osteozyten sind dafür bekannt den Knochenumbau zu orchestrieren. Jedoch ist die genaue Rolle der Osteozyten während der Mineralhomöostase sowie ihr potenzieller Einfluss auf die Materialqualität des Knochens noch nicht vollständig geklärt. Um die Wechselwirkung von Osteozyten mit der extrazellulären Matrix zu verstehen, ist es wichtig, die Netzwerk-Organisation im Hinblick auf die Eigenschaften des umgebenden Materials zu untersuchen [4]. Mit Hilfe von Synchrotron-Röntgenkleinwinkelstreuung ist es möglich, die Größe und Anordnung von Mineralpartikeln im Knochen zu bestimmen. Abbildung 2 zeigt die Größe (T-Parameter in nm) von Mineralpartikeln in Relation zum Osteozytennetzwerk sowie die Anordnung und Orientierung der Mineralpartikel (Rho-Parameter). Eine wichtige Erkenntnis dabei ist, dass diese Eigenschaften der Mineralpartikel von dem Abstand zum Zellnetzwerk abhängen. Mit dieser Kombination von Untersuchungsmethoden konnte gezeigt werden, dass die Osteozyten über ihr Netzwerk Zugang zu einem riesigen Mineralreservoir im Knochen haben. Die beobachtete Korrelation zwischen der Architektur der Osteozytennetzwerke und den Eigenschaften des Knochenmaterials unterstützt die Hypothese, dass Osteozyten in Wechselwirkungen mit ihrer mineralisierten Umgebung stehen und damit auch an der Mineralhomöostase mitwirken.
In vitro: Künstliches Gewebewachstum

Abb. 3: Vier lichtmikroskopische Aufnahmen von Knochengewebe als eine Funktion der Zeit (2, 7, 14 und 21 Tage). Das Gewebe bildete sich durch Osteoblasten in viereckigen Poren.
Parallel zu in vivo Untersuchungen der Knochenstruktur und des Knochenwachstums können auch in vitro Zellkulturexperimente durchgeführt werden, um zu untersuchen, wie sich knochenartige Gewebe unter kontrollierten Umgebungsbedingungen formen. In den letzten Jahren konnte gezeigt werden, dass zusätzlich zu biologischen Signalen, beispielsweise Wachstumsfaktoren, auch physikalische Parameter, wie lokale mechanische Eigenschaften und geometrische Form des Substrates, von einer Zelle wahrgenommen werden. Um herauszufinden, ob sich die Zellen im Gewebeverbund ähnlich verhalten, hat sich Rapid-Prototyping (3D-Druck) als sehr hilfreiche Methode herauskristallisiert. Diese Technologie erlaubt es, dreidimensionale Formen mit genau definierten Geometrien unterschiedlicher Größen herzustellen (siehe Abb. 3). Osteoblasten und auch Stammzellen (in Kollaboration mit Forschern vom Max Bergmann Zentrum für Biomaterialien in Dresden) werden danach auf die hergestellten Formen „ausgesät“ und für mehrere Wochen auf den Formen belassen, währenddessen sie Gewebe bilden. Mittels konventioneller Lichtmikroskopie sowie konfokaler Laser-Scanning-Mikroskopie wird das Gewebewachstum innerhalb der Poren als eine Funktion der jeweiligen Position und der Zeit beobachtet [5-7].
Die lichtmikroskopischen Aufnahmen in Abbildung 3 zeigen Gewebewachstum in quadratischen Poren in Abhängigkeit von der Zeit, wobei das Gewebe (hellbraun) bevorzugt in den Ecken der Poren und nicht auf geraden Oberflächen wächst. Erstaunlicherweise reagieren die Zellen immer noch auf die Porengeometrie, obwohl die Porengröße (1 mm) sehr viel größer ist als der Zelldurchmesser (50/1000 mm). Weitere Experimente haben gezeigt, dass sich die Wachstumsrate von Gewebe auch mit der lokalen Krümmung des Substrates ändert [6, 7]. Die Geometrie wirkt sich auch auf die Gewebestruktur aus, insbesondere auf die Orientierung der Zellen und deren produzierte extrazelluläre Matrix (Kollagenfibrillen).
In silico: Simulationen von Knochenwachstum
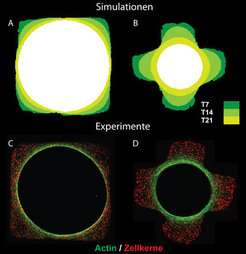
Abb. 4: Gewebewachstum – Simulation (oben) und Experiment (unten). Die Bilder A und C zeigen das Wachstum in viereckigen Poren, Bilder B und D in kreuzförmigen Poren. Die Bilder C und D wurden mit konfokaler Laser-Scanning-Mikroskopie aufgenommen.
Die Theorie, dass die lokale Wachstumsrate proportional mit der lokalen Krümmung zunimmt, kann anhand mathematischer Gleichungen beschrieben werden und wurde erfolgreich in ein Computermodell implementiert [6, 7]. Computermodelle erlauben es, Gewebewachstum in silico (rechnerisch) zu testen und mit in vitro Experimenten zu vergleichen. Abbildung 4 zeigt beispielhaft rechnerisch vorhergesagte Wachstumsprofile in quadratischen und kreuzförmigen Poren, wobei die Poren exakt gleich große verfügbare Oberflächen für Zellwachstum aufweisen. Der einzige Unterschied zwischen den Poren ist die durchschnittliche Krümmung der Oberflächen. Unser einfaches Modell des krümmungskontrollierten Wachstums sagt eine doppelt so hohe Wachstumsrate in den kreuzförmigen Poren im Vergleich zu den quadratischen Poren vorher. Diese Vorhersage konnte mittels des vorher beschriebenen Experiments (Abb. 4) getestet werden. Bemerkenswert ist, wie gut dieses einfache, rein geometrische Modell die Experimente beschreibt: Gewebewachstum kann durch alleinige Änderung der Geometrie beschleunigt werden.
Anhand dieses geometrischen Modells alleine ist es aber schwierig relevante biologische und physikalische Parameter, die das Verhalten der individuellen Zelle beschreiben, zu extrahieren. Um dieser Fragestellung näher zu kommen, wurde ein mechanisches Modell, das auf bestehenden Theorien der Kontinuumsmechanik basiert, entwickelt in Kollaboration mit Forschern von der Montanuniversität Leoben [8, 9]. Solche Modelle werden üblicherweise angewendet, um Phasenübergänge in Metalllegierungen zu beschreiben, sie sind aber auch geeignet, um die Thermodynamik wachsender Gewebe zu beschreiben. Dieser Ansatz stimmt mit dem einfacheren geometrischen Modell überein, erlaubt es aber auch, sowohl den Einfluss der Gewebe- und Scaffoldsteifigkeit als auch die Rolle der Biochemie auf das Wachstum mit zu berücksichtigen. Selbstverständlich wird auch dieses Modell sowohl mit in vitro als auch in vivo Experimenten überprüft.



