Forschungsbericht 2012 - Max-Planck-Institut für Infektionsbiologie
Immunität und Entwicklung – zwei Seiten einer Medaille?
Neutrophile: als erste vor Ort
Um den Körper vor Krankheitserregern zu schützen, hat das Immunsystem im Laufe der Evolution viele unterschiedliche Werkzeuge entwickelt. Eines davon sind Zellen, die eingedrungene Keime vertilgen. Von diesen sogenannten Fresszellen sind die Neutrophilen oder neutrophilen Granulozyten die ersten, die am Infektionsherd eintreffen. Neutrophile gehören zu den weißen Blutkörperchen und haben zwei auffallende Besonderheiten: Sie weisen Granula und einen in drei bis fünf Segmente unterteilten Zellkern auf (Abb. 1).
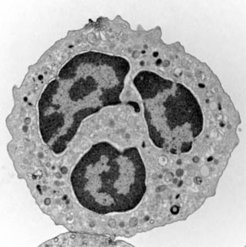
Abb. 1: Typischer Aufbau eines neutrophilen Granulozyten mitsamt Granula und – hier dreifach – segmentiertem Zellkern (transmissionselektronenmikroskopische Aufnahme).
Bei den Granula handelt es sich um Bläschen, die mit verschiedenen Enzymen befüllt sind. Die Bedeutung der Zellkernsegmentierung ist noch unklar. Neutrophile werden im Knochenmark aus Stammzellen gebildet, reifen dort aus und treten dann in die Blutbahn ein. Kommen sie innerhalb von sechs Stunden nicht in Kontakt mit einem Krankheitserreger, sterben sie ab. Trifft der neutrophile Granulozyt jedoch auf einen Erreger, umfließt er diesen und schließt ihn in einer Blase, dem Phagosom, ein. Das Phagosom verschmilzt mit den Granula, die dann ihre Enzyme in den so entstandenen Hohlraum ausschütten. Gleichzeitig werden an der Membran des Phagosoms Superoxid und Wasserstoffperoxid produziert. Für die eingeschlossene Mikrobe entsteht so ein äußerst unwirtliches Milieu, in dem sie schließlich abgetötet wird. Dieser als Phagozytose bezeichnete Prozess spielt in der Immunabwehr eine große Rolle und wurde erstmals im 19. Jahrhundert beschrieben.
Das Immunsystem wirft seine Netze aus
Erst vor wenigen Jahren entdeckten Wissenschaftler, dass Neutrophile zusätzlich noch über einen ganz anderen Abwehrmechanismus verfügen [1]: Bei Kontakt mit einem Krankheitserreger werfen sie ein Netz aus (Neutrophil Extracellular Trap, abgekürzt NETz; Abb. 2). Dieser Vorgang geht mit tiefgreifenden Veränderungen einher und die Neutrophile sterben dabei ([2], Abb. 3).
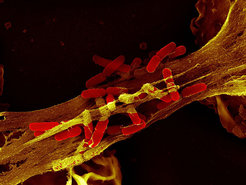
Abb. 2: Neutrophile Granulozyten (orange) haben ein NETz (gelb) ausgeworfen und darin Shigellen (rot), die Erreger der Bakterienruhr, gefangen (rasterelektronenmikroskopische Aufnahme).
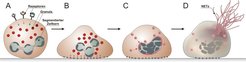
Abb. 3: Ein neutrophiler Granulozyt stirbt und macht NETze. (A) Über Rezeptoren auf der Zellmembran erkennt der Granulozyt Krankheitserreger. (B) Der Granulozyt verändert seine Form von rund zu flach, die Zellkernmembran beginnt, sich aufzulösen. (C) Der Zellkern verliert seine Segmentierung, die Chromosomen dekondensieren, die Granula lösen sich auf, die Bestandteile von Zell- und Zellkernplasma vermischen sich. (D) Der Granulozyt nimmt erneut eine runde Form an und zieht sich zusammen, bis die Zellmembran reißt, und der Zellinhalt wird als NETz nach außen geschleudert.
Bemerkenswert ist der molekulare Aufbau der NETze: Die Fasern werden von der DNA der Neutrophilen gebildet und sind wie mit Perlen über und über mit Enzymen aus den Granula und mit Histonen besetzt. Histone sind Proteine aus dem Zellkern: Sie sorgen dafür, dass die DNA in Chromosomen aufgewickelt vorliegt und, sobald genetische Information abgelesen werden muss, sind sie dafür zuständig, dass die entsprechenden DNA-Abschnitte abgewickelt werden. Bekannt ist, dass Histone aber auch zusätzlich dazu in der Lage sind, Bakterien effizient abzutöten.
Folgende Stoffe sind für die Produktion von NETzen unabdingbar: die Granula-Enzyme Myeloperoxidase (MPO) und Neutrophile Elastase (NE) sowie Verbindungen wie Superoxid und Wasserstoffperoxid, die als reaktive Sauerstoffspezies bezeichnet werden. NETze fangen die Krankheitserreger zunächst ein, und die Mikroben werden dabei durch Unterschiede in der elektrischen Ladung in den NETzen gehalten [3]. Die in den NETzen enthaltenen Enzyme und Histone töten dann die Erreger.
Wie können NETze wissenschaftlich analysiert werden?
Das Experimentieren mit Neutrophilen ist wegen ihrer kurzen Lebenszeit schwierig. Viele konventionelle molekularbiologische Methoden greifen daher nicht. Hinzu kommt, dass NETze sehr fragile Strukturen sind. Für die Erfassung von NETzen kann man sich aber ihrer einzigartigen Zusammensetzung bedienen: extrazellulärer DNA, die eng mit MPO, NE und Histonen verknüpft ist. Das Sichtbarmachen der NETze geschieht durch die Technik der Immunfluoreszenz: Die Probe wird dabei mit Antikörpern, die mit verschiedenen fluoreszierenden Farbstoffen gekoppelt sind und selektiv an einen der NETz-Bestandteile binden, versetzt [4]. Diese Technik ist sogar an lebenden Zellen durchführbar, der Prozess der NETz-Bildung kann so Schritt für Schritt verfolgt werden.
Um die Wirkung von NETzen zu messen, versetzt man eine Neutrophilenkultur mit Krankheitserregern und zählt die Anzahl der überlebenden Mikroorganismen. Auf diese Weise konnte nachgewiesen werden, dass NETze nicht nur Bakterien, sondern auch Viren, Parasiten und Pilze abtöten. Ein besonders eindrucksvoller Beleg für die Wichtigkeit von NETzen bei der Immunabwehr konnte anhand eines Patienten erbracht werden, der an septischer Granulomatose leidet [5]. Bei dieser Erbkrankheit können aufgrund eines Gendefekts keine radikalen Sauerstoffspezies gebildet werden. Bei dem Patienten hatte sich eine chronische Pilzinfektion in der Lunge entwickelt, die ihm das Atmen zunehmend erschwerte und sein Leben bedrohte. Im Labor konnte gezeigt werden, dass seine Neutrophilen nicht in der Lage waren, NETze zu bilden. Sie konnten deswegen auch keine Pilzmikroorganismen bekämpfen, da diese zu groß sind, um einfach „aufgefressen“ zu werden. NETze jedoch sind 10– bis 15-fach größer als der ursprüngliche neutrophile Granulozyt und ermöglichen so das Einfangen von Pilzgeflechten. Der Patient wurde einer Stammzelltherapie unterzogen, durch die der Gendefekt repariert werden konnte. Danach war sein Körper wieder fähig, Sauerstoffradikale und NETze zu bilden. Innerhalb weniger Wochen nach Therapieende konnte das Immunsystem des Patienten die Pilzerkrankung ausheilen.
Die dunkle Seite der NETze
NETze sind nicht nur wichtig für die Immunabwehr, es ist auch notwendig, dass sie nach der Bekämpfung von Erregern wieder abgebaut werden. Hierbei spielt das Enzym DNase 1 eine entscheidende Rolle [6]. Kann der Organismus aufgrund eines Gendefekts NETze nicht abbauen, kommt es zu lebensbedrohlichen Erkrankungen: Bei Mukoviszidose, einer der häufigsten und schwersten Erbkrankheiten bei Europäern, werden nach einer Entzündungsreaktion NETze nicht abgebaut und tragen so zur Entstehung eines zähflüssigen Schleimes bei, der die Lunge zunehmend zerstört. Auch Präeklampsie, die bei 5 – 7 % aller Schwangerschaften in Westeuropa auftritt, scheint mit einem unzureichenden Abbau von NETzen verknüpft zu sein. Eine Fehlentwicklung der äußeren Plazentaschicht ist vermutlich die Ursache dafür, dass diese von NETzen verklebt wird, was zu Bluthochdruck, Eiweiß im Urin, Nieren- und Leberversagen, Zerstörung der roten Blutkörperchen und mangelnder Sauerstoffversorgung des Fetus führt. Bei der Autoimmunerkrankung Lupus wiederum werden Antikörper gegen NETz-Bestandteile gebildet. Charakteristisch für diese Krankheit ist, dass sie in Schüben voranschreitet, die häufig von einer Infektion ausgelöst werden. Zwei Dinge scheinen bei Lupus eine Rolle zu spielen: überbordende NETz-Bildung und unzureichender NETz-Abbau. Dies führt zu einem Teufelskreis: NETze werden vermehrt gebildet, können nicht abgebaut werden, häufen sich daher an und führen schlimmstenfalls zu Nierenversagen [7].
Aus der evolutionären Perspektive betrachtet
NETze aus DNA und Histonen, die zur Immunabwehr ausgeworfen werden, sind im Organismenreich weit verbreitet: Beim Menschen werden sie nicht nur von Neutrophilen produziert, sondern auch von Mastzellen, einer weiteren Art von Immunzellen. Analoge Strukturen wurden bei anderen Säugetieren, Vögeln und Fischen beschrieben. Auch Insekten machen NETze, wobei statt DNA RNA eingesetzt wird, und selbst bei Pflanzen konnten NETze gefunden werden [7].
Das Interessante an NETzen ist, dass zwei ihrer Bestandteile eine Doppelfunktion haben: DNA und Histone. DNA – an sich für die Speicherung der genetischen Information zuständig - bildet hier die Grundstruktur eines Netzes, in dem Krankheitserreger eingefangen und abgetötet werden. Histone – im Zellkern dafür verantwortlich, dass die DNA in der richtigen Struktur vorliegt und die Entwicklung eines Organismus in geordneten Bahnen verläuft - nehmen hier ihren Zweitjob als Killer von Krankheitserregern auf. Histone sind allen Lebewesen – mit der Ausnahme von Bakterien – gemeinsam. DNA und Histone scheinen also schon frühzeitig in der Evolution zwei ganz verschiedene Aufgaben übernommen zu haben: einerseits die Organisation der genetischen Information, andererseits die Abwehr von Fremdorganismen. Entwicklung und Immunität sind bei NETzen also sehr eng miteinander verknüpft.
Das Immunsystem hat sich entwickelt, um die für den Organismus lebenswichtige Unterscheidung von „Selbst“ und „Fremd“ zu treffen. Zwischen Wirt und Erreger besteht dabei ein kontinuierliches Wechselspiel: Im Laufe der Evolution haben beide jeweils neue Strategien entwickelt, den anderen für die eigenen Zwecke auszutricksen. Auf neue Abwehrstrategien des Wirts reagiert der Erreger irgendwann mit neuen Infektionsmechanismen – und umgekehrt. Auch bei den NETzen ist die Evolution nicht zum Stillstand gekommen [8]: So können einige Pathogene ihre Oberflächenladung verändern oder sich in einer Kapsel verstecken, um nicht von NETzen gefangen zu werden. Verschiedene Bakterien sind sogar in der Lage, sich durch das Anbringen spezieller Enzyme an ihrer Oberfläche aus den NETzen zu befreien.
Den ersten Krankheitserregern gelingt es also bereits wieder, dem Immunsystem buchstäblich durch die Maschen zu schlüpfen.


