Forschungsbericht 2011 - Max-Planck-Institut für Biophysik
Optogenetik: Die molekularen Grundlagen und Anwendungen
Einleitung
Licht gesteuerte Ionenkanäle und Ionenpumpen aus der Klasse der mikrobiellen Rhodopsine wurden in den letzten Jahren sehr erfolgreich in der Neurobiologie und zunehmend auch in der Zellbiologie zur präzisen Lichtsteuerung von Zellen in Kultur und im lebenden Organismus eingesetzt. Das aus diesem experimentellen Ansatz entstandene Gebiet der Optogenetik hat in vielfältiger Sicht die Neurobiologie revolutioniert. Der Einsatz dieser Rhodopsine hat Möglichkeiten des Experimentierens eröffnet, was „jedes Jahr zu einer Rekordernte hochinteressanter Entdeckungen“ geführt hat [1]. In erster Linie wird der Wildtyp des Channelrhodopsin 2 (ChR2) auf Grund seiner einzigartigen, Licht gesteuerten Eigenschaften als depolarisierender Kationenkanal zur Aktivierung von Neuronen eingesetzt. Zusammen mit der Licht getriebenen Chloridpumpe Halorhodopsin (NphR) zur Hyperpolarisierung (Abschalten) bildet ChR2 eine ideale Kombination, um abhängig von der Wellenlänge Zellen ein- bzw. abzuschalten [2].
Molekulare und funktionelle Eigenschaften von Channelrhodopsin2
In der vergangenen Berichtsperiode sind, um die Anwendungsmöglichkeiten zu verbessern, einerseits die Arbeiten zum molekularen Verständnis und andererseits zur Entwicklung neuer Rhodopsinvarianten vorangetrieben worden. Zum ersten wurden Strukturuntersuchungen, spektroskopische und korrespondierende elektrophysiologische Untersuchungen durchgeführt. Maria Müller und Werner Kühlbrandt, Abteilung Strukturbiologie, und Christian Bamann, Abteilung Biophysikalische Chemie, konnten auf Grund von elektronenmikroskopischen Studien an 2D Kristallen erste Informationen über Struktur und Oligomerenzustand von ChR2 gewinnen [3]. ChR2 hat mit seinen sieben membranüberspannenden α-Helices eine homologe Anordnung wie die bekannte Struktur der Licht getriebenen Protonenpumpe Bakteriorhodopsin (bR). Interessanterweise liegt aber ChR2 als Dimer vor und nicht wie das bR als Trimer, wie sich dies aus Immunoblotexperimenten an Zellmembranen schon angedeutet hatte. Die funktionelle Bedeutung dieser für Rhodopsine einmaligen Anordnung in der Membran ist unbekannt. Die 3D Struktur, die kürzlich von einer japanischen Gruppe vorgestellt wurde, bestätigt diese Befunde.
Durch eine Punktmutation an Position D156 in Helix 4 wurden Hinweise zur Lokalisation für das Gating des Kanals gefunden. Genauere spektroskopische Untersuchungen haben ergeben, dass eine Wasserstoffbrückenbildung zu C128 in Helix 3 aufgehoben wird. Resultat dieser Mutation ist eine dramatische Verlängerung der Offenzeit vom Millisekundenbereich in den 10 Minutenbereich (Bamann und Zusammenarbeit mit Joachim Heberle, Berlin [4]).
Neue Experimentiermöglichkeiten
Es wurde einerseits, um die Experimentiermöglichkeiten im zellbiologischen und im neurobiologischen Bereich zu verbessern, nach Varianten mit höherer Lichtempfindlichkeit gesucht. Andererseits wurde eine Tandemkassette entwickelt, die eine stöchiometrische 1:1 Expression verschiedener Rhodopsine erlaubt.
Höhere Lichtempfindlichkeit ist für viele Anwendungen der Licht gesteuerten Kanäle wünschenswert. Dadurch könnten wegen der äußerst geringen Lichtdurchlässigkeit des Gewebes tiefere Bereiche der Hirnregion von Nagern bei Verhaltensstudien erreicht werden. Für den Einsatz in der Retina zur Wiederherstellung des Sehens, wo bereits der proof of principle von anderen Forschergruppen gezeigt werden konnte, ist ebenso eine deutliche Steigerung der Lichtempfindlichkeit für eine eventuelle biomedizinische Anwendung notwendig, da mit den derzeit zur Verfügung stehenden Rhodopsinen noch sehr hohe Lichtintensitäten eingesetzt werden müssen, die zu Zellschädigungen führen können. Da die Quantenausbeute von Rhodopsinen bei etwa 0,5 liegt, ist eine Steigerung der Lichtempfindlichkeit nur bis zum theoretischen Wert von 1,0 möglich, das heißt, eine wesentliche Steigerung der Lichtempfindlichkeit kann durch Änderung des chromophoren Systems Retinal - gebunden über eine Schiff`sche Base an ein Lysin in Helix 7 - nicht erreicht werden.
Eine Möglichkeit, die Lichtempfindlichkeit der Zellen zu verbessern, ist, durch Mutationen in den Positionen C128 und D156 die Lebensdauer der Kanäle und damit auch den Ladungstransport pro absorbiertem Photon zu steigern. Der Nachteil dieser Vorgehensweise besteht in der langsamen Kinetik, sodass diese ChR2 Varianten nur bei bestimmten neurobiologischen Fragestellungen, bei denen die Frequenz der durch Lichtpulse induzierten Aktionspotenziale eine untergeordnete Rolle spielt, sinnvoll eingesetzt werden können ([5], Zusammenarbeit mit B. Roska, Basel, und G. Nagel, Würzburg).
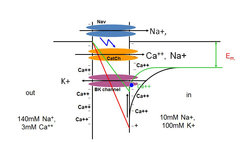
Um diese Schwierigkeiten zu umgehen, wurde von uns ein völlig neuer Ansatz gewählt. Durch eine Punktmutation im ChR2 wurde die Permeabilität des Kanals für Kalziumionen (Ca++) um das 6-fache erhöht. Wird der von uns als CatCh (Calcium transporting Channelrhodopsin) bezeichnete Kanal in eine Nervenzelle eingebracht, dann werden, so unsere Hypothese, nach Belichtung die in das Zellinnere geschleusten Ca++ Ionen die negative Oberflächenladungsdichte derart verringern, sodass das Oberflächenpotenzial an der Innenseite der Plasmamembran positiver und damit auch der Potenzialgradient über der Membran geringer wird (Abb. 1). Dadurch wird für die Aktivierung der spannungsabhängigen Natriumkanäle eine kleinere depolarisierende Spannung durch CatCh benötigt, wofür als Konsequenz auch weniger Licht notwendig ist. Durch die eingeschleusten Ca++ Ionen werden mit einer Verzögerung von wenigen Millisekunden Ca++ aktivierte Kaliumkanäle geöffnet, die durch den Kaliumausstrom die Zelle repolarisieren. Damit werden sehr schnelle und mit hoher Frequenz erscheinende Aktionspotentiale erzeugt [6]. Mit dieser Vorgehensweise konnten wir zeigen, dass CatCh an Neuronen die Lichtempfindlichkeit für die Aktivierung um einen Faktor von 70 im Vergleich zum Wildtyp ChR2 steigert. CatCh kann somit als lichtgesteuerte und membran gebundene Ca++ Quelle angesehen werden und wird inzwischen in vielen Labors sowohl für neuro- wie auch für zellbiologische Fragestellungen (Licht gesteuerte Ca++ Konzentrationssprünge) eingesetzt.
Die Koexpression von Channelrhodopsin (ChR2) und Halorhodopsin (NphR) erlaubt, mit verschiedenen Wellenlängen Nervenzellen einzuschalten beziehungsweise still zu legen. Da die Koexpression im Tierversuch im Gehirn von Zelle zu Zelle normalerweise stark variiert, ist es wünschenswert, in allen zu untersuchenden Zellen ein stabiles stöchiometrisches Verhältnis der verschiedenen Rhodopsine zu erhalten, damit das Belichtungsprogramm nicht immer neu angepasst werden muss. Ferner gelingt durch diese Vorgehensweise auch eine ortsspezifische Koexpression in den ausdifferenzierten Nervenzellen. In Fortsetzung früherer Arbeiten ist es uns gelungen, eine Fusionskassette herzustellen, die es erlaubt, antagonistische wie auch synergistische Rhodopsine in einem Tandemkomplex im 1:1 Verhältnis zusammenzuführen. In acht unterschiedlichen Kombinationen wurde das Tandem in verschiedenen Zellen (HEK293-, Neuroblastoma- und Hippokampuszellen) erfolgreich auf seine Funktion getestet, und die Erwartungen bezüglich der Stöchiometrie, Wellenlängen- und Lichtintensitätsabhängigkeit wurden voll erfüllt [7].
Ausblick
Da die Ionenselektivität und Lichtempfindlichkeit von ChR2 trotz der oben angeführten Verbesserungen noch nicht optimal sind, werden von uns derzeit Anstrengungen unternommen, Kanäle zu konstruieren, die zum Beispiel eine selektive Kaliumpermeabilität aufweisen und möglicherweise eine noch höhere Lichtempfindlichkeit an Neuronen induzieren. Derartige Konstrukte würden für biomedizinische Anwendungen wie zur Wiederherstellung des Sehens sehr wertvoll sein. Die Zusammenarbeit auf dem Gebiet der Photorezeptordegeneration mit Botond Roska, Basel, und Jose Sahel, Paris, wird fortgesetzt und hat durch die von Fovea/Aventis vorgenommene Lizensierung unserer Patente eine weitere Intensivierung erfahren.
Mit Hilfe der elektronenmikroskopischen Strukturuntersuchungen sollen lichtinduzierte Konformationsänderungen von ChR2 bestimmt werden, um den Offen- bzw. den Geschlossen-Zustand des Kanals zu beschreiben (Zusammenarbeit mit Maria Müller und Werner Kühlbrandt). Begleitende Infrarotuntersuchungen zur Kinetik der Konformationsänderungen in Zusammenarbeit mit Joachim Heberle, Berlin, werden fortgesetzt.
