Forschungsbericht 2009 - Max-Planck-Institute für experimentelle Medizin
Neuroligin-2 reguliert den Aufbau inhibitorischer Synapsen im Nervensystem
Molekulare Neurobiologie (Prof. Dr. Nils Brose)
MPI für experimentelle Medizin, Göttingen
Einführung
Als Synaptogenese bezeichnet man die Entstehung und Reifung funktioneller Synapsen zwischen den Nervenzellen. Dieser Prozess ist von grundlegender Bedeutung für die Entwicklung neuronaler Netzwerke im Gehirn. Synapsen sind asymmetrische Kontaktstellen zwischen Nervenzellen, die auf eine
zeitlich und räumlich exakte Signalübertragung ausgelegt sind. Die Signalübertragung an Synapsen wird durch die Ausschüttung von Neurotransmittern in den synaptischen Spalt initiiert, wobei mit Transmitter gefüllte kleine synaptische Vesikel mit einem spezialisierten Bereich der präsynaptischen Membran, der
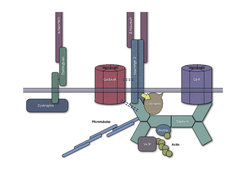
'Aktiven Zone', fusionieren. Freigesetzte Neurotransmitter werden dann von spezifischen Rezeptoren in der gegenüberliegenden postsynaptischen Membran gebunden und verändern den physiologischen Status der postsynaptischen Zelle, was zur Weiterleitung des synaptischen Signals führt. Die Neurotransmitter-Rezeptoren sind Teil eines komplexen Proteinnetzwerkes in der postsynaptischen Membran, das als ,Postsynaptic Density’ oder PSD bezeichnet wird (Abb. 1).

Es wird vermutet, dass Adhäsionsproteine maßgeblich an den molekularen Prozessen der Synapsenbildung beteiligt sind, insbesondere bei der Initiation des ersten Kontakts eines axonalen Wachstumskegels mit der Zielmembran und bei der anschließenden Reifung und Konsolidierung der Synapse durch Rekrutierung spezifischer Proteine in das jeweilige prä- und postsynaptische Kompartiment. Neuroligine sind postsynaptische Adhäsionsproteine, die durch direkte Interaktion mit präsynaptischen Adhäsionsproteinen der Neurexin-Familie prä- und postsynaptische Proteinnetzwerke miteinander verbinden. Die Neuroligin-Neurexin-Interaktion erfolgt durch die Bindung der jeweiligen extrazellulären Bereiche der beiden heterologen Adhäsionsproteine. Obwohl sich die molekularen Eigenschaften und Bestandteile erregender und hemmender Synapsen teilweise sehr unterscheiden, dient das von Neuroliginen und Neurexinen gebildete heterotypische Adhäsionssystem als Organisator beider Typen von Synapsen. Während die molekularen Grundlagen der Funktion von Neuroliginen in erregenden Synapsen weitgehend bekannt sind, blieben die der Neuroligin-Funktion an inhibitorischen Synapsen zu Grunde liegenden molekularen Mechanismen bislang allerdings unklar.
Die Struktur der Neuroligine
Das Maus-Genom enthält vier Neuroligin-Gene (Nlgn1 bis Nlgn4). Neuroligine sind Typ-1- Transmembranproteine mit einer großen extrazellulären Domäne, die Ähnlichkeiten zur Acetylcholinesterase aufweist, aber enzymatisch inaktiv ist. Es wird derzeit angenommen, dass verschiedene Spleißvarianten der extrazellulären Domäne von Neuroliginen spezifisch mit verschiedenen Neurexin-Spleißvarianten interagieren können. Neuroligine besitzen eine kurze intrazelluläre Domäne, die am C-terminalen Ende ein konserviertes Motiv für die Interaktion mit PDZ-Domänen enthaltenden Proteinen aufweist (Abb.2; [1]).

Gerüstproteine erregender Postsynapsen (MAGUKs, MAGIs, u.a. PSD-95) enthalten eine Reihe solcher PDZ-Domänen. Weil diese PDZ-Domänen-Proteine wiederum direkt mit postsynaptischen Rezeptoren, Ionenkanälen und anderen Signalproteinen interagieren, können Neuroligine indirekt Einfluss auf die Zusammensetzung des postsynaptischen Proteinnetzwerkes ausüben. An hemmenden Synapsen sind solche durch PDZ-Domänen vermittelten Interaktionen offenbar nicht von Bedeutung.
Neuroligin-Verteilung im Gehirn
In vivo ist Neuroligin-1 hauptsächlich in erregenden Synapsen zu finden, während Neuroligin-2 zumeist nur in inhibitorischen GABAergen und glycinergen Postsynapsen anzutreffen ist (Abb. 3; [2]).
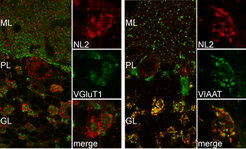
Die Verteilung der beiden übrigen Neuroligin-Isoformen ist bislang noch nicht im Gehirn studiert worden. In Primärkulturen von Neuronen, die aus dem Hippocampus gewonnen wurden, findet man Neuroligin-3 sowohl in erregenden als auch in hemmenden Postsynapsen. Weitere In-vitro-Untersuchungen lassen auf eine bevorzugte Lokalisierung von Neuroligin-4 in erregenden Synapsen schließen.
Funktionelle Konsequenzen der Neuroligin-Deletion in Mäusen
Während der Gehirnentwicklung kann man eine ansteigende Expression von allen Neuroliginen beobachten, wobei Neuroligin-4 während aller Entwicklungsphasen weniger stark exprimiert wird als die übrigen drei Isoformen. Die genetische Elimination der drei häufigeren Neuroligin-Isoformen in der Maus (Neuroligin-1, Neuroligin-2 und Neuroligin-3) hat dramatische Konsequenzen für die Gehirnfunktion. Entsprechende dreifach-deletionsmutante Mäuse (NL-TKOs) sterben schon wenige Stunden nach der Geburt aufgrund einer komplexen synaptischen Fehlfunktion [3] insbesondere im Atmungszentrum des Hirnstamms. Morphologische Untersuchungen zeigten, dass Synapsen in NL-TKOs zwar noch in normaler Anzahl angelegt werden, deren Reifung jedoch stark behindert ist. Weiterhin ist das ausbalancierte Zusammenspiel zwischen erregender und hemmender Neurotransmission, das für eine normale Funktionsfähigkeit des Gehirns notwendig ist, in NL-TKOs gestört [3]. Ursprünglich war vermutet worden, dass Neuroligine bereits bei der Initiation der Ausbildung von Synapsen eine wichtige Rolle spielen. Im Gegensatz dazu hat die Analyse der NL-TKOs gezeigt, dass Neuroligine nicht die Initialphase der Synaptogenese, sondern vielmehr die Reifung von Synapsen regulieren und so für eine funktionierende Signalübertragung zwischen Nervenzellen sorgen.
Im Gegensatz zu NL-TKOs leben und vermehren sich Neuroligin-2-defiziente Mäuse genauso wie ihre Wildtyp-Geschwister. Allerdings ergab eine detaillierte Analyse dieser Mutanten, dass Neuroligin-2 für die hemmende Neurotransmission von wesentlicher Bedeutung ist. Elektrophysiologische Untersuchungen am Stammhirn von Neuroligin-2-defizienten Mäusen zeigten klare und spezifische Defizite in GABAergen und glycinergen Synapsen, d.h. in allen inhibitorischen Synapsentypen. Begleitende biochemische Untersuchungen weisen darauf hin, dass diese Defizite auf eine erniedrigte Anzahl funktioneller GABA- und Glyzinrezeptoren an der Oberfläche hemmender Synapsen zurückzuführen ist [4].
Molekulare Grundlagen der Neuroligin-2-Funktion an hemmenden Postsynapsen
Jüngst haben wir im Rahmen einer Suche nach möglichen Interaktionspartnern des intrazellulären C-Terminus von Neuroligin-2 mit Gephyrin ein Protein identifiziert, das für die funktionelle Rolle von Neuroligin-2 an inhibitorischen Synapsen eine wesentliche Rolle spielen könnte [4]. Gephyrin ist das einzige bekannte Gerüstprotein hemmender Synapsen und dort für die Rekrutierung von GABA- und Glycinrezeptoren essentiell. Die Bedeutung der Interaktion von Neuroligin-2 mit Gephyrin wird durch die auf GABAerge und glycinerge Synapsen beschränkten phänotypischen Veränderungen in
Neuroligin-2-defizienten Mäusen untermauert. Überraschenderweise enthalten jedoch alle Neuroligin-Isoformen die Aminosäuresequenz, die für die Gephyrinbindung zuständig ist (Gephyrin BM, Abb. 2; [4]), sodass dieses Sequenzmotiv nicht allein für die Sortierung der verschiedenen Neuroligin-Isoformen in verschiedene Synapsen verantwortlich sein kann.
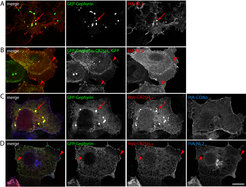
Neben Neuroligin-2 ist der GDP/GTP-Austauschfaktor Collybistin als wichtiger Interaktionspartner von Gephyrin bekannt. In Koexpressionsexperimenten in heterologen Zellen wurde gezeigt, dass Collybistin die Lokalisierung von Gephyrin entscheidend beeinflussen kann. Interessanterweise konnte diese Aktivität bislang aber nur für Collybistin ohne SH3-Domäne nachgewiesen werden, obwohl der überwiegende Teil von Collybistin im Gehirn diese SH3-Domäne aufweist. Es war also bislang unbekannt, welcher Faktor das native Collybistin aktivieren könnte. Wir fanden nun, dass die Anwesenheit von Neuroligin-2 zur Umverteilung von Gephyrin führt, wenn gleichzeitig Collybistin (mit oder ohne SH3-Domäne) anwesend ist (Abb.4; [4]).
Zusammenfassung
Die verschiedenen Neuroligin-Isoformen sind spezifisch in verschiedenen postsynaptischen Membranen lokalisiert. Während Neuroligin-1, Neuroligin-3 und Neuroligin-4 hauptsächlich in erregenden Postsynapsen angetroffen werden, wo sie mittels ihres PDZ-Domänen-Bindungsmotivs mit Gerüstproteinen dieses Synapsentyps interagieren und somit entscheidend für den funktionellen Aufbau dieser Synapsen sind, befindet sich Neuroligin-2 hauptsächlich in hemmenden Synapsen. Dort kann es direkt mit dem Gerüstprotein Gephyrin und dem GTP/GDP-Austauschfaktor Collybistin interagieren.
Gephyrin organisiert die Rekrutierung von GABA- und Glycinrezeptoren an hemmenden Synapsen. Die Befunde der Wissenschaftler am MPI für experimentelle Medizin zeigen, dass Neuroligin-2 einen entscheidenden Beitrag zur molekularen Organisation des Proteinnetzwerkes in hemmenden Postsynapsen leistet.
Die Wissenschaftler schlagen ein Modell vor (Abb. 5; [4]), demzufolge Neuroligine durch zwei Bindungsmotive differentiell mit Gerüstproteinen erregender und hemmender Synapsen interagieren können und so deren strukturelle und funktionelle Reifung steuern. Im Falle hemmender Synapsen koordiniert ein Komplex aus Neuroligin-2, Gephyrin und Collybistin die Rekrutierung von GABA- und Glycinrezeptoren an die postsynaptische Membran.




