Forschungsbericht 2009 - Max-Planck-Institut für Infektionsbiologie
Malaria: Warum wir einen Impfstoff brauchen
Parasitologie ()
MPI für Infektionsbiologie, Berlin
Malaria: Einzellige Blutparasiten aus den Tropen

Malaria bleibt auch in der heutigen Zeit die bedeutendste, durch Mücken übertragene Infektionskrankheit. 40% der Weltbevölkerung lebt in Malaria-Endemiegebieten, und hunderte Millionen Menschen erkranken jedes Jahr durch den nächtlichen Stich eines Weibchens der Anopheles-Mücke, das auf der Suche nach einer Blutkapillare mehrere Dutzend Parasiten des Genus Plasmodium (Erreger aus der Gruppe der Sporentierchen) unter die Haut injiziert (Abb. 1). Plasmodium falciparum ist der mit Abstand gefährlichste der fünf humanpathogenen Malaria-Erreger. Schätzungen gehen davon aus, dass jedes Jahr etwa 1 - 2 Millionen Kinder an Malaria sterben [1] - das bedeutet: jede Minute ein Kind. Besonders stark betroffen sind Kleinkinder in Subsahara-Afrika, wo die Malaria die soziale und wirtschaftliche Entwicklung des Landes grundlegend blockiert [2]. Wieso haben wir es bis ins 21. Jahrhundert immer noch nicht geschafft, diese weiter fortwährende humane Katastrophe wirkungsvoll einzudämmen?
Ein Erkranken an Malaria ist nur über kurze Zeiträume kontrollierbar
Die charakteristischen Krankheitssymptome, nämlich periodische Fieber- und Kälte-Schübe, werden durch die Plasmodien, einzellige eukaryontische Erreger im Blut, ausgelöst. Plasmodium hat die einzigartige Fähigkeit entwickelt, sich in den roten Blutzellen zu vermehren. Dies funktioniert für den Erreger problemlos, weil rote Blutzellen terminal differenzierte Zellen ohne Organellen sind und über keinerlei Antigenpräsentation verfügen. Gegen diese Stadien wirken unsere Medikamente, die wir bei einem Tropenaufenthalt als Dauerbehandlung einnehmen, um so wirkungsvoll einen Ausbruch der Krankheit zu verhindern. Das funktioniert verlässlich aber nur bei einem kurzen Besuch. Bei einem Daueraufenthalt muss dagegen auf andere Schutzmechanismen zurückgegriffen werden, nicht zuletzt wegen möglicher Nebenwirkungen bei einer Dauermedikation.
Seit der Aufklärung des Parasiten-Lebenszyklus durch Ronald Ross vor über hundert Jahren haben Vektorkontrollprogramme und persönlicher Mosquito-Schutz wesentlich zur Vertreibung der Malaria aus vielen Teilen der Welt, etwa im Mittelmeerraum und in einigen Teilen Süd-Ostasiens, beigetragen. Heute stehen uns eine Reihe von Interventions-Maßnahmen zur Verfügung: Insektizide, etwa Deltamethrin und Carbemate, die das Trichlor-bis-(chlorphenyl)-ethan, unter dem Kürzel DDT in Verruf geraten, wirkungsvoll ersetzen, gelten immer noch als die mit Abstand wirkungsvollste Waffe zur Bekämpfung der Malaria. Mit Pyrethroiden imprägnierte Bettnetze bieten einen zusätzlichen Expositionsschutz, der die Zahl der Neuinfektionen nachhaltig reduziert. Und ein klinischer Verdacht auf Malaria lässt sich diagnostisch absichern durch einen erfahrenen Mikroskopiker, der einen Giemsa-gefärbten Blutausstrich durchmustert.
Kombinationspräparate und Insektizide halten die Ausbreitung der Malaria in Schach
In der Therapie haben sich inzwischen Kombinationspräparate bewährt, die alle das Naturprodukt Artemisinin enthalten, das aus einer chinesischen Heilpflanze, einem Beifuß-Gewächs, gewonnen wird. Diese Artemisinin-basierten Kombinationstherapien sind heute ein zuverlässiger Partner in der Therapie der schweren Malaria. Leider wächst die Pflanze zu langsam für die dringend benötigten Mengen; Plantagenbesitzer haben ihre Auftragsbücher schon auf Jahre im Voraus gefüllt. Und die ersten Hinweise auf Therapieversagen, eventuell hervorgerufen durch resistente Parasiten-Stämme, sind äußerst Besorgnis erregende Alarmzeichen, die eine enorme Malariawelle ankündigen könnten [3]. Ein andere dramatische Entwicklung ist vor ein paar Jahren auch erstmals in der Malariatherapie aufgetreten: Wirkungslose oder unterdosierte Plagiate westlicher Medikamente werden im großen Maßstab in China, Indien und Nigeria hergestellt und sind für den Laien nicht unterscheidbar von den wirkungsvollen Originalsubstanzen. Die Dunkelziffer der betroffenen Opfer ist, ebenso wie bei Diabetes und anderen Krankheiten, nicht abschätzbar.
Bekommen wir denn die Malaria unter bestmöglichen Bedingungen in den Griff? Historische Beispiele sind Sri Lanka und Zanzibar – tropische Inseln, auf denen vor 50 Jahren innerhalb weniger Jahre die Zahl der Malariafälle auf ein paar hundert zurückgedrängt wurde. Während auf Sri Lanka die Eliminationsphase über viele Jahre stabil war, gelang dies auf Zanzibar nicht. Die Vektorbiologie und die Populationsdynamik der Anopheles Mücken und Plasmodium Parasiten sind in Afrika eine ganz andere und erschweren eine wirkungsvolle Eliminierung um ein Vielfaches. Diese Besorgnis zeichnet sich auch aktuell in Bioko, einer Insel im Golf von Kamerun, ab. Seit der Erdölförderung vor 6 Jahren hat das Land Äquatorial-Guinea einen ökonomischen Sprung nach oben erlebt und steht mittlerweile in der Weltbank-Statistik knapp hinter Deutschland. Auf der Insel, die gerade mal so lang wie Sylt ist und so viele Einwohner wie Heidelberg hat, wurde über Jahre durch die Marathon-Ölkompanie ein nahezu perfektes Malaria-Kontrollprogramm, das in dieser Form nirgendwo auf dem Kontinent finanzierbar gewesen wäre, durchgeführt - mit jedoch überraschend nur mäßigem Erfolg [4]. Dank der massiv und flächendeckend eingesetzten Insektizide und der begleitenden Maßnahmen, unter anderem freie Medikamenten- und Bettnetz-Versorgung, gingen die Malariafälle und die Zahl der infizierten Mücken zwar deutlich zurück, pendelten sich aber auch nach vier Jahren noch auf ein erstaunlich hohes Niveau ein. Noch immer erkrankt jeder Fünfte auf Bioko an Malaria. Die Experten sind ratlos, was sie noch verbessern können.
Schützende Immunmechanismen und Antigene der Malaria sind immer noch unbekannt
Obwohl auf den Inseln und an den Küsten Afrikas erste Erfolge der Interventionsprogramme gegen die Malaria sichtbar werden, setzt sich immer mehr die Erkenntnis durch, dass Malaria in Afrika vielleicht doch nur mit der zuverlässigsten Waffe der Mediziner in den Griff zu bekommen ist: mit einer Impfung. Und: Impfprogramme funktionieren in Afrika. Im Rahmen der so genannten expanded pediatric immunization (EPI) Programme werden Kinder auch in Afrika häufig flächendeckend gegen die Kinderkrankheiten, aber auch gegen Hepatitis B und Gelbfieber geimpft. Um es aber gleich vorweg zu nehmen: Es gibt keine sichere, andauernde und vor allem bezahlbare Impfung gegen Malaria. Sie ist noch nicht einmal in Sichtweite, sondern wahrscheinlich noch Jahrzehnte entfernt. Überhaupt ist eine Entwicklung von Vakzinen gegen irgendeinen echten Parasiten, wie eben beispielsweise Plasmodien, sehr schwer: es gibt zurzeit keinerlei Impfstoffe. Denn Parasiten beherrschen ihr Spiel nahezu perfekt, dem Immunsystem immer wieder zu entwischen. Sie haben vielfältige Mechanismen entwickelt, beispielsweise Antigenvariation und alternative Formen im Lebenszyklus, um sich einer schützenden Immunantwort des Wirts zu entziehen und können so oft viele Jahre in ihm wachsen und sich vermehren. Unsere bekannten Impfstoffe, beispielsweise gegen Viruserkrankungen, sind der Natur abgeschaut und schützen vor akuten Infektionen, die, wenn sie einmal überstanden sind, einen dauerhaften Schutz gegen Re-Infektionen auslösen. In Malariagebieten hingegen baut der Mensch erst über viele Jahre hinweg einen partiellen und nur kurzlebigen Abwehrschirm auf, der sich nicht gegen die Parasiten richtet, sondern nur vor dem Krankheitsverlauf (der Pathologie des Parasiten) schützt. Um dies zu erreichen, muss ein Kind aber viele Dutzend Neuinfektionen durchmachen. Bislang sind bedauerlicherweise schützende Immunmechanismen und vor allem Antigene der Malaria nahezu unbekannt. Selbst wenn schützende Antigene eines Tages entschlüsselt würden, würde eine Immunisierung viel zu viele Injektionen erfordern, bis ein Immunschutz gewährleistet ist. Deswegen müssen die Malariaforscher völlig neue Wege gehen, mit dem Anspruch, die Natur noch zu überbieten.
Erster Lichtblick: Kombipräparat mit Hepatitis B Impfstoff und neue gentechnische Ansätze
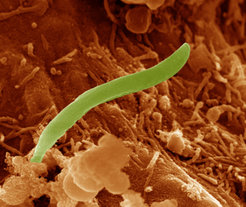
Am weitesten fortgeschritten ist ein rekombinanter Impfstoff, der von der Firma GlaxoSmithKline Biologicals hergestellt wird und der auf dem pädiatrischen Hepatitis B Impfstoff basiert. Die Idee ist faszinierend: Die erfolgreiche und sichere Impfung gegen das Virus kann nämlich genutzt werden, um zusätzlich noch einen Teilschutz gegen Malaria aufzubauen. Dazu wird ein Teil des Hauptoberflächenproteins von Sporozoiten (Abb. 2), also demjenigen Parasitenstadium, das durch Anopheles-Mücken auf den Menschen übertragen wird, an das HBV S-Antigen fusioniert. Als dieses neuartige Vakzin, genannt RTS,S/ AS02A, zusammen mit einem neuen, sehr starken Adjuvanz in Testreihen geimpft wurde, konnten erstmals Erfolge verzeichnet werden [5]. Zwar konnten Neuinfektionen nur für ein paar Monate verzögert werden, dafür wiederum schien bei einigen Kindern die Malaria milder zu verlaufen. Dieser überraschende Befund muss jetzt in „Phase 3“ Studien in vielen afrikanischen Ländern statistisch gesichert werden und stellt einen ersten Teilerfolg in der Impfstoffentwicklung gegen Malaria dar. Eine schützende Immunität, wie wir sie von Vakzinen gegen Viruserkrankungen kennen, wird aber auch hier nicht aufgebaut. Diese kann sehr wahrscheinlich sowieso nicht gegen einzelne Proteine der Plasmodien, sondern nur gewissermaßen gegen den kompletten Parasiten erzeugt werden.
Mithilfe präziser Gendeletionen konnte in einem Maus-Malaria-Versuchsmodell ein sicherer, lang-anhaltender und steriler Schutz gegen Neuinfektionen erzeugt werden [6]. Dazu wurden zunächst stadienspezifisch exprimierte Gene im Sporozoitenstadium identifiziert, die eine Rolle in der klinisch unauffälligen Leberphase spielen. Es wurde gefunden, dass eines der gefundenen Gene, UIS3, essentiell für die Infektion der Blutzellen unmittelbar nach der Leberphase ist. Wir konnten zeigen, dass UIS3-defiziente Sporozoiten zwar noch Leberzellen erfolgreich infizieren können, aber nicht mehr zu einem Übergang auf die Blutzellen in der Lage sind – mit der Folge, dass die Krankheit nicht ausbricht! Mithilfe dieser attenuierten, also stark abgeschwächten Sporozoit-Mutanten konnte nachfolgend eine Immunisierung in Maus-Malaria-Experimenten hervorgerufen werden.
Gentechnisch hergestellte, attenuierte Pathogene ermöglichten somit zum ersten Mal neue Perspektiven der Immunisierung gegen komplexe Krankheiten. In vergleichbaren Modellsystemen können verschiedene solcher „genetisch arretierter Parasiten“ verglichen werden, um so das Repertoire schützender Antigene einzugrenzen. Zusätzlich müssen noch weitere, biotechnologische Hürden genommen werden, wie etwa die axenische Kultivierung von Sporozoiten und deren schonende Konservierung.
Niemand kann aber vorhersagen, welche Strategie zum Erfolg führen wird und wie ein pädiatrischer Malariaimpfstoff aussehen wird. In der Zwischenzeit, und damit noch auf viele Jahrzehnte, sind wir auf die Entwicklung neuer Medikamente für die erkrankten Menschen und Insektizide gegen die Überträger der Malaria angewiesen, um eine der weltweit wichtigsten Infektionskrankheiten einzudämmen.

