Forschungsbericht 2009 - Max-Planck-Institut für Biologie Tübingen
Die Anfänge der Embryonalentwicklung von Arabidopsis
Abt. 5 Zellbiologie (Prof. Dr. Gerd Jürgens)
MPI für Entwicklungsbiologie, Tübingen
Besonderheiten der pflanzlichen Embryonalentwicklung
Vielzellige Organismen entwickeln sich aus einer einzelnen Zelle (Zygote), die durch die Befruchtung der Eizelle durch ein Spermium entstanden ist. Während der Embryonalentwicklung entstehen aus der Zygote durch Zellteilung viele Zellen, die sich zu verschiedenen Zelltypen differenzieren. Diese Zelltypen sind in einem räumlichen Muster angeordnet, das die charakteristische Körperorganisation des erwachsenen Organismus zumindest in den Grundzügen darstellt. Die molekularen Mechanismen der Musterbildung in der Embryonalentwicklung von Tieren, wie zum Beispiel Drosophila, sind im Detail analysiert worden. Im Gegensatz dazu ist erst in Ansätzen verstanden, wie die Grundzüge der Körperorganisation von Pflanzen, wie beispielsweise Arabidopsis, in der Embryonalentwicklung entstehen. Es ist anzunehmen, dass daran andere molekulare Mechanismen beteiligt sind, da Pflanzen und Tiere in der Evolution unabhängig voneinander aus einzelligen Vorfahren hervorgegangen sind.
Die Embryonalentwicklung der Blütenpflanzen weist einige Besonderheiten auf. So gibt es eine doppelte Befruchtung, bei der zwei genetisch identische weibliche Keimzellen (Eizelle, Zentralzelle) in einer Samenanlage von zwei genetisch identischen Spermien eines Pollens befruchtet werden. Die befruchtete Zentralzelle bringt das Endosperm hervor, das zur Ernährung des Embryos beiträgt. Die befruchtete Eizelle bildet nicht nur den Embryo, sondern auch eine extra-embryonale Struktur (Suspensor), die den Embryo im mütterlichen Gewebe der Samenanlage verankert. Die Eizelle verfügt nur über einen geringen Vorrat an Proteinen, die für die Embryonalentwicklung verwendet werden könnten. Die Entwicklung des Pflanzenembryos hängt daher in hohem Maße von der im Embryo selbst stattfindenden Proteinsynthese ab. Der Ausfall einzelner essentieller Proteine mit allgemeinen zellulären Funktionen (house keeping) kann daher zum Abbruch der Embryonalentwicklung führen, während dies bei Drosophila wegen des mütterlichen Vorrats an Proteinen im Ei im Allgemeinen nicht der Fall ist.
Pflanzenzellen sind von einer Zellwand umgeben, weshalb sie ihren Entstehungsort nicht verlassen können. Änderungen in der Gestalt des sich entwickelnden Embryos kommen dadurch zu Stande, dass einzelne Zellen oder Zellgruppen sich unterschiedlich schnell teilen und dass die Orientierung der Zellteilungsebene reguliert wird. Im Vergleich zum gleichaltrigen Embryo anderer Pflanzenarten besteht der Embryo von Arabidopsis thaliana aus wenigen Zellen. Damit verbunden ist ein sehr regelmäßiges Zellteilungsmuster, das auf eine frühe Festlegung von Zellschicksalen hinzudeuten scheint [1]. De facto hängt das Schicksal einer Zelle jedoch nicht von ihrer Herkunft, sondern von ihrer Lage im sich entwickelnden Embryo ab.
Frühe Embryonalentwicklung von Arabidopsis thaliana

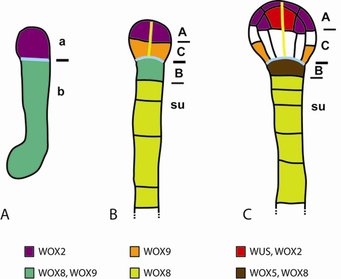
Die Zygote von Arabidopsis thaliana streckt sich in der zukünftigen apikal-basalen Achse und teilt sich asymmetrisch in eine kleinere apikale und eine größere basale Zelle (Abb. 1). Die apikale Zelle wird durch charakteristische Zellteilungen mit wechselnden Orientierungen den Proembryo (das heißt den Embryo ohne die Wurzelspitze) hervorbringen, die basale Zelle durch wiederholte horizontale Zellteilungen einen fädigen extra-embryonalen Suspensor, der den Embryo in der Samenanlage verankert. Nur die oberste Zelle des Suspensors (B, Abb. 1) wird sekundär ein embryonales Schicksal annehmen und die Bildung des Wurzelmeristems initiieren. Damit ist das Muster entlang der apikal-basalen Polaritätsachse mit den Hauptregionen apikal (A), zentral (C), basal (B) und Suspensor (su) etabliert. Quer zur apikal-basalen Achse wird ein radiales Muster aus konzentrisch angelegten Gewebeschichten gebildet [1].
Der Unterteilung der apikal-basalen Achse in der frühen Embryogenese entsprechen Expressionsdomänen von Mitgliedern der WOX-Genfamilie, die Transkriptionsfaktoren kodieren (Abb. 1) [2]. Das spricht dafür, dass Zellen mit verschiedenen Schicksalen sich schon in der Expression von Genen unterscheiden, bevor morphologische Unterschiede zwischen den Zellen sichtbar werden. Allerdings ist noch nicht geklärt, wie es zu diesen charakteristischen dynamischen Expressionsmustern kommt.
Auxin und die Hauptachse der Polarität
Auxin ist das einzige bekannte Pflanzenhormon, das gerichtet transportiert wird. Dieser gerichtete Transport wird durch Auxin-Efflux-Carrier der PIN-Familie bewirkt, die in der Plasmamembran auf einer Seite der Zelle lokalisiert sind und Auxin aus der Zelle „pumpen“. Zwei Mitglieder der PIN-Familie, PIN1 und PIN7, spielen in der frühen Embryogenese eine wichtige Rolle [3]. Nach der Teilung der Zygote wird PIN7 in der basalen Tochterzelle exprimiert und in der Plasmamembran an der Grenze zur apikalen Tochterzelle der Zygote lokalisiert (Abb. 2). Dadurch kommt es zur Akkumulation von Auxin in der apikalen Tochterzelle. Im Experiment wird Auxin nicht direkt, sondern durch auxin-induzierte Reportergenexpression nachgewiesen. Auch die Nachkommen der apikalen Zelle, die zusammen den Proembryo ausmachen, akkumulieren Auxin. In diesen Zellen lokalisiert PIN1 in allen während der Zellteilungen neu gebildeten Plasmamembranen, weshalb Auxin nicht gerichtet zwischen diesen Zellen transportiert wird. Später kommt es zur Neusynthese von Auxin im oberen Teil des Embryos [4]. Wenn der Embryo aus 32 Zellen besteht, werden PIN1 und PIN7 an die basalen Seiten der Zellen umgelagert (Abb. 2C). Dadurch wird der Auxin-Transport nach unten gerichtet, und es kommt zur Akkumulation von Auxin am basalen Ende des Embryos. Diese Verteilung des Auxins bleibt bis zum Ende der Embryonalentwicklung erhalten [3].

Die Auxin-Antwort im jungen Embryo wird durch den Transkriptionsfaktor MONOPTEROS (MP; auch als AUXIN RESPONSE FACTOR 5, ARF5, bezeichnet) und seinen Inhibitor BODENLOS (BDL, alias IAA12) vermittelt [5]. In Abwesenheit von Auxin verhindert der Inhibitor BDL die Aktivierung von auxin-induzierbaren Genen durch MP, während die Akkumulation von Auxin zum Abbau von BDL und damit zur Freisetzung von MP führt [6]. MP und BDL werden zwar nur im Proembryo exprimiert, aber für die Änderung des Schicksals der angrenzenden Suspensorzelle (H, Abb. 2C) benötigt [5]. Diese nicht-autonome Wirkung der Auxin-Antwort wird offenbar durch zwei nachgeschaltete Vorgänge vermittelt. Zum einen sorgt die Freisetzung von MP aus dem Komplex mit seinem Inhibitor BDL dafür, dass PIN1 im Proembryo exprimiert wird. Ein Regulator des Membranflusses, das Protein GNOM, vermittelt die polare Lokalisierung von PIN1 an der Unterseite der Zellen des Proembryos, wodurch Auxin zur obersten Suspensorzelle transportiert wird. Jedoch kann der Ausfall von MP nicht durch die externe Zugabe von Auxin kompensiert werden [5]. Offenbar ist also noch ein anderer MP-abhängiger Prozess beteiligt. Durch eine genomumfassende Suche nach Zielgenen von MP, die nur nach Abbau des Inhibitors BDL exprimiert werden, wurde unter anderem ein Gen identifiziert, das einen Transkriptionsfaktor kodiert, der sich aus dem unteren Bereich des Proembryos in die benachbarte Suspensorzelle bewegt und deren Schicksal dahingehend beeinflusst, dass eine embryonale Wurzel angelegt wird [7]. Anders als bei Tieren können Transkriptionsfaktoren bei Pflanzen von einer Zelle in eine Nachbarzelle transportiert werden.
Die ersten Zellschicksale zu Beginn der Embryonalentwicklung

Wie bereits beschrieben, teilt sich die Zygote von Arabidopsis in zwei verschieden große Zellen, die dann verschiedene Gene exprimieren und verschiedene Zellschicksale annehmen. Die kleinere apikale Zelle bringt durch eine charakteristische Abfolge regulierter Zellteilungen einen kugelförmigen Proembryos hervor, während die größere basale Zelle durch wiederholte horizontale Zellteilungen einen fädigen Suspensor aus wenigen Zellen bildet. Wie diese Unterschiede entstehen, ist nicht bekannt. Denkbar ist, dass noch unbekannte Determinanten durch die asymmetrische Teilung der Zygote ungleich auf die beiden Tochterzellen verteilt werden. Es ist aber auch nicht auszuschließen, dass die Unterschiede zwischen den Tochterzellen erst nachträglich zu Stande kommen. Antworten auf diese Frage werden in unserer Arbeitsgruppe auf verschiedene Weise experimentell gesucht. Ein Ansatz beruht auf der Trennung von fluoreszierenden Zellkernen, die dem Proembryo beziehungsweise dem Suspensor entstammen (Abb. 3). Für die beiden Zellpopulationen werden genomweite Genexpressionsprofile erstellt, und die Regulationssequenzen der Gene werden auf gemeinsame Motive untersucht, um übergeordnete Regulatoren zu identifizieren.