Forschungsbericht 2006 - Max-Planck-Institut für Kolloid- und Grenzflächenforschung
Über das mechanische Design der Holzzellwand
Biomaterialien (Prof. Dr. Peter Fratzl)
MPI für Kolloid- und Grenzflächenforschung, Potsdam
Einleitung
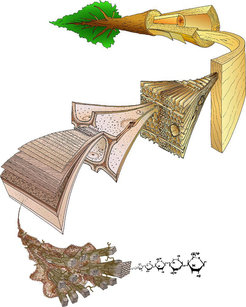
Biologische Materialien wie Knochen, Sehnen oder auch Pflanzengewebe werden zunehmend als wertvolle Vorbilder aus der Natur für das Design neuer bio-inspirierter Werkstoffe gesehen [1, 2]. Allen biologischen Materialien gemein ist ihr hierarchischer Aufbau, d.h., von der Makrostruktur bis hinunter zur Nanostruktur existieren mehrere hierarchische Ebenen, welche im Hinblick auf die Struktur-Funktionsbeziehungen des Organismus eng miteinander verknüpft sind [3] (Abb. 1). Daraus folgt, dass sich kleinste Veränderungen in der Nanostruktur direkt auf die makroskopischen Eigenschaften des Organs auswirken, woraus sich höchst effektive Mechanismen zur Anpassung an veränderliche äußere Bedingungen ergeben. Der entscheidende Unterschied zu herkömmlichen Werkstoffen liegt aber im Wachstum der biologischen Systeme, womit sich eine Vielzahl von erstrebenswerten Eigenschaften verbinden. Hier sind exemplarisch die Fähigkeit zur Anpassung von Struktur und Form und die Fähigkeit zur Selbstheilung bzw. dem Erhalt der strukturellen Integrität nach Schädigung zu nennen. Dies führt zu einem schlankeren Design, welches im Gegensatz zu technischen Konstruktionen nicht bereits im Ansatz alle möglichen Maximallasten berücksichtigen muss.
Die Forschung zur Biomechanik der Pflanzen kann als erster Schritt des biomimetischen Prozesses verstanden werden, da Struktur-Funktionsbeziehungen des Organismus untersucht und allgemeine Prinzipien des Designs in der Natur abgeleitet werden [4]. Die Forschungsgruppe „Plant Systems Biomechanics“ beschäftigt sich dabei hauptsächlich auf der Ebene der Mikro- und Nanostruktur mit dem Aufbau und den Eigenschaften von Zellwänden diverser Pflanzen und Gewebetypen [5]. In diesem Bericht liegt der Fokus auf Bäumen (Nadelbäumen), die aufgrund ihrer relativ homogenen Gewebestruktur und ihres kontinuierlichen adaptiven Wachstums besonders geeignete Untersuchungsobjekte sind.
Struktur und Eigenschaften der Holzzellwand
Der Stamm dient dem Baum vor allem dazu, die Krone in möglichst großer Höhe zu bilden, um sich in Konkurrenz um Licht einen Vorteil zu verschaffen. In diesem Sinne ist der Stamm für den Baum Stütze und zugleich Transportweg zwischen Wurzel und Krone. Das Holz der Bäume entsteht im Zuge des sekundären Dickenwachstums, wenn durch Zellteilung im Kambium nach innen Holz und nach außen Bast gebildet wird. Dabei ist das Holz hauptsächlich für die Festigung und die Wasserleitung zuständig. Für ein tieferes Verständnis der mechanischen Funktion des Holzes bedarf es im Hinblick auf die hierarchische Strukturierung insbesondere der näheren Beschäftigung mit der mikro- und nanostrukturellen Ebene. Hier sind die Zusammensetzung der Holzzellwand und ihre mechanischen Eigenschaften von besonderem Interesse.
Die Zellwand kann als Faserverbundmaterial charakterisiert werden, bestehend aus steifen Zellulosefibrillen, welche nur wenige Nanometer dick sind sowie einer weichen Matrix aus Hemizellulosen, Pektin oder Lignin [6] (siehe auch Abb. 1). Nachdem eine Holzzelle vom Kambium gebildet wurde, wächst sie zunächst zu ihrer endgültigen Größe und Gestalt. In diesem Stadium umgibt die Zelle lediglich eine so genannte Primärwand. Diese lässt sich aufgrund des Innendrucks der Zelle, der biochemischen Veränderungen und der räumlichen Umorientierung der Zellulosefibrillen im Zellwandgefüge im Zuge des Zellwachstums stark verformen [7]. Sobald die endgültige Größe der Zelle erreicht ist, wird die Sekundärwand, die im Gegensatz zur Primärwand eine strikte Paralleltextur der Zellulose zeigt, aufgelagert. Da die Zellwandauflagerungen von innen erfolgen, kann man sich diesen Vorgang wie das Auftragen mehrerer Tapetenschichten in einen Raum vorstellen. Dabei werden nacheinander drei Sekundärwandschichten gebildet, die sich in ihren Dicken und maßgeblich in der Orientierung der Zellulosefibrillen unterscheiden. Die dominierende Sekundärwandschicht ist die mittlere, auch als Sekundärwandschicht 2 (S2) bezeichnet. Die Neigung ihrer Zellulosefibrillen zur Zellachse (der so genannte Mikrofibrillenwinkel) ist für die mechanischen Eigenschaften des Holzes von entscheidender Bedeutung. Auf diese Weise kann der Baum über die Veränderung der Zellulosefibrillenorientierung seine mechanischen Eigenschaften variieren bzw. anpassen. Ein kleiner Mikrofibrillenwinkel, d.h. eine nahezu longitudinale Ausrichtung der Zellulosefibrillen resultiert in einem steifen, aber recht spröden Holz. Große Mikrofibrillenwinkel führen dagegen zu einem wenig steifen und sehr zähen Holz. Im lebenden Baum lässt sich diese Anpassung eindrucksvoll anhand des Alterungsprozesses zeigen. Da der junge schlanke Stamm vom Wind stark ausgelenkt werden kann, ist sein juveniles Holz sehr zäh, d.h. mit einem großen Mikrofibrillenwinkel ausgestattet. Der ältere Baum hingegen bildet adultes Holz mit einem kleinen Fibrillenwinkel, was ihm die notwendige Steifigkeit bei Windbelastung verschafft.
Deformationen in der Zellwand
Die Mechanik der Zellwand wird maßgeblich von den spezifischen Eigenschaften der Zellwandpolymere, ihrer räumlichen Anordnung und mechanischen Interaktion bestimmt. Durch eine mechanische Beanspruchung von Geweben und einzelnen Zellen bei gleichzeitiger nanostruktureller Beobachtung, beispielsweise mit Röntgenstreumethoden oder spektroskopischen Methoden, kann das Deformationsverhalten des Zellverbundes und einzelner Komponenten mit hoher Auflösung beobachtet werden.
Mikromechanische Tests bei gleichzeitiger Beobachtung im Röntgenstrahl wurden am ESRF (Electron Synchrotron Radiation Facility) in Grenoble durchgeführt [8] (Abb. 2). Messungen an Geweben und einzelnen Zellen mit einem großen Mikrofibrillenwinkel in der Sekundärwand (µ ~ 45°) haben gezeigt, dass sich die Zellulosefibrillen bei einer Zugbeanspruchung „aufrichten“ und sich so der gemessene Fibrillenwinkel verkleinert. Dabei entsteht in der Matrix eine Scherspannung, die ab einem kritischen Wert ein „Fließen“ der Matrix verursacht. Dieser Moment wird im Spannungs-Dehnungsdiagramm im Übergang von einem steilen zu einem flachen Anstieg der Kurve deutlich. Interessanterweise führt im weiteren Verlauf eine Unterbrechung der Dehnung („Stufen“ im Spannungs-Dehnungsdiagramm) bzw. ein zyklisches Be- und Entlasten der Probe erneut zu einem steilen Anstieg der Kurve. Dies zeigt, dass die Probe zwar irreversibel verformt, dabei jedoch nur unwesentlich geschädigt wurde. Eine mögliche Erklärung leitet sich aus der Analogie zum Klettverschluss ab, in diesem Fall jedoch auf der nanostrukturellen Ebene der Biopolymere der Zellwand. Die Zellulosefibrillen sind mit der Matrix über eine Vielzahl von Wasserstoffbrückenbindungen verbunden. Wenn bei der mechanischen Beanspruchung eine kritische Spannung überschritten wird, lösen sich diese Bindungen und die Zellulosefibrillen gleiten aneinander vorbei, was zu einer irreversiblen Verformung führt. Wird die Probe wieder entlastet, können sich die Bindungen erneut ausbilden, allerdings als Brücken zwischen jetzt dauerhaft verschobenen Zellulosefibrillen.
![(a) Spannungs-Dehnungsdiagramm einer feuchten Druckholzprobe der Fichte (Picea abies) mit kurzfristiger Unterbrechung der Dehnung im zweiten Teil der biphasischen Kurve; (b) Simultane Veränderung des Mikrofibrillenwinkels (MFA) [8]; (c) Schematische Darstellung des „Aufrichtens“ der Zellulosefibrillen in der Zellwand.](/393773/original-1293749288.jpg?t=eyJ3aWR0aCI6MjQ2LCJvYmpfaWQiOjM5Mzc3M30%3D--daaf8678f977876a7af8e05d022dc65d7db41214)
Weitere wichtige Erkenntnisse zum Deformationsverhalten der Zellwandpolymere können bei der mechanischen Beanspruchung einzelner Zellen in Kombination mit Raman-Spektroskopie gewonnen werden [9]. Dabei wird eine Verschiebung charakteristischer Banden von polymertypischen Bindungen bei der Zugbeanspruchung beobachtet. Die Verschiebung zu einer kleineren Wellenzahl zeigt beispielsweise an, dass die Bindung gestreckt wird. Eine derartige Reaktion auf die mechanische Beanspruchung ist bei einer für die Zellulose typischen Bindung zu beobachten (Abb. 3). Mit zunehmender Zugspannung verschiebt sich die zugehörige Bandenlage kontinuierlich zu kleineren Wellenzahlen. Beim Bruch der Probe kehrt die Bandenlage sofort zu ihrem Ursprungswert zurück, was darauf schließen lässt, dass eine rein elastische Deformation dieser Bindung stattgefunden hat. Im gleichen Diagramm ist auch der Verlauf der Wellenzahl einer typischen Bande für die Matrixsubstanz Lignin gezeigt, die allerdings nicht verschoben wird.
![Spannungs-Dehnungsdiagramm einer einzelnen Fichtenholzzelle (Picea abies) und der Verlauf charakteristischer Banden, 1097 cm-1 (graue Quadrate) für Zellulose und 1602 cm-1 (schwarze Kreise) für Lignin [9].](/393829/original-1293749526.jpg?t=eyJ3aWR0aCI6MjQ2LCJvYmpfaWQiOjM5MzgyOX0%3D--eb0d66808d0fc744f94f89f4668d6ca289d089b0)
Spannungserzeugung in der Zellwand
Pflanzen können durch Quellen bzw. Schwinden ihrer Zellwände gerichtete Bewegungen ausführen. Bemerkenswerte Beispiele dieses Verformungsprinzips sind der Zapfen der Kiefer [10] oder die Grannen des Weizens [11]. Im lebenden Baum können ähnliche Mechanismen zum Spannungsaufbau in Holzzellwänden und zur gezielten Verformung von Organen genutzt werden.
Die Festigkeit des Holzes bei Beanspruchung auf Druck ist nur halb so groß wie bei Beanspruchung auf Zug. Dies bedeutet, dass bei durch Wind verursachter Biegung des Stammes insbesondere die windabgewandte Seite gefährdet ist. Zur Kompensation dieser strukturellen Schwäche bauen Bäume so genannte Wachstumsspannungen auf. An der Peripherie des Stammes werden die Gewebe unter eine longitudinale Zugspannung gesetzt, sodass die kritischen Druckspannungen bei Biegung geringer ausfallen. Das umgekehrte Prinzip findet sich beim Spannbeton, bei dem der Beton unter eine Druckspannung gesetzt wird, um seine schlechteren Zugeigenschaften zu kompensieren.
Die Vorspannung entsteht bei der Bildung der einzelnen Zellen, die am Ende des Ausdifferenzierungsprozesses sich zu kürzen versuchen. Da dies im Zellverbund nicht möglich ist, wird im gesamten Gewebe eine Zugspannung aufgebaut. Dementsprechend verkürzt sich das Holz in den peripheren Bereichen des Stammes in longitudinaler Richtung, wenn man einen Baum quer zur Faser einschneidet.
Dieser Vorspannungszustand besteht in jedem geraden Stamm. Das Prinzip der Vorspannung ermöglicht es Bäumen aber auch, ihre Organe gezielt auszurichten bzw. die Wuchsrichtung durch ein „Aufkrümmen“ zu verändern. Dabei verfolgen Laub- und Nadelbäume interessanterweise unterschiedliche Strategien. Laubbäume bilden auf der Oberseite von Ästen und schief stehenden Stämmen das so genannte Zugholz, welches aufgrund einer höheren Zugvorspannung als im normalen Holz das Organ aufwärts zieht. Nadelbäume hingegen bilden auf der Unterseite das so genannte Druckholz. Dieses Gewebe versucht sich nicht zu verkürzen sondern in longitudinaler Richtung auszudehnen. Daher entsteht eine Druckspannung, welche das Organ aufwärts drückt.
Die Frage, wie es dem Nadelbaum gelingen kann je nach Bedarf sowohl longitudinale Zug- als auch Druckspannungen zu erzeugen, ist von großem Interesse und beschäftigt Wissenschaftler seit geraumer Zeit.
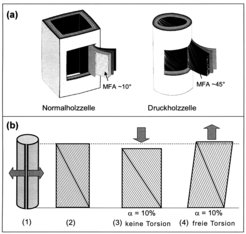
Ausgangspunkt der Überlegungen zur Klärung dieses Phänomens sind Unterschiede in der Nano- und Mikrostruktur zwischen den jeweiligen Zelltypen [12]. Während die Normalholzzellen des geraden Stammes einen annähernd rechteckigen Querschnitt und einen kleinen Zellulosemikrofibrillenwinkel in der dominierenden Zellwandschicht besitzen (µ ~ 10°), haben typische Druckholzzellen einen runden Querschnitt und einen großen Mikrofibrillenwinkel (µ ~ 45°). Zusätzlich können bei einigen Baumarten lumenseitig auch spiralförmig verlaufende Spalten beobachtet werden (Abb. 4a).
Für eine Modellierung des Spannungsaufbaus in beiden Zelltypen wurden folgende vereinfachende Annahmen getroffen: a) das mechanische Verhalten der Zellen wird hauptsächlich von den Sekundärwänden bestimmt; b) die Zellulosefibrillen fungieren als lange, praktisch undehnbare Fasern; c) die Matrix zeigt ein elastisch isotropes Verhalten; und d) ein Quellen des Verbundes führt zu einer isotropen Volumenzunahme.
Die Berechnungen deuten auf interessante geometrische Randbedingungen, falls es im Zuge der Ausdifferenzierung der Zellen zu einem Quellen der Zellwand kommt. Dabei ist vor allem entscheidend, ob die Zell- und Gewebestruktur eine geringe Torsion der einzelnen Zelle erlaubt oder diese komplett ausschließt. Dieser Zusammenhang ist in Abbildung 4b dargestellt. Die Abwicklung der Zellwand ergibt ein Rechteck, welches bei einer Vergrößerung der Fläche rechteckig bleibt, sofern keine Torsion möglich ist. Da die Länge der Diagonale konstant bleiben muss (undehnbare Zellulosefibrille) führt eine Maximierung der Fläche zu einem Quadrat. Dies bedeutet für einen Mikrofibrillenwinkel unter 45° eine Verkürzung in longitudinaler Richtung. Ist jedoch eine geringe Torsion möglich, kann sich das Rechteck in ein Parallelogramm verschieben, was bei einer Flächenvergrößerung zu einer Längenzunahme in longitudinaler Richtung führt.
Die „normalen“ Holzzellen haben einen annähernd rechteckigen Querschnitt, welcher im Zellverbund eine Torsionsbewegung der Einzelzelle unterdrückt. Folglich führt der kleine Mikrofibrillenwinkel zu einer longitudinalen Verkürzung der Zelle, wenn die Matrix gequollen wird. Im Gegensatz dazu könnten der runde Querschnitt und die spiralförmig verlaufenden Spalten für eine Verformung der Druckholzzellen bei Torsion förderlich sein.
Zusammenfassung und Ausblick
Bäume sind hierarchisch aufgebaut und besitzen außergewöhnliche mechanische Eigenschaften. Ein Grund hierfür liegt in der Adaptionsfähigkeit, die nicht nur die äußere Form des Organismus, sondern auch die Anpassung der molekularen Struktur an die natürlichen Anforderungen umfasst. Die Holzzellwand kann als Faserverbundmaterial charakterisiert werden, bestehend aus steifen Zellulosefibrillen, welche nur wenige Nanometer dick sind, sowie einer weichen Matrix aus Hemizellulosen und Lignin. Untersuchungen zum Deformationsverhalten der Zellwand sowie zur Spannungserzeugung in der Zelle haben die Bedeutung der mechanischen Interaktionen der Zellwandpolymere gezeigt. Ziel ist es daher, weitere Untersuchungen am Nanoverbund der Zellwand durchzuführen, um einerseits Optimierungsstrategien der lebenden Pflanze und anderseits das Materialdesign als solches zu ergründen. Die bisher extrahierten Prinzipien des Zellwanddesigns sollen genutzt werden, um den Aufbau von Spannungen in Zellwänden und die Aktuation von Organbewegungen in Pflanzen besser zu verstehen. Das Faser-Matrix-Konzept in Zellwänden kann als Inspiration für einen Transfer in technische Anwendungen dienen: für die Entwicklung anisotroper Hydrogele und für neuartige technische Faserverbundwerkstoffe.

![(a) Spannungs-Dehnungsdiagramm einer feuchten Druckholzprobe der Fichte (Picea abies) mit kurzfristiger Unterbrechung der Dehnung im zweiten Teil der biphasischen Kurve; (b) Simultane Veränderung des Mikrofibrillenwinkels (MFA) [8]; (c) Schematische Darstellung des „Aufrichtens“ der Zellulosefibrillen in der Zellwand. (a) Spannungs-Dehnungsdiagramm einer feuchten Druckholzprobe der Fichte (Picea abies) mit kurzfristiger Unterbrechung der Dehnung im zweiten Teil der biphasischen Kurve; (b) Simultane Veränderung des Mikrofibrillenwinkels (MFA) [8]; (c) Schematische Darstellung des „Aufrichtens“ der Zellulosefibrillen in der Zellwand.](/393773/original-1293749288.jpg?t=eyJ3aWR0aCI6MzQxLCJmaWxlX2V4dGVuc2lvbiI6ImpwZyIsIm9ial9pZCI6MzkzNzczfQ%3D%3D--1eb84867f6c67a4746dfdd16a3b3643566a887ef)
![Spannungs-Dehnungsdiagramm einer einzelnen Fichtenholzzelle (Picea abies) und der Verlauf charakteristischer Banden, 1097 cm-1 (graue Quadrate) für Zellulose und 1602 cm-1 (schwarze Kreise) für Lignin [9]. Spannungs-Dehnungsdiagramm einer einzelnen Fichtenholzzelle (Picea abies) und der Verlauf charakteristischer Banden, 1097 cm-1 (graue Quadrate) für Zellulose und 1602 cm-1 (schwarze Kreise) für Lignin [9].](/393829/original-1293749526.jpg?t=eyJ3aWR0aCI6MzQxLCJmaWxlX2V4dGVuc2lvbiI6ImpwZyIsIm9ial9pZCI6MzkzODI5fQ%3D%3D--5b1aaf615bdcd4632d5acdfe06b1db81a4ef10fd)
