Forschungsbericht 2021 - Max-Planck-Institut für Biochemie
Die Vermessung der tRNA-Welt durch mim-tRNAseq
tRNAs sind die Vehikel für die Translation der genetischen Information und können einzigartige Strukturen aufweisen
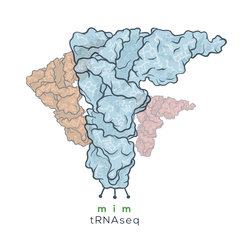
Eine Zelle enthält mehrere hunderttausend tRNA-Moleküle, von denen jedes aus nur 70 bis 90 Nukleotiden besteht. Die tRNAs in ihrer dreidimensionalen Form ähneln einem auf dem Kopf stehenden „L“ (Abb. 1) und tragen an einem Ende eine der zwanzig Aminosäuren, die als Proteinbausteine dienen. Das andere Ende der tRNAs interagiert bei der Translation mit dem für diese Aminosäure komplementären Codon auf der Boten-RNA. Zellen verschiedener Organismen können hunderte von einzigartigen tRNA-Molekülen enthalten, von denen sich einige nur durch ein einziges Nukleotid unterscheiden. Viele Nukleotide in tRNAs sind außerdem mit chemischen Modifikationen versehen, die den tRNAs helfen, sich zu falten oder das richtige Codon zu binden. Bei diesen Modifikationen handelt es sich um eine Vielzahl von möglichen chemischen Abwandlungen der Nukleoside Adenosin, Uridin, Cytidin und Guanosin.
Die Mengen einzelner tRNAs werden in verschiedenen Geweben und während der Entwicklung dynamisch reguliert. Außerdem werden tRNA-Defekte mit neurologischen Erkrankungen und Krebs in Verbindung gebracht. Die molekularen Ursachen dieser Zusammenhänge sind nach wie vor unklar, denn die Quantifizierung der Mengen und die Feststellung vorhandener Modifikationen von tRNAs in Zellen war lange Zeit eine Herausforderung. Wir haben nun die Methode mim-tRNAseq entwickelt, mithilfe derer die Menge und der Modifikationsstatus verschiedener tRNAs genau erfasst werden kann.
Sequenzierung von tRNAs dank einer speziellen Reversen Transkriptase
Um die Mengen mehrerer RNAs gleichzeitig zu messen, verwenden wir das Enzym Reverse Transkriptase, um zunächst RNA in DNA umzuschreiben. Millionen dieser DNA-Kopien können dann parallel durch Hochdurchsatz-Sequenzierung quantifiziert werden. Das Umschreiben von tRNAs in DNA war bisher äußerst anspruchsvoll, da viele tRNA-Modifikationen die Reverse Transkriptase derart blockieren, dass sie keine DNA mehr synthetisieren kann. Viele Forschende haben bereits elegante Lösungen für dieses Problem vorgeschlagen, aber alle beheben nur einen Bruchteil der Modifikationsblockaden in tRNAs.
Uns ist aufgefallen, dass eine bestimmte Reverse Transkriptase viel besser in der Lage zu sein scheint, modifizierte tRNA-Stellen abzulesen. Durch die Optimierung der Reaktionsbedingungen konnten wir die Effizienz dieses Enzyms deutlich verbessern, bis es in der Lage war, fast alle tRNA-Modifikationsstellen abzulesen. Dadurch war es uns erstmals möglich, DNA-Bibliotheken aus tRNA-Kopien in voller Länge zu erstellen und diese für die Hochdurchsatz-Sequenzierung zu nutzen.
Die mim-tRNAseq-Berechnungs-Software
Auch die Analyse der daraus gewonnenen Sequenzdaten stellte eine große Herausforderung dar. Wir haben zwei große Themen identifiziert: Das erste ist die große Sequenzähnlichkeit zwischen verschiedenen tRNA-Transkripten. Das zweite Thema ergibt sich aus der Tatsache, dass bei der reversen Transkription an vielen modifizierten Stellen ein falsches Nukleotid, also eine Fehlinkorporation, eingeführt wird. Beides macht es extrem schwierig, jeden Abschnitt der DNA demjenigen tRNA-Molekül zuzuordnen, aus dem dieser Abschnitt stammt.
Unser Team begegnete diesen Problemen mit neuartigen Berechnungsansätzen, einschließlich der Verwendung von sogenannten Modifikations-Annotationen, um eine genaue „Sequenz-Alinierung“ zu ermöglichen. Bei dieser sogenannten Alinierung werden die Abfolgen von Nukleotiden mit der Sequenz der bekannten Gene im Genom verglichen. So kann der Ursprung der ermittelten Sequenz zu ähnlichen oder gleichen Nukleotidsequenzen gefunden werden. Die von uns entwickelte, automatisierte Software ermöglicht die Alinierung, die Analyse und die Visualisierung von tRNA-Sequenzierungsdaten, und ist frei verfügbar (https://github.com/nedialkova-lab/mim-tRNAseq).
Der Fehlercode
Forschende können mit mim-tRNAseq nicht nur die tRNA-Häufigkeit messen, sondern auch diejenigen tRNA-Modifikationen kartieren und quantifizieren, an denen es, durch die Reverse Transkriptase induziert, zu Nukleotid-Fehlinkorportationen kam. Viele der tRNA-Modifikationen sind für deren Stabilität und Konformation entscheidend, und ebenso für die genaue und effiziente Bindung an das korrekte Codon während der mRNA-Translation.
Wir haben festgestellt, dass die Fehler, die bei der reversen Transkription modifizierter Nukleoside auftreten, nicht zufällig sind. Sie weisen ein Muster auf, das für jeden Modifikationstyp einzigartig ist. Dieser „Fehlercode“ kann zur Vorhersage der Identität von bisher unbekannten Modifikationen verwendet werden. Die Häufigkeit der Fehler entspricht auch direkt der Stöchiometrie jeder Modifikation in den tRNA-Molekülen in der Zelle. So können wir zum Beispiel herausfinden, welche fehlerhaften tRNA-Modifikationen mit neurologischen Erkrankungen in Zusammenhang stehen könnten.
Dank mim-tRNAseq eröffnen sich unzählige und neuartige Forschungsansätze. Wir erwarten, dass viele offene Fragen zur Regulation von tRNAs in gesunden Zellen beantwortet werden können und vor allem diejenigen Mechanismen verständlich macht, die aufgrund fehlerhafter tRNAs Krankheiten auslösen.