Forschungsbericht 2010 - Max-Planck-Institute für experimentelle Medizin
Ionenkanäle als Ziel der Krebstherapie … oder wie man Tumorzellen in den Selbstmord treibt!
Onkophysiologie (Pardo)
Max-Planck-Institut für experimentelle Medizin, Göttingen
Einführung
Ionenkanäle sind Membranproteine, die das Äußere mit dem Inneren einer Zelle verbinden und durch bestimmte Signale den Austausch von elektrisch geladenen Teilchen (Ionen) ermöglichen. Sie stellen auch einen wichtigen Kommunikationsmechanismus zwischen Zellen dar. Die Arbeit der Abteilung beschäftigt sich mit der Struktur und Funktion spannungsabhängiger Ionenkanäle, insbesondere der Kaliumkanäle. Diese Kanäle erlauben einen selektiven Austausch von Kaliumionen, wenn sich die Spannungsdifferenz zwischen dem Zellinneren und dem Zelläußeren verringert. Dies tritt speziell bei erregbaren Zellen, wie z.B. Neuronen oder Muskelzellen auf. Bei einer Erregung fließen Kaliumionen aus der Zelle und sorgen dafür, dass die Membranspannung des Ruhezustands wiederhergestellt wird. Inzwischen sind über 100 verschiedene, durch unterschiedliche Gene kodierte Kaliumkanäle bekannt. Neben der Fähigkeit, die Membranspannung zu beeinflussen, besitzen sie noch weitere Funktionen, wie z. B. die Änderung der Osmolarität und damit die Änderung des Zellvolumens, was bei der Zellteilung von Bedeutung ist. Eag1, ein spannungsabhängiger Kaliumkanal, kommt in den Zellen des zentralen Nervensystems (ZNS) vor, wobei seine physiologische Rolle noch unbekannt ist. Überraschenderweise zeigte sich bei der Analyse von Gewebe aus mehr als 1.200 Biopsien, dass Eag1 außerhalb des ZNS auf über 70% aller untersuchten humanen Tumore zu finden ist [3]. Als Tumormarker wird Eag1 somit zu einem attraktiven Ziel für die Entwicklung neuer Strategien zur Diagnose und Behandlung vieler Krebsarten. In Abbildung 1 sind einige Strategien für die Verwendung von Antikörpern in der Therapie aufgezeigt. Durch die Spezifität des Antikörpers für den Tumormarker wird ermöglicht, dass „normale“ Zellen nicht angegriffen werden.
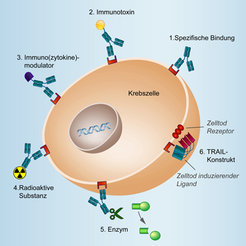
Aktivierung des Selbstmordsignals auf Tumorzellen
Die in Abbildung 1 beschriebene Variante (6) wurde in unserem Labor weiterentwickelt und besteht aus dem Eag1-bindenden Teil eines spezifischen Antikörpers und dem Selbstmord auslösenden Botenstoff TRAIL. TRAIL befindet sich auf verschiedenen Zellen des humanen Abwehrsystems und ist dafür verantwortlich, potenziell schädliche Zellen zu eliminieren [4]. Einige Krebszellen haben eine Resistenz gegen diesen Abwehrmechanismus entwickelt und reagieren nicht auf das Selbstmordsignal, obwohl sie die TRAIL-Rezeptoren auf ihrer Oberfläche haben. Oft ist es für die Abwehrzellen auch nicht möglich, in die Bereiche des Tumors zu gelangen. Durch die Kopplung von TRAIL an einen tumorspezifischen Antikörper wird ein genauer Transport zu den Zielzellen garantiert. Die Verwendung von verschiedenen Chemotherapeutika kann die Auslösung des Zelltods noch verstärken und die Effizienz der Therapie steigern.
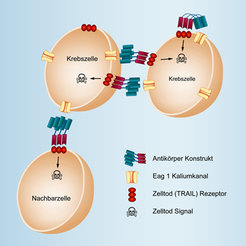
Stark entwickelte Tumore bestehen meist aus verschiedenen Zellen. Mithilfe des von uns hergestellten Konstrukts wird ermöglicht, dass neben den Eag1-positiven Krebszellen auch bei Nachbarkrebszellen, die kein Eag1 tragen, der Zelltod über den TRAIL-Rezeptor induziert wird (Abb. 2). Dadurch wird eine hohe Effizienz gewährleistet, weil möglichst alle vom Krebsgeschehen betroffenen Zellen eliminiert werden. Zellen des ZNS, die auch Eag1 auf der Zelloberfläche tragen, werden nicht angegriffen, weil größere Proteine wie zum Beispiel Antikörper die Blut-Hirn-Schranke nicht überwinden können.
Quantifizierung der zelltötenden Wirkung auf Prostatazellen
Um das hergestellte Konstrukt zu testen, wurden unter anderem verschiedene humane Prostatakrebs-Zelllinien verwendet, die generell resistent gegen konventionelle Therapien sind. Als Kontrollen wurden normale Prostatazellen und Eag1-positive Nicht-Krebszellen verwendet. Die Behandlung der Zellen erfolgte mit dem Konstrukt in Kombination mit einem Chemotherapeutikum. Für die Analyse der Zellen wurde die Methode der Durchflusszytometrie (FACS = Fluorescence Activated Cell Sorting) verwendet. Hierbei fließen Zellen in einzelnen Tröpfchen mit einer hohen Geschwindigkeit an einem Laserstrahl vorbei. Das gestreute oder emittierte Licht des Laserstrahls gibt Aufschluss über die Zellgröße, die Menge granulärer Strukturen in der Zelle und die Färbung einer Zelle. Dadurch ist es möglich, lebende von toten Zellen zu unterscheiden und festzustellen, in welcher Phase des induzierten Zelltods sich die einzelne Zelle befindet. Mithilfe von speziellen Farbstoff-markierten Antikörpern ist es auch möglich, Eag1-Kanäle und TRAIL-Rezeptoren auf der Zelloberfläche zu quantifizieren. Die Experimente haben gezeigt, dass das Antikörper-TRAIL-Konstrukt den Zelltod spezifisch in Eag1-positiven Prostatakrebszellen auslöst, währende normale Prostatazellen und Eag1-positive Nicht-Krebszellen nicht angegriffen wurden. Der Effekt, dass auch Eag1-negative Krebszellen, die sich in der unmittelbaren Nachbarschaft der Eag1-positiven Krebszellen befinden, attackiert und abgetötet werden, konnte ebenfalls nachgewiesen werden.
Ionenkanäle, wie Eag1, die in Tumoren hochreguliert bzw. bei der Krebsentstehung gebildet werden, stellen ein neuartiges Ziel der Tumorbekämpfung dar. Verschiedene Untersuchungen haben ergeben, dass Eag1-Kanäle direkt am Zellwachstum beteiligt sind und vermutlich eine wichtige Rolle bei der Entwicklung von Tumorzellen aus normalen Zellen spielen. Wie dieser Mechanismus funktioniert, ist Gegenstand der aktuellen Forschung in der Abteilung.
Eag1 bietet einen vielversprechenden Ansatz zur Diagnose und der Behandlung von Krebs. Als Membranprotein ist Eag1 von außerhalb der Tumorzelle mit spezifischen Antikörpern zugänglich. Mit der Kopplung eines Eag1-spezifischen Antikörpers an ein Signal, das den Zelltod auslöst, ist es möglich, spezifisch Tumorzellen zu eliminieren. Die Weiterentwicklung dieser Technologie stellt einen vielversprechenden Ansatz für die maßgeschneiderte Behandlung menschlicher Tumore dar.

