Forschungsbericht 2010 - Max-Planck-Institut für Kolloid- und Grenzflächenforschung
Bioorganisch-synthetische Polymere als bioinspirierte Struktur- und Funktionsmaterialien
Max-Planck-Institut für Kolloid- und Grenzflächenforschung, Potsdam
Einführung
Die Natur hat eine Vielfalt an hochentwickelten und raffinierten Systemen, Materialien und Konzepten/Mechanismen hervorgebracht, die für synthetisch-technische Anwendungen von großem Interesse sind. Aus Gründen der Machbarkeit und Wirtschaftlichkeit sind biologische Systeme meist nicht direkt anwendbar, sondern dienen als Inspiration für eine technische Lösung. Ein typisches Beispiel für eine bioinspirierte Anwendung sind strukturierte Oberflächen mit selbstreinigenden Eigenschaften nach dem Vorbild von Lotusblättern (Lotus-Effekt®).
Unsere Inspirationen ergeben sich aus den biologischen Zellmembranen mit ihren spezifischen Wechselwirkungen mit biologischen Systemen, z.B. Proteinen, und aus den hierarchischen Strukturen von Knochen oder Holz, deren Strukturebenen sich über viele Größenordnungen erstrecken (Nanometer → Mikrometer → Meter) und herausragende mechanische Eigenschaften aufweisen. Ziel ist nicht die Rekonstruktion eines biologischen Systems, sondern die vereinfachte oder abstrakte Übertragung in ein synthetisches Polymersystem. Ein Beispiel für die erfolgreiche Umsetzung dieses Konzepts ist NylonTM (DuPont, 1937), ein lange bekanntes, aber erst seit jüngster Zeit als bioinspiriert bezeichnetes Polymer. Weitere bioinspirierte Polymere sind modifizierte Biopolymere (insbesondere Polysaccharide), synthetische Seiden oder Elastine, bioorganisch-synthetische Polymere, etc.
Im Folgenden werden einige Beispiele bioorganisch-synthetischer Polymere als bioinspirierte Funktions- und Strukturmaterialien vorgestellt, mit denen „intelligente“ biofunktionale Polymermembranen oder -partikel und hierarchische Strukturen erhalten werden können.
Synthetische Polymerchemie
Bioorganisch-synthetische Polymere (auch Biohybride oder molekulare „Chimären“) auf der Basis von Peptiden und Sacchariden werden mit möglichst einfachen und effizienten Verfahren hergestellt. Hauptaugenmerk liegt hierbei auf der Anwendung und Entwicklung von metallfreien ionischen Polymerisationsmethoden und photochemischen Polymermodifikationen.
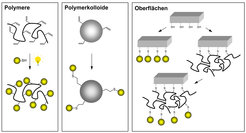
Polypeptide und strukturisomere Poly(N-acyl-ethylenimine) (Pseudopeptide) sind durch ringöffnende Polymerisationen von Aminosäure-N-carboxyanhydriden (Leuchs’sche Anhydride) bzw. heterozyklischen Iminoethern (2-Oxazoline) in größerem Maßstab zugänglich. Speziell eingeführte ungesättigte Seitengruppen, insbesondere Doppelbindungen, können dann photochemisch mit Cystein-, Thiozuckerderivaten oder sonstigen Thiolen weiter umgesetzt werden (Abb. 1). Die photochemische Modifizierung ungesättigter Polymere mit Thiolen verläuft üblicherweise glatt unter milden, mitunter „grünen“ Reaktionsbedingungen (Bestrahlung mit UVA- oder Sonnenlicht bei Raumtemperatur in Wasser als Lösemittel) und erfüllt alle wesentlichen Bedingungen einer Klickreaktion [1, 2].
Abgesehen von Polymeren können mit dieser Methode auch Polymerkolloide und anorganische Oberflächen, beispielsweise Glasfasern und -platten, in Heterophase photochemisch modifiziert werden (Abb. 1) [3, 4].
Bioorganisch-synthetische Polymervesikel
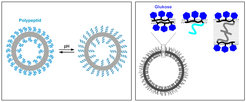
Die hergestellten Polymere mit bioorganischen (Polypeptid oder Zucker/Saccharid) und synthetischen Anteilen (Polybutadien, Polystyrol, oder Polyethylenoxid) bilden in Wasser in der Regel vesikuläre Strukturen im Größenbereich von 0,1-1 Mikrometer aus. Vesikel sind sackartige Strukturen bestehend aus einer molekular dünnen Membran (Abb. 2), ähnlich den aus Phospholipiden aufgebauten biologischen Zellmembranen.
Bei Polymervesikeln mit einer wasserlöslichen Polypeptidschicht, können deren Löslichkeit (geladen oder ungeladen) und Konformation (räumliche Anordnung, Zufallsknäuel oder Helix) durch Änderungen des pH-Wertes der Lösung kontrolliert werden (Abb. 2, links). Durch das Schalten vom geladenen Knäuel in die ungeladene Helix rücken die Polymerketten an der Grenzfläche dichter zusammen, wodurch das Vesikel schrumpft und die Membran weniger durchlässig wird [5]. Dieses System könnte für den Transport und die gezielte Freisetzung medizinischer Wirkstoffe oder als „Vektor“ in der Gentherapie eingesetzt werden.
Polymervesikel mit einer Oberfläche aus Glukose können ebenso in Wasser hergestellt werden [6-8]. Die Dicke der wasserunlöslichen Schicht der Membran kann durch entsprechende Wahl der synthetischen Polymerkomponente im Bereich von ca. 4-20 Nanometern kontrolliert werden. Insbesondere sind Polymervesikel mit einer asymmetrischen Membran, deren Außenseite aus Glukose und die Innenseite aus Polyethylenoxid besteht, zugänglich. Der asymmetrische Aufbau erlaubt es, der äußeren sowie der inneren Schicht unterschiedliche Aufgaben zuzuweisen. So könnten die Polymervesikel in dem Polyethylenoxid Arzneimittel einhüllen und über ihre zuckrige Oberfläche an bestimmten Zellen, wie etwa Tumorzellen, andocken. Derzeit wird versucht, dieses Konzept auf pH- und/oder temperaturempfindliche Polymervesikel und komplexere Oligosacccharide zu erweitern.
Hierarchische Strukturen

Die Bildung von Materialen mit geordneten Strukturen auf mehreren Längenskalen, sogenannte hierarchische Strukturen, gelingt mit Knäuel-Stäbchen-Blockcopolymeren auf der Basis helikaler Polypeptide. Polymerlösungen werden als dünne Filme auf Siliziumplatten aufgeschleudert, im organischen Lösemitteldampf gequollen und einem Selbstorganisationsprozess unterzogen. Es entstehen hoch geordnete Strukturen und auch komplexe Muster im Mikrometer-Längenbereich (Abb. 3) [9]. Die der Bildung dieser Strukturen zugrunde liegenden Mechanismen wurden detailliert untersucht.

Ein anderes hierarchisch strukturiertes Material entsteht bei Kristallisation von Poly(2-isopropyl-2-oxazolin), ein Strukturisomeres des Polyleucins, in verdünnt wässriger Lösung bei Temperaturen oberhalb von +40 °C. Die Struktur besteht üblicherweise aus einheitlich 1-2 Mikrometer großen Kugeln, die wiederum aus kristallinen, etwa 50 Nanometer breiten Nanofasern aufgebaut sind (Abb. 4); der Schmelzpunkt dieses Materials liegt bei nahezu 200 °C. Mechanistische und kinetische Untersuchungen zeigten, dass die Partikel nicht aus einem Nukleationskeim heraus entstehen sondern durch Kollaps eines ausgedehnten Polymernetzwerks [10]. Die Morphologie auf der Mikrometerskala kann durch Zusätze wie organische Lösemittel oder Tenside, also grenzflächenaktive Stoffe, maßgeblich beeinflusst werden.
Die Kristallisation gelingt ebenso bei statistischen Copolyoxazolinen des Poly(2-isopropyl-2-oxazolin)s mit bis zu 10% ungesättigten Seitengruppen. Die erhaltenen hierarchisch strukturierten bzw. porösen Polymerkolloide können mit Thiolen funktionalisiert werden. Derartige Polymerstrukturen werden derzeit für chromatographische Anwendungen und die Herstellung von hierarchisch strukturierten Verbundsystemen mit anorganischen Kristallen bzw. Biomineralien verwendet.
Biofunktionale Systeme
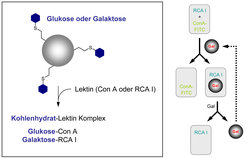
Die mit Zuckereinheiten hergestellten Polymere und Polymerkolloide werden in Vorversuchen auf ihre Wechselwirkungen mit biologischen Systemen, insbesondere mit pflanzlichen Lektinen, untersucht. Lektine sind komplexe Proteine oder Glykoproteine, die spezifische Kohlenhydratstrukturen „erkennen“ und dadurch spezifisch an Zellen bzw. Zellmembranen binden können. Alle Versuche verliefen bislang positiv, und so konnten beispielsweise Galaktose enthaltene kristalline Polymerpartikel zur Trennung eines Gemisches zweier Lektine eingesetzt werden (Abb. 5) [3].
Zusammenfassung und Ausblick
Mit ionischen Polymerisationsmethoden und photochemischen Polymermodifizierungen konnte eine modulare und vielfältig anwendbare Syntheseplattform zur Herstellung neuer bioorganisch-synthetischer Polymere entwickelt werden. Daraus ergeben sich neue Wege zu bioinspirierten Strukturen in Lösung, beispielsweise asymmetrische Glykopolymervesikel, ähnlich den biologischen Zellmembranen, oder komplexe hierarchische Strukturen.
Ein Schwerpunkt weiterer Forschungen soll auf der Entwicklung „intelligenter“ asymmetrischer Glykopolymervesikel liegen. Diese Systeme sind biologischen Zellmembranen ähnlich und sind für Anwendungen in der Biomedizin, sprich den Transport und die gezielte Freisetzung von Medikamenten, äußerst interessant. Weiterhin soll die hierarchische und komplexe Strukturbildung von Polymeren, insbesondere in wässrigen Medien, verfolgt werden. Hierzu sollen Mechanismen aus der Biologie als Vorbild dienen und zudem die Mikrophasenseparation und Kristallisation synthetischer Polymere ausgenutzt werden. Ziel wird es sein, die Symmetrie innerhalb des Systems zu brechen, oder zumindest zu verringern, um dadurch die Bildung größerer Strukturen mit höherer Ordnung einzuleiten. Außerdem sollen die Untersuchungen auf anorganisch-biohybride Systeme erweitert werden, mit dem Fernziel, über die Struktur zu neuen Materialen mit herausragenden Eigenschaften zu kommen („künstlicher Knochen“).




