Optogenetik für die Suche von Wirkstoffen
Lizenzvereinbarung zwischen Max Planck Innovation und Photoswitch Biosciences ist die Basis für neue Plattform zur Suche und Testung neuer Kandidaten für Medikamente
Mit lichtempfindlichen Channelrhodopsin-Proteinen können Wissenschaftler auf völlig neue Weise erforschen, wie die Kandidaten für ein neues Medikament auf kritische Funktionen von Herz- und Nervenzellen wirken. Die von Max-Planck Wissenschaftlern entdeckten Proteine werden dabei in Versuchszellen eingebracht und mit einem Gerät der Firma Photoswitch Biosciences dazu genutzt, die Funktion anderer Ionenkanäle zu steuern. Die Überwachung winziger Spannungsänderungen in der Zelle erlaubt es den Wissenschaftlern, chemische Substanzdatenbanken nach neuen Wirkstoffen zu durchsuchen oder abzuschätzen, wie sicher neue Medikamente für den Einsatz am Menschen sind.
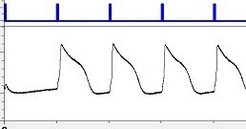
2002 haben Max-Planck-Wissenschaftler Channelrhodopsine erstmals aus Grünalgen des Typs Chlamydomonas reiinhardii isoliert und sowohl im Reagenzglas als auch im lebenden Organismus erfolgreich eingesetzt. Damit lassen sich eine Vielzahl kritischer bioelektrischer Systeme erfolgreich steuern und studieren. Nun entwickelt das amerikanische Unternehmen Photoswitch Biosciences ein komplettes Testsystem für die Wirkstoffsuche und pharmakologische Sicherheitsstudien. Damit können sich die Forscher die Vorteile der auf Channelrhodopsin basierenden optischen Steuerung zu Nutze machen. Das System analysiert die Funktion von Nerven- und Herzzellen deutlich schneller und kostengünstiger als bisherige Methoden.
Die neue Geräteplattform wurde zum Teil auf der Grundlage einer nicht-exklusiven Lizenzvereinbarung mit Max-Planck-Innovation, der Technologietransfer-Organisation der Max-Planck-Gesellschaft, entwickelt, um biologische Fotorezeptoren zu nutzen, um durch Licht aktivierte Ionenkanäle direkt zu steuern.
