Forschungsbericht 2015 - Max-Planck-Institut für Kolloid- und Grenzflächenforschung
Metallische Verstärkung von Proteinen
Metallkoordination in biopolymeren Materialien
Die Natur ist bei der nachhaltigen Entwicklung neuer Materialien der beste Lehrmeister. Inspirierende Vorbilder für neuartige Hochleistungspolymere sind insbesondere Stoffe auf Proteinbasis wie Spinnenseide, Sehnen oder Haare. Erst kürzlich zeigte sich, dass Metallkomplexe basierend auf Zink, Kupfer oder Eisen in biologischen Organismen wie Spinnen, Meereswürmer, Schnecken und Muscheln wichtige mechanische Funktionen übernehmen, indem sie proteinreiche Materialien verstärken [1]. Dabei werden natürliche proteinbasierte Polymere durch koordinative Bindungen mit Metallionen verstärkt. Metallkomplexe entstehen immer dann, wenn freie Orbitale eines Metallions durch Elektronenpaare von einem oder mehreren chemischen Gruppen, den sogenannten Liganden, gefüllt werden. Eine solche Bindung aufzubrechen, ist schwer und fast ebenso energieaufwendig wie eine kovalente Bindung zwischen zwei Atomen. Zwar ist die Metall-Protein-Bindung ähnlich stabil, hat aber einen entscheidenden Vorteil gegenüber der kovalenten: Sie kann sich jederzeit spontan wieder bilden, nachdem sie zerstört wurde. Ziel der Forschungen ist es zu verstehen, wie und warum Organismen diese ungewöhnliche Strategie zur Vernetzung von biopolymeren Materialien verwenden, um diese Methode dann auf Metallopolymere für biomedizinische und technische Anwendungen zu übertragen.
Forscher der Abteilung Biomaterialien untersuchen die Rolle der koordinativen Bindungen von Metalloproteinen in den Byssusfäden von Miesmuscheln. Mit diesen faserigen proteinbasierten Organen heften sich Muscheln in der Küstenregion am felsigen Untergrund fest und trotzen so der Brandung in der Gezeitenzone (siehe Abb. 1).

Die Byssusfäden der Miesmuscheln sind ein ideales Experimentalsystem, da sie unterschiedliche Metallkoordinationsbindungen in verschiedenen Bereichen der Fäden verwenden. Byssusfäden lassen sich in drei morphologisch und funktionell verschiedene Bereiche einteilen: den Stamm, den Faden und die Plaque. Diese unterscheiden sich in Härte, Zähigkeit, Abriebfestigkeit, Haftung und ihrer Fähigkeit zur Selbstheilung. Aktuelle Forschungsergebnisse über die Rolle der Metallkoordination im faserigen Kern und in der Außenhaut der Byssusfäden sollen im Folgenden vorgestellt werden (siehe Abb. 1).
Der faserige Kern der Muschelfäden – ein selbstheilender Stoßdämpfer
Um die brechenden Wellen an steinigen Meeresufern zu überleben, haben die hier ansässigen Organismen verschiedene Strategien entwickelt. Miesmuscheln überstehen diesen ständigen Kampf nur, weil der Kern der Byssusfäden in der Lage ist, die Zugkräfte des Brandungswassers abzuschwächen. Sie funktionieren ähnlich wie ein Stoßdämpfer, der die Schwingungen der gefederten Massen schnell abklingen lässt. Bemerkenswerterweise können die im Faserkern entstandene Schäden von selbst heilen, obwohl dieser nur aus Proteinen besteht und keine lebenden Zellen enthält. Die Hauptbestandteile des Fadenkerns, die auch dessen mechanischen Eigenschaften bestimmen, bilden die kollagenen preCol-Blockcopolymere, die etwa 95 Prozent des distalen Kerns ausmachen. Diese organisieren sich selbst zu einem hoch angepassten halbkristallinen Gerüst (siehe Abb. 2) [2]. Gewöhnlich verwendet die Natur Kollagen dazu, steifes, faseriges Material wie etwa in unseren Sehnen auszubilden und auf diese Weise Kräfte effizient von den Muskeln an die Knochen weiterzuleiten.
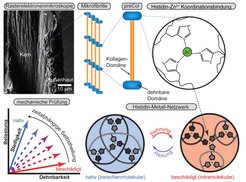
Abb.2: Der faserige Kern der Byssus-Fäden ist in der Lage sich nach mechanischer Beschädigung im Laufe der Zeit selbst zu reparieren. Die Geschwindigkeit der Heilung hängt davon ab, wie schnell sich das dichte Netzwerk der zwischenmolekularen Histidin-Metall-Koordinationsketten erholen kann. Dieses befindet sich in den dehnbaren Domänen an beiden Enden des kollagenen Fadenproteins preCol.
Forschungen am MPI für Kolloid- und Grenzflächenforschung legen nahe, dass die preCols spezielle dehnbare Proteine an beiden Enden der Kollagendomäne einsetzen. Diese Fäden sind härter und zäher als Sehnen und besitzen darüber hinaus die Fähigkeit zur Selbstheilung [2]. Insbesondere terminale Domänen, die für die Metallbindung mit der Aminosäure Histidin angereichert sind, tragen signifikant zur Ausbildung dieser Eigenschaften bei. Dies geschieht durch Histidin-Zink-Koordinationsbindungen (siehe Abb. 2) [3,4].
Mittels moderner analytischer Methoden wurde gezeigt, dass Histidin-Zink-Bindungen ein starkes intermolekulares Netzwerk ausbilden, das bei starker Belastung aufbrechen und Energie dissipieren kann, ohne die Faser dadurch komplett zu zerstören. Diese Bindungen können sich wieder von selbst reparieren, sobald die Fäden keinen Zugkräften mehr ausgesetzt sind und sich im Ruhezustand befinden [3,4]. Diese Erkenntnisse untermauern die kritische Rolle der Histidin-Zink-Koordinationsbindungen für das mechanische Verhalten von Byssusfäden. Des Weiteren können sie Lösungswege für die Entwicklung von selbstheilenden Polymeren aufzeigen.
Die Außenhaut der Muschel-Byssusfäden – eine harte und dehnbare Beschichtung

Abb.3: Die körnige Struktur der Außenhaut, die sowohl hart als auch dehnbar ist, resultiert aus sich abwechselnden Bereichen mit hoher Dichte (Granulat) und niedriger Dichte (Matrix) des DOPA-Metall-Netzwerks.
Die Außenhaut der Muschel-Byssusfäden besteht aus einer harten, proteinbasierten Beschichtung, die den dehnbaren Kern vor Abriebschäden bewegten marinen Umgebung schützen soll (siehe Abb. 3). Das nachzubauen, ist eine besonders schwierige Aufgabe, und es ist noch nicht verstanden, wie sich eine harte Beschichtung auf ein dehnbares Material aufbringen lässt. Harte Materialien sind gewöhnlich nicht biegsam oder dehnbar. Beides ist aber für die Beschichtung der Byssusfäden erforderlich. Die Muschel löst dieses Problem, in dem sie die Außenhaut durch harte Partikel verstärkt. Runde, mikrometergroße Granulatkörnchen sorgen für die nötige Härte, während ein weicheres Matrixmaterial die Dehnbarkeit garantiert (siehe Abb. 3) [5-7].
Literaturhinweise
DOI: 10.1002/anie.201404272
Biomacromolecules 14, 1520-1528. (2013)
DOI: 10.1021/bm4001712
DOI: 10.1021/bm500017u
DOI: 10.1021/acs.biomac.5b00803
Nature Materials, 6(9), 669-672. (2007).
DOI: 10.1038/nmat1956
Science, 328(5975), 216-220. (2010).
DOI: 10.1126/science.1181044
DOI: 10.1039/C4PY01415D
DOI: 10.1073/pnas.1015862108
DOI: 10.1021/ma301791n
Advanced Functional Materials. 22(12) 2519-2528.
DOI: 10.1002/adfm.201200063


